
01
化学方程式相关计算(求生成物 / 反应物质量、质量比);
溶液稀释 / 浓缩计算(求加水 / 加溶质质量、溶质质量分数);
求反应后溶液质量(总质量 - 气体 / 沉淀质量)。


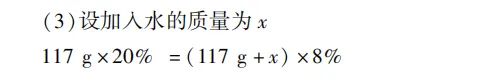


根据化学方程式,直接由相对分子质量得质量比:H₂:Cl₂=2:71(不用算具体量,一步出答案); 先算参加反应的 NaCl 质量 = 117g×20%=23.4g,再根据方程式比例求出生成 NaOH16g、H₂0.4g、Cl₂14.2g; 反应后溶液质量 = 总质量 - 气体质量 = 117g-0.4g-14.2g=102.4g,NaOH 质量分数 = 16g/102.4g×100%≈15.6%;
质量守恒只适用于 质量 ,与体积、分子个数无关;
计算反应后溶液质量,务必减去 逸出的气体 和 生成的沉淀 ;
只关注 参加反应 的物质质量,未反应的不计入守恒关系。

02
物质成分推断(判断生成物 / 反应物的组成);
复杂反应的质量计算(如混合物反应中某元素的质量);
验证化学反应的产物是否完整。

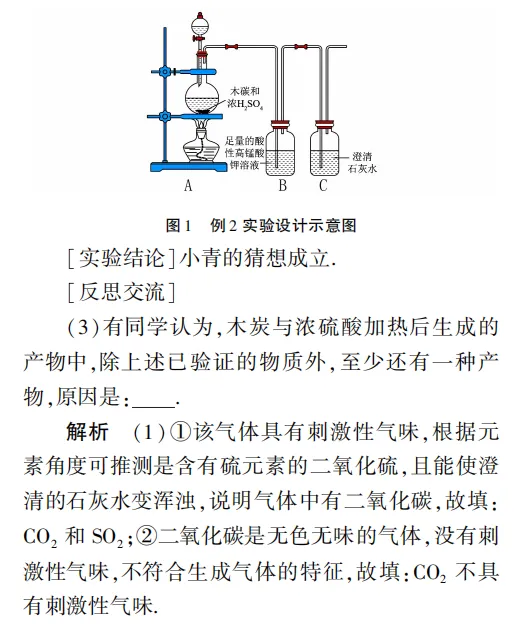


由现象推气体含 SO₂(有刺激性)和 CO₂(使石灰水变浑); 由元素守恒推其他产物:反应物 C 和 H₂SO₄含 C、H、S、O 四种元素,生成的 SO₂和 CO₂只有 C、S、O, 缺少 H 元素 ,故一定还有含 H 的产物(H₂O);
推断题中,先圈出反应物的 所有元素 ,再对比生成物的元素,缺失的元素必然在未验证的产物中;
计算中,先找到某一 守恒元素 ,算出其在反应物中的质量,即为生成物中该元素的总质量,再推导具体物质质量。

03




计算阳离子总正电荷:Na⁺带 1 个正电荷,Al³⁺带 3 个正电荷,总正电荷 = a+3b ; 计算阴离子总负电荷:NO₃⁻带 1 个负电荷,SO₄²⁻带 2 个负电荷,总负电荷 = c+2d ; 根据守恒列等式: a+3b=c+2d 。
离子所带电荷数 = 元素的化合价(如 Mg²+ 带 2 个正电荷,CO₃²- 带 2 个负电荷);
计算总电荷时, 离子个数 × 每个离子所带电荷数 ,再求和相等。

04
第一步:审题定守恒读题后明确题目考查的是 质量、元素、电荷 哪种守恒,圈出守恒的 “不变量”(如总质量、某元素、离子电荷)。 第二步:找量列等式根据守恒类型,找到反应前后不变量的 数量关系 ,列出等式(如溶质质量不变、元素质量不变、正负电荷相等)。 第三步:计算 / 推导得答案

05
质量守恒:化学方程式计算、溶液稀释 / 混合计算、反应后溶液质量分数计算(必考,占计算分值 70%);
元素守恒:物质成分推断、反应物 / 生成物组成判断、混合物中元素质量计算(推断题核心,占推断分值 80%);
电荷守恒:溶液中离子数量关系判断(选填压轴,难度中等,掌握即拿分)。

06

喜欢就点击关注我哦~



文章来源:
四季读书网
版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌抄袭侵权/违法违规的内容, 请发送邮件至23467321@qq.com举报,一经查实,本站将立刻删除;如已特别标注为本站原创文章的,转载时请以链接形式注明文章出处,谢谢!







