一、气体制备(中考实验第 1 核心)
1. 高锰酸钾制氧气
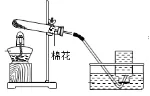
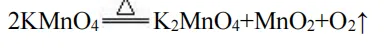
先连接仪器再检查气密性
试管口略向下倾斜:防冷凝水倒流炸裂试管 试管口放棉花:防粉末进入导管 步骤:查、装、定、点、收、移、熄 收集:排水法(纯净)、向上排空气法(干燥) 开始收集: 导管口气泡均匀连续冒出 结束收集:集气瓶口气泡均匀连续冒出 实验完毕时,先移导管后熄灯:防止水槽中的水倒流炸裂试管
氧气的检验方法:将带火星的木条伸入集气瓶中;若木条复燃,证明气体为氧气。
氧气的验满方法:将带火星的木条放在集气瓶口;若木条复燃,证明已收集满。
实验过程中和实验结束后试管炸裂的原因可能有哪些?加热前试管外壁有水;试管口未略向下倾斜;试管底部接触灯芯;停止加热时未将导管从水槽中取出;实验结束后未冷却就洗刷试管;
2. 过氧化氢制氧气
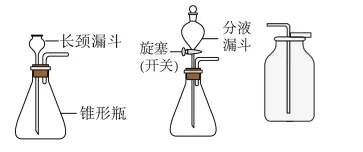
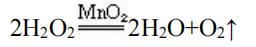
催化剂 MnO₂:可以 改变过氧化氢分解的速率 ,本身的质量、化学性质不变 装置优点:简单、安全、可控制速率 长颈漏斗需液封,便于添加液体药品 分液漏斗:可以控制反应速率
3. 实验室制 CO₂
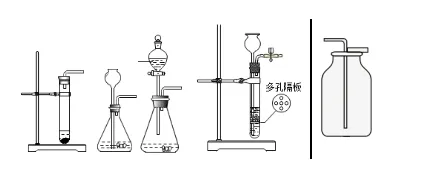
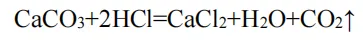
药品:大理石(或石灰石)与稀盐酸 收集:向上排空气法(密度比空气大、能溶于水) 检验:澄清石灰水变浑浊 验满:燃着木条放瓶口熄灭 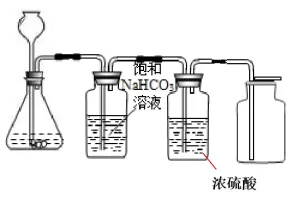
制取的 CO2中混有少量HCl气体(盐酸能挥发出HCl气体)和水蒸气,实验室常将制取的气体先通过饱和 NaHCO3溶液除去HCl气体,再通过浓硫酸除去水蒸气。
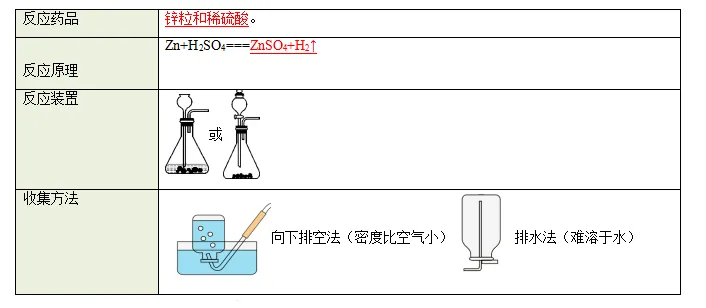
1. 空气中氧气含量测定
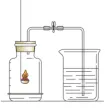
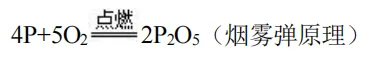
药品:红磷(燃烧生成固体) 现象:红磷燃烧产生大量 白烟,冷却后打开弹簧夹,烧杯内的水 沿导管流入集气瓶,约占 瓶内空气体积的1 /5
结论:O₂约占空气体积 1/5 偏小:红磷不足、装置漏气、未冷却至室温 偏大:点燃伸入过慢、弹簧夹未夹紧
2. 电解水实验
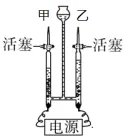
口诀:正氧负氢,体积比 氢二氧一,质量比 氧八氢一 加稀硫酸 / NaOH:增强导电性 结论:水由氢、氧元素组成
3. 分子运动实验
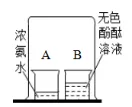
现象:烧杯 B 中溶液变红色,烧杯 A 中溶液不变色。
结论: 分子在不断运动。
该实验说明:浓氨水具有挥发性;氨水能使酚酞溶液变红色;
4. 燃烧条件探究
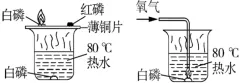
燃烧条件:可燃物、与 O₂接触、温度达着火点 铜片白磷燃、红磷不燃→温度需要达到着火点 水中白磷通 O₂才燃→需要氧气
5. 质量守恒定律

实验1的现象红色的铜变成黑色,气球先膨胀后变瘪。
气球的作用是缓冲压强,防止橡胶塞被冲开。反应后,天平是否平衡?是。
实验2的现象是铁钉表面出现红色固体,溶液由蓝色变浅绿色,
化学方程式 CuSO4+Fe=FeSO4+Fe 。反应后,天平是否平衡?是。
实验3结束后,天平是否平衡?否,原因是反应生成的CO2逸散到空气中。
如何改进装置以验证质量守恒定律在密闭容器中进行实验。
实验4:反应前称量镁条和石棉网质量,反应后称量石棉网和燃烧后得到的产物质量:
①如果测得反应后质量比反应前质量大,原因增加了的氧元素的质量。
②如果测得反应后质量比反应前质量小,原因镁条燃烧时形成白烟逸散到空气中。
③如果测得反应后的质量与反应前总质量相等,原因是增加的氧元素的质量与减少的白烟的质量相等。
如果所选化学反应有气体参加或生成,则反应必须在密闭容器中进行。
6. 金属活动性(Al>Cu>Ag)
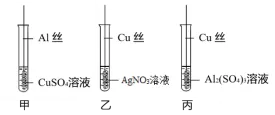
甲中现象:铝丝表面出现红色固体,溶液由蓝色变为无色。
甲实验的铝丝用砂纸打磨的目的是除去表面的氧化膜,化学方程式:2Al+3CuSO4=3Cu+Al2(SO4)3
乙中现象:铜丝表面出现银白色固体,溶液由无色逐渐变蓝色。
通过这个实验可以得到三种金属的活动性顺序是 Al>Cu>Ag ,
其中实验甲或丙(填“甲”“乙”或“丙”)不用做,也可以比较出三种金属的活动性。
7. 铁生锈条件
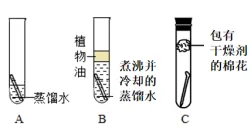
必须同时有:水 + 氧气 防锈:保持干燥、涂油、喷漆、镀金属 煮沸过的蒸馏水的作用是除去水中溶解的氧气
试管B中水面上加一层植物油的作用是防止氧气再次溶解在水中
- 棉花中包有干燥剂无水CaCl2其作用是除去空气中的水蒸气
本期 实验篇(下)11 大必考实验 就整理完啦!
基础操作 + 核心实验全覆盖,中考化学实验题稳稳拿分!
下期我们将带来中考化学冲刺|高频易错实验(必考版)
记得点赞 + 在看 + 关注,不错过每一期提分干货,陪你冲刺中考!






