在中考化学的备考之路上,有一个定律如同一座灯塔,指引着我们理解化学反应的本质——那就是质量守恒定律。它不仅是初中化学的核心基石,更是中考的高频考点(近3年考查频率极高)。很多同学在面对相关题目时,常常感到无从下手,或者容易掉入命题人设置的“陷阱”。
今天,老师就带大家结合历年真题母题,通过图文并茂的方式,深度剖析“质量守恒定律”的理解、验证与应用,帮你一举突破这个高频考点!
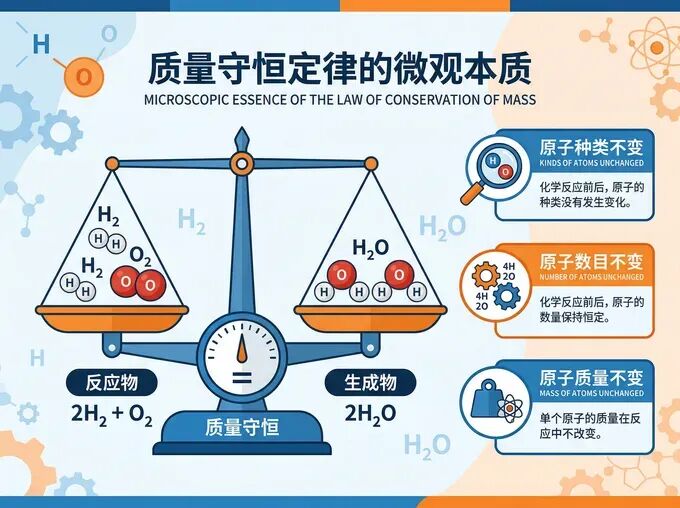
考点一:质量守恒定律的深度理解
很多同学对质量守恒定律的记忆仅停留在“反应前后质量不变”,但这远远不够。要真正掌握它,必须建立清晰的判断逻辑。
1. 判断是否符合质量守恒定律的“三步法”
- 第一步:判断是否发生化学反应。 质量守恒定律只适用于化学变化。物理变化(如冰融化成水、酒精与水混合体积缩小、食盐溶解等)不能用质量守恒定律来解释。 - 第二步:判断是否为“质量”的变化。 该定律强调的是“质量”守恒,不包括体积、分子数目等其他物理量的守恒。 - 第三步:确认守恒的主体。 是“参加化学反应的各物质质量总和”等于“反应后生成的各物质质量总和”。未参与反应的物质(如过量的反应物、杂质、催化剂)不计算在内。 |
【经典解析】
题目: 下列事实符合质量守恒定律的是( ) A. 100g冰受热融化成100g水 B. 50mL水和50mL乙醇混合后总体积小于100mL C. 30g氯化钠固体溶解在100g水中形成130g氯化钠溶液 D. 4.8g镁与3.2g氧气恰好完全反应生成8.0g氧化镁 |
【老师点拨】 A、B、C选项描述的都是物理变化,没有新物质生成,因此不能用质量守恒定律解释。D选项中镁与氧气发生化学反应生成氧化镁,且参加反应的镁和氧气质量之和(4.8g+3.2g)等于生成的氧化镁质量(8.0g),完美契合定律。故选D。
考点二:质量守恒定律中的“变”与“不变”
在化学反应的微观与宏观世界里,有些量是永恒不变的,有些则是必然或可能改变的。牢记“六个不变、两个一定变、两个可能变”,是破解此类题目的关键。
1. 六个“不变”
- 宏观层面: ① 反应前后物质的总质量不变;② 元素的种类不变;③ 元素的质量不变。
- 微观层面: ④ 原子的种类不变;⑤ 原子的数目不变;⑥ 原子的质量不变。
2. 两个“一定改变”
- 宏观层面: 物质的种类一定改变(因为有新物质生成)。
- 微观层面: 分子的种类一定改变(旧分子破裂,新分子生成)。
3. 两个“可能改变”
- 微观层面: 分子的数目可能改变;元素的化合价可能改变。
【避坑指南】 当题目中出现“蜡烛燃烧后质量减小”或“细铁丝燃烧后固体质量增加”时,不要怀疑质量守恒定律。蜡烛燃烧生成的二氧化碳和水蒸气逸散到了空气中;铁丝燃烧时,空气中的氧气参与了反应。如果把逸散的气体或参与反应的气体质量都算上,总质量绝对是守恒的! |
考点三:质量守恒定律的实验验证
如何通过实验来验证这个伟大的定律呢?这里有几个核心原则必须遵守。
1. 验证实验的设计思路
- 必须是化学反应: 实验中必须有新物质生成。
- 现象要明显: 如产生沉淀、气体或颜色变化,便于观察反应是否发生。
- 装置要密闭(关键): 如果反应中有气体参与(如铁丝在氧气中燃烧)或有气体生成(如碳酸钠与盐酸反应生成二氧化碳),实验装置必须完全密闭。否则,气体的逸出或进入会导致称量结果不平衡,从而无法直观验证定律。

2. 常见验证实验对比
- 红磷燃烧实验: 在密闭的锥形瓶中进行,气球的作用是缓冲瓶内气压,防止胶塞弹飞。反应前后天平平衡,能验证。
- 铁与硫酸铜溶液反应: 没有气体参与或生成,在敞口烧杯中进行即可。反应前后天平平衡,能验证。
- 碳酸钠与盐酸反应: 生成二氧化碳气体,如果在敞口烧杯中进行,气体逸散会导致反应后质量减轻,不能直接验证(需改为密闭装置)。
- 镁条在空气中燃烧: 产生白烟(氧化镁固体小颗粒)易逸散,且有空气中的氧气参与,在敞口坩埚中进行会导致称量不准,不能直接验证。
考点四:质量守恒定律的高阶应用
掌握了基础,接下来就是中考中最容易拉开差距的应用题型。
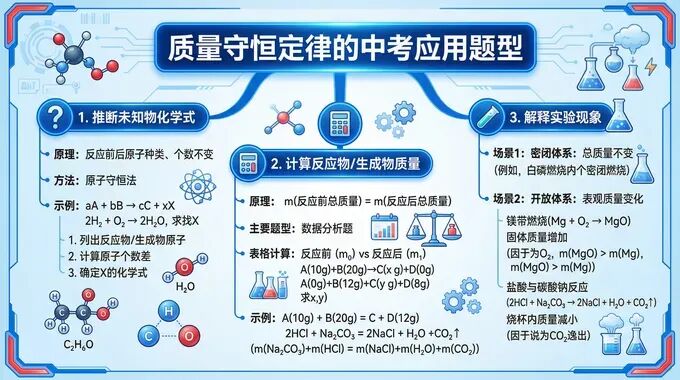
类型一:推断物质的元素组成(定性+定量)
【核心逻辑】 反应前后元素的种类和质量不变。
如果某物质在氧气中燃烧生成了二氧化碳和水,那么:
- 定性分析: 生成物中有C、H、O三种元素。因为氧气只提供O元素,所以该物质中一定含有C、H元素,可能含有O元素。
- 定量计算: 计算出生成的二氧化碳中C元素的质量,以及水中H元素的质量。将这两者相加,如果等于原物质的质量,说明不含O元素;如果小于原物质的质量,差值就是原物质中O元素的质量。
类型二:推断未知物的化学式
【核心逻辑】 反应前后原子的种类和数目不变。
【解题技巧——列表法】
1. 统计反应前各种原子的总数。
2. 统计反应后已知物质中各种原子的总数。
3. 将两者相减,求出差值。
4. 将差值除以未知物的化学计量数,即可得出未知物的化学式。
类型三:密闭容器中的数据分析
此类题目常以表格形式出现,考查数据处理能力。
【解题四步法】
1. 求未知量: 利用反应前后物质总质量相等,求出表格中的待测数据。
2. 定反应物与生成物: 反应后质量增加的物质是生成物;质量减少的物质是反应物。
3. 找催化剂/杂质: 反应前后质量完全不变的物质,可能是催化剂或未参与反应的杂质。
4. 写表达式: 根据反应物和生成物,写出反应的文字或符号表达式,进而判断反应类型(如化合反应、分解反应)。
类型四:微观反应示意图解析
微观示意图是近年来中考的“新宠”,它将抽象的化学反应具象化。
【解题攻略】
1. 去同存异: 观察反应前后是否有完全相同的微观粒子(即未参与反应的过量物质),如果有,先将其“划掉”。
2. 转化化学式: 根据图例,将剩余的微观模型转化为对应的化学式。
3. 写方程式并配平: 根据转化出的化学式,写出完整的化学方程式,并根据微观粒子的个数比例进行配平。
4. 深度分析: 根据配平后的方程式,计算物质质量比、判断反应类型或分析元素化合价的变化。
结语
质量守恒定律不仅是解题的工具,更是我们认识物质世界变化规律的一把钥匙。希望通过这篇推文的梳理,同学们能够建立起清晰的知识框架,在面对中考化学的选择题、推断题或实验探究题时,都能游刃有余。

化学总是学不明白?搞懂这套“化学密码”,化合价、分子式、方程式从此零失误!






