文末可下载填空版
物质的转化与推断
一、解题思路

二、推断题常见的突破口
1. 常见的物质(溶液)和颜色
(1)黑色固体可能是炭粉(C)、铁粉、CuO、MnO2、Fe3O4。
(2)红色固体可能是Cu、Fe2O3;红色单质可能是Cu;暗紫色(紫黑色)固体是KMnO4。
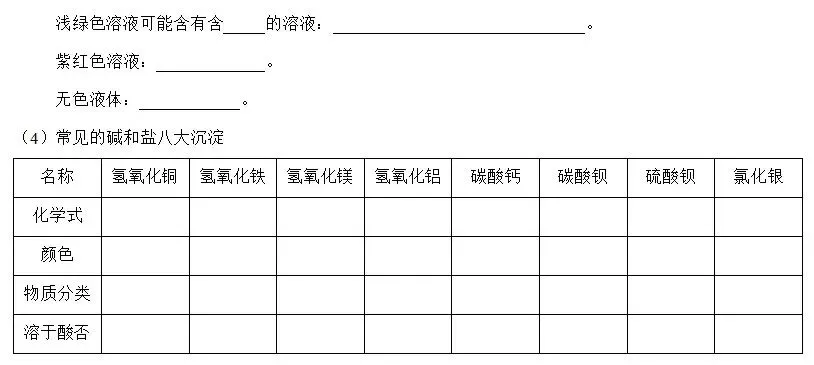
(3)蓝色溶液可能含有含Cu2+的溶液:CuSO4、CuCl2、Cu(NO3)2。
浅绿色溶液可能含有含Fe2+的溶液:FeSO4、FeCl2、Fe(NO3)2。
黄色溶液可能含有含Fe3+的溶液:Fe2(SO4)3、FeCl3、Fe(NO3)3。
紫红色溶液:KMnO4溶液。
无色液体:水、双氧水。
(4)常见的碱和盐八大沉淀
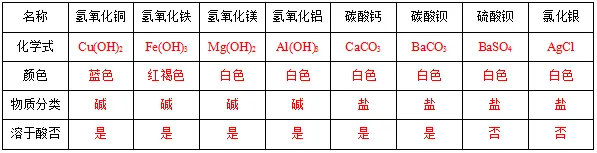
2. 常考物质的俗称
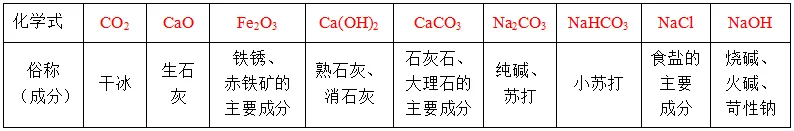
3.物质的性质和用途
(1)能供给呼吸、支持燃烧和用于炼钢的物质:O2。
(2)常用于人工降雨(固体)、灭火、制汽水、作气体肥料的物质:CO2。
(3)可用作燃料、冶炼金属的气体:CO、H2。
(4)可用于金属除锈的物质:稀盐酸、稀硫酸。
(5)可用于焙制糕点、治疗胃酸过多的物质:NaHCO3。
(6)常用作干燥剂的固体物质:CaO、NaOH、无水CaCl2;液体物质:浓硫酸。
(7)可作建筑材料的盐:CaCO3;碱:Ca(OH)2。
(8)溶于水放热,能使酚酞溶液变红,实验室常用其溶液来吸收二氧化碳的物质:NaOH。
(9)微溶于水,常用于检验二氧化碳,还可用于改良酸性土壤的物质:Ca(OH)2。
(10)常用来作生活调味品且医疗上用来配制生理盐水的物质:NaCl。
(11)可广泛用于玻璃、造纸、纺织和洗涤剂的生产,工业制取烧碱的物质:Na2CO3。
(12)实验室制取二氧化碳的原料,也可做补钙剂的物质:CaCO3。
(13)常用作燃料且为最简单的有机物的物质:CH4。
(14)医疗上可用于杀菌消毒,且是实验室最常用的燃料的物质:C2H5OH。
(15)与酸反应产生气泡:金属活动性顺序位于氢前面的金属(如Fe、Zn)、碳酸盐(如Na2CO3、CaCO3)等。
(16)能与碱性物质反应生成有刺激性气味气体的化肥:铵态氮肥(如NH4Cl等)。
(17)可用作调味品的是NaCl。
(18)人体胃液中用于帮助消化的酸是盐酸。
(19)用于治疗胃酸过多的是Al(OH)3、Mg(OH)2和NaHCO3。
(20)可用于实验室检验水的是无水硫酸铜。
4.元素或物质之最
(1)地壳中含量最多的元素是O。
(2)地壳中含量最多的金属元素是Al。
(3)人体中含量最多的元素是O。
(4)人体中含量最多的金属元素是Ca。
(5)形成化合物种类最多的元素是C。
(6)最轻的气体是H2。
(7)天然存在的最硬的物质是金刚石。
(8)生物体内含量最多的物质是H2O。
(9)相对分子质量最小的氧化物是H2O。
(10)最常用的溶剂是H2O。
(11)最理想(清洁)的燃料是H2。
(12)人类最早使用的金属是Cu。
(13)熔点最低的金属是Hg。
(14)导电性最强的金属是Ag。
(13)目前使用最广泛、年产量最高的金属是 Fe 。
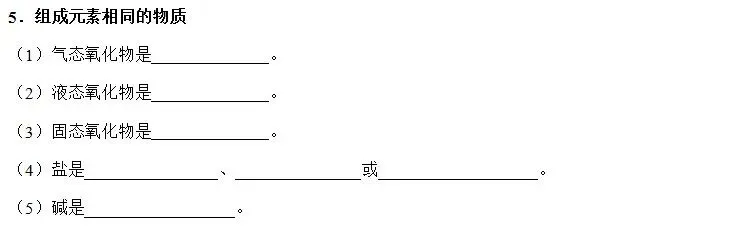
5.组成元素相同的物质
(1)气态氧化物是CO2和CO。
(2)液态氧化物是H2O和H2O2。
(3)固态氧化物是FeO、Fe2O3、Fe3O4。
(4)盐是FeCl2和FeCl3、FeSO4和Fe2(SO4)3或Fe(NO3)2和Fe(NO3)3。
(5)碱是Fe(OH)2和Fe(OH)3。
6.特殊反应条件
(1)点燃:大多数有O2参加的反应。
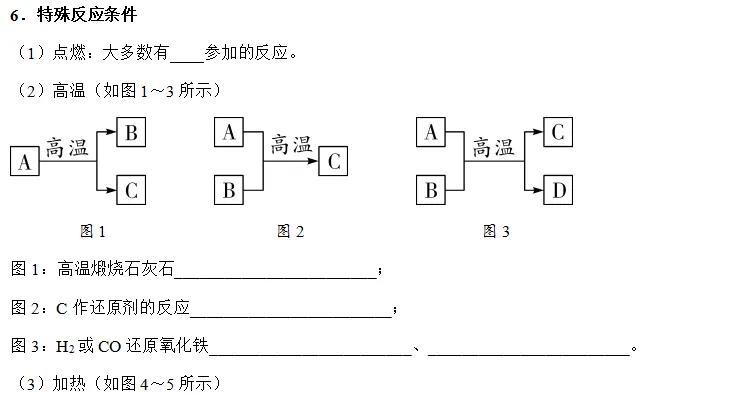
(2)高温(如图1~3所示)
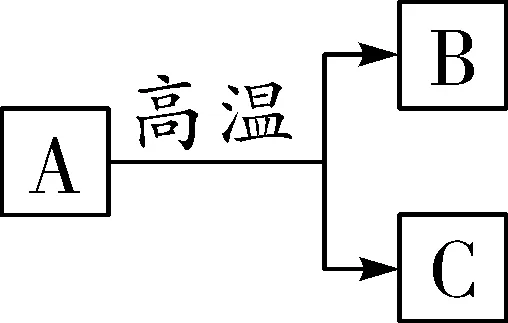 图1
图1
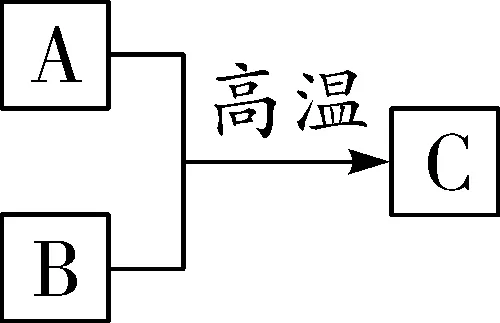 图2
图2
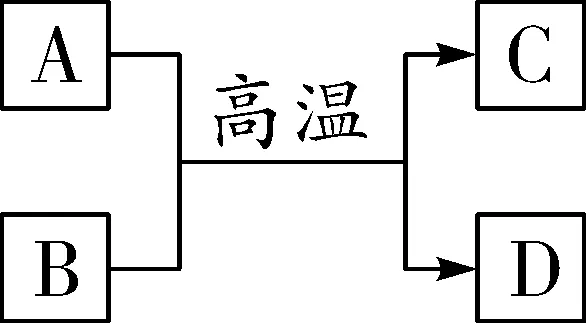 图3
图3
图1:高温煅烧石灰石CaCO3高温CaO+CO2↑;
图2:C作还原剂的反应_CO2+C高温 2CO_;
图3:H2或CO还原氧化铁_3H2+Fe2O3高温2Fe+3H2O_、_3CO+Fe2O3高温 2Fe+3CO2_。
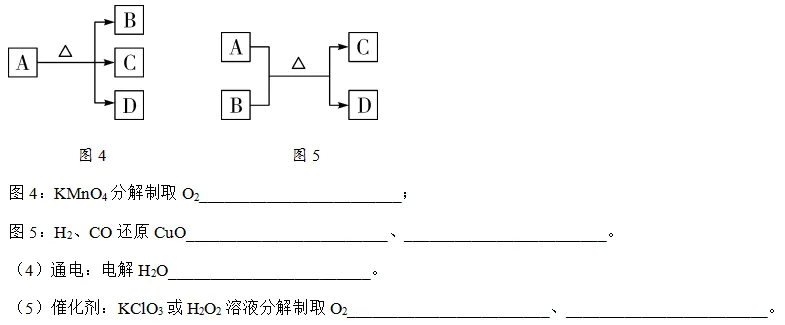
(3)加热(如图4~5所示)
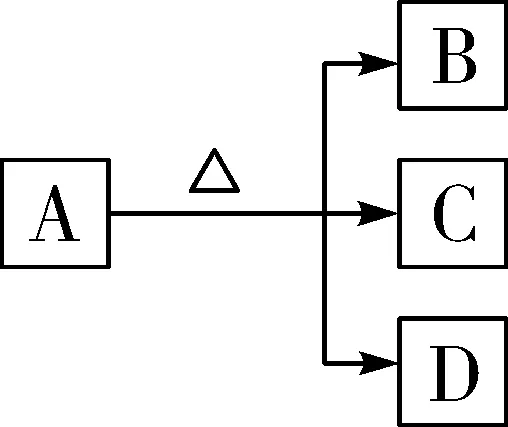
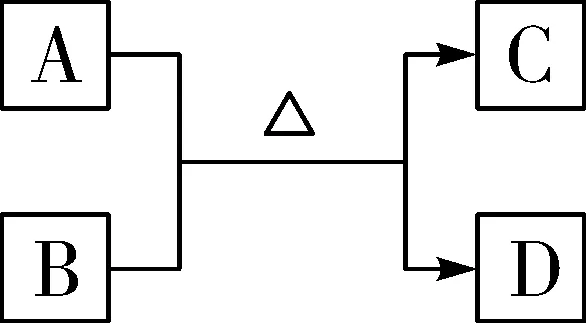
图4图5
图4:KMnO4分解制取O2_2KMnO4△K2MnO4+MnO2+O2↑_;
图5:H2、CO还原CuO_CuO+H2△Cu+H2O_、_CuO+CO△Cu+CO2_。
(4)通电:电解H2O_ 2H2O通电2H2↑+O2↑__。
(5)催化剂:KClO3或H2O2溶液分解制取O2_2KClO3=====MnO2△ 2KCl+3O2↑_、_2H2O2MnO22H2O+O2↑。
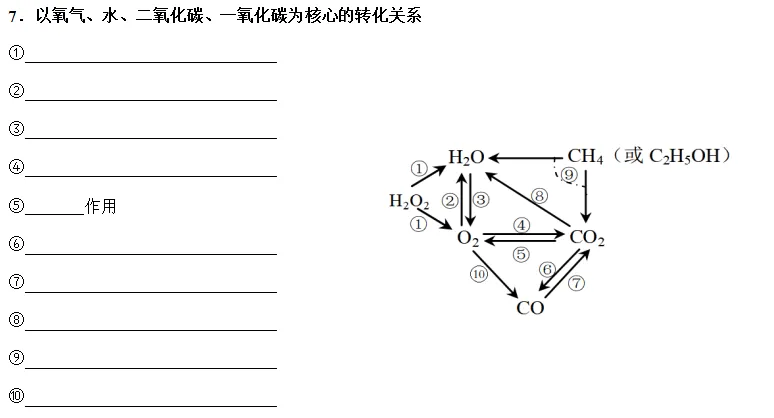
7.以氧气、水、二氧化碳、一氧化碳为核心的转化关系
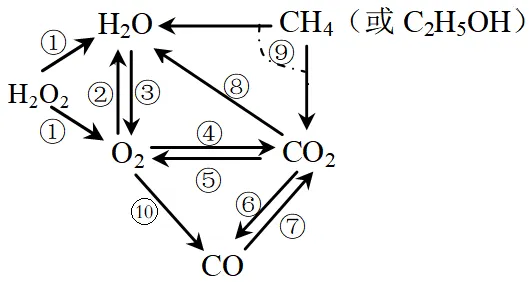
①2H2O2MnO22H2O+O2 ↑
②2H2+O2 点燃 2H2O
③2H2O 通电 2H2↑+O2 ↑
④C+O2 点燃 CO2
⑤光合作用
⑥C+CO2 高温 2CO
⑦2CO+O2 点燃 2CO2或CO+CuO ∆ Cu+CO2
⑧2NaOH+CO2=Na2CO3+H2O
⑨CH4+2O2 点燃 CO2+2H2O、C2H5OH+3O2点燃 2CO2+3H2O
⑩2C+O2 点燃 2CO
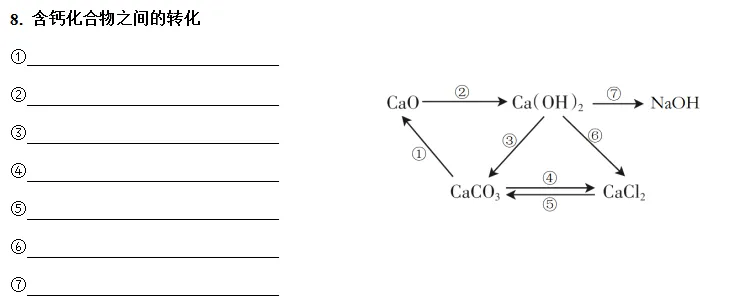
8. 含钙化合物之间的转化
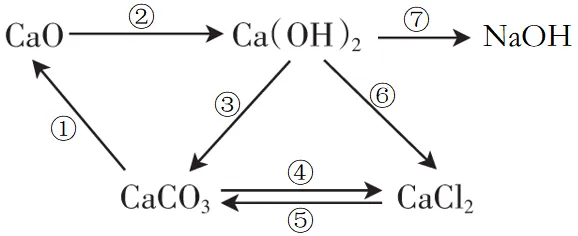
①CaCO3 高温 CaO+CO2↑
②CaO+H2O = Ca(OH)2
③CO2+Ca(OH)2=CaCO3↓+H2O
④CaCO3+2HCl=CaCl2+H2O+CO2↑
⑤CaCl2+Na2CO3= CaCO3↓+2NaCl
⑥Ca(OH)2+2HCl=CaCl2+2H2O
⑦Na2CO3+Ca(OH)2= CaCO3↓+2NaOH
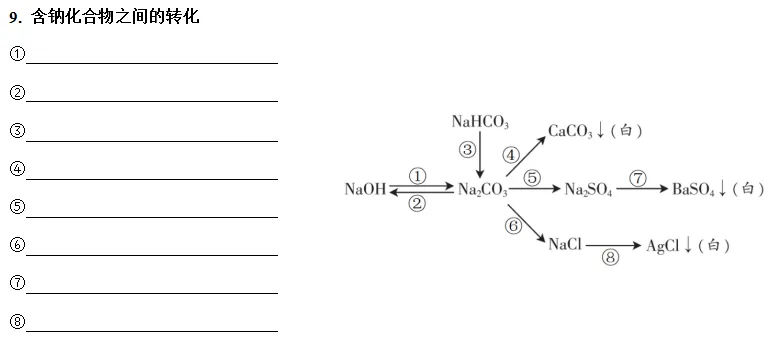
9. 含钠化合物之间的转化
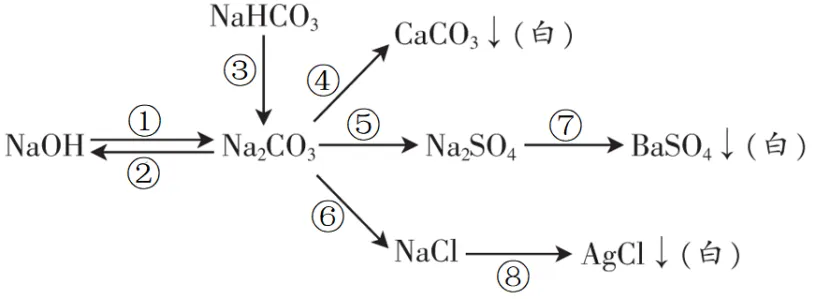
①2NaOH+CO2=Na2CO3+H2O
②Na2CO3+Ca(OH)2= CaCO3↓+2NaOH
③2NaHCO3∆ Na2CO3+H2O+CO2 ↑
④Na2CO3+Ca(OH)2= CaCO3↓+2NaOH
⑤Na2CO3+H2SO4=Na2SO4+H2O+CO2 ↑
⑥Na2CO3+2HCl=2NaCl+H2O+CO2↑或Na2CO3+CaCl2=CaCO3↓+2NaCl
⑦Na2SO4+ BaCl2= BaSO4↓+2NaCl或Na2SO4+ Ba(OH)2= BaSO4↓+2NaOH
⑧NaCl+ AgNO3= AgCl↓+NaNO3
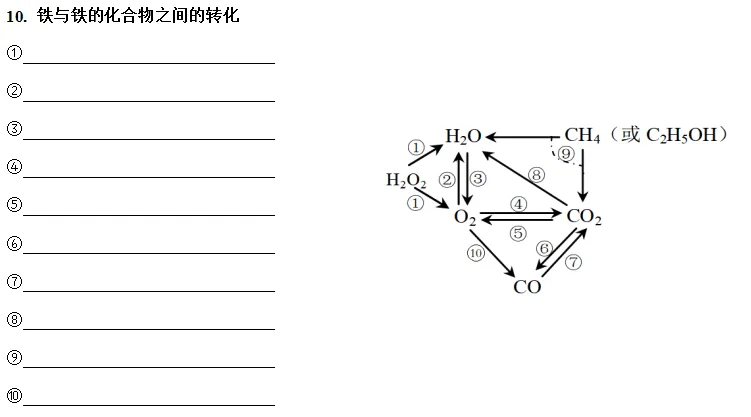
10. 铁与铁的化合物之间的转化
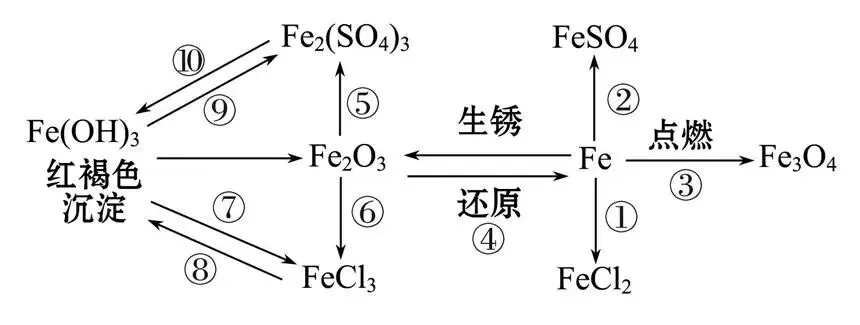
①Fe+2HCl= FeCl2+H2↑
②Fe+H2SO4= FeSO4+H2↑
③3Fe+2O2 点燃 Fe3O4
④Fe2O3+3CO 高温 2Fe+3CO2
⑤Fe2O3+3H2SO4= Fe2(SO4)3+3H2O
⑥Fe2O3+6HCl= 2FeCl3+3H2O
⑦3HCl+Fe(OH)3= FeCl3+3H2O
⑧3NaOH+FeCl3= Fe(OH)3↓+3NaCl
⑨3H2SO4+2Fe(OH)3= Fe2(SO4)3+6H2O
⑩6NaOH+Fe2(SO4)3= 2Fe(OH)3↓+3Na2SO4
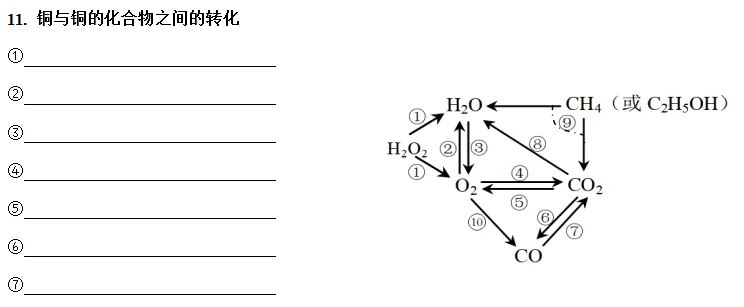
11. 铜与铜的化合物之间的转化
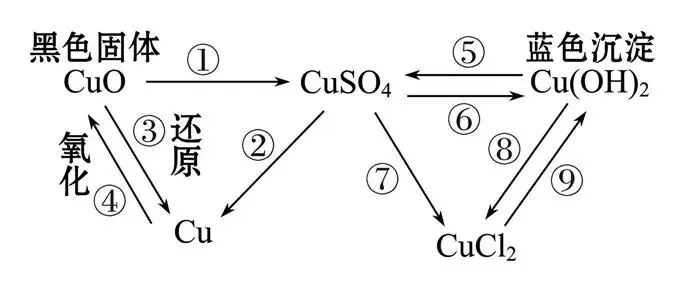
①CuO+H2SO4=CuSO4+H2O
②CuSO4+Fe=FeSO4+Cu
③2CuO+C 高温 2Cu+CO2↑
④2Cu+O2 ∆ 2CuO
⑤Cu(OH)2+H2SO4=CuSO4+2H2O
⑥CuSO4+2NaOH=Cu(OH)2↓+Na2SO4
⑦CuSO4+BaCl2=BaSO4↓+CuCl2
⑧Cu(OH)2+2HCl=CuCl2+2H2O
⑨CuCl2+2NaOH=Cu(OH)2↓+2NaCl





综合来源:简戎资料、途途课堂,仅供学习参考。我们尊重原创,如存在文章/图片/音视频使用不当的情况,请随时与我们联系删除!
【免费领取方式】
点击页面左下角进入公众号首页
发消息专题复习