 期末考试
期末考试
高二化学
可能用到的相对原子质量:H 1C 12N 14O 16Na 23Ti 48
一、单项选择题:共13小题,每题3分,共39分。每题只有一个选项最符合题意。
1. 人形机器人传动关节的材料含有Si、Fe、Cr、Ni等元素,其中不属于第四周期的是
A. Ni B. Fe C. Cr D. Si
2. 反应2H2S+SO2===3S+2H2O可用于制取硫单质。下列说法正确的是
A. H2S的电子式为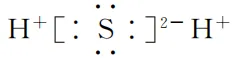 B. SO2分子的空间构型为直线形
B. SO2分子的空间构型为直线形
C. S6、S8、S12等硫单质互为同素异形体D. 冰是含极性键的共价晶体
3. 常温下,Fe(OH)3与KClO在碱性条件下反应可制得K2FeO4。实验室制备K2FeO4的装置(夹持装置未画出)和原理不能达到实验目的的是
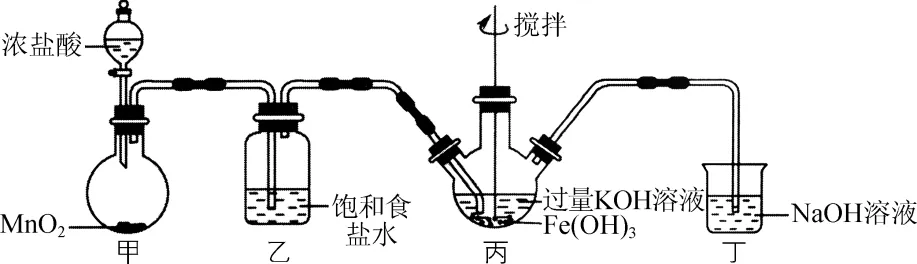
A. 用装置甲制取Cl2B. 用装置乙除去HCl
C. 用装置丙制备K2FeO4D. 用装置丁吸收尾气
4. 硫氰铝镁[MgAl(SCN)5]可作为C2H4聚合反应的催化剂。下列说法正确的是
A. 半径:r(Mg)<r(S) B. 电负性:χ(C)>χ(N)
C. 电离能:I1(N)>I1(S) D. 碱性:Mg(OH)2<Al(OH)3
阅读下列材料,完成5~7题。
Cu和CuCl是许多有机反应的催化剂。Cu可催化反应CO2(g)+3H2(g) CH3OH(g)+H2O(g)ΔH<0,用于制CH3OH。CuCl是一种可溶于浓氨水,难溶于水和乙醇的白色固体,在潮湿的环境中易被氧气氧化为Cu2(OH)3Cl。实验室制备CuCl的过程为:将硫酸铜与氯化钠加水溶解,用盐酸调节酸度,加入铜粉后加热,得到可溶性的配合物Na[CuCl2],再加水稀释、过滤、洗涤、干燥,即得CuCl产品。
CH3OH(g)+H2O(g)ΔH<0,用于制CH3OH。CuCl是一种可溶于浓氨水,难溶于水和乙醇的白色固体,在潮湿的环境中易被氧气氧化为Cu2(OH)3Cl。实验室制备CuCl的过程为:将硫酸铜与氯化钠加水溶解,用盐酸调节酸度,加入铜粉后加热,得到可溶性的配合物Na[CuCl2],再加水稀释、过滤、洗涤、干燥,即得CuCl产品。
A. Cu位于元素周期表的d区
B. NH3中所含键角大于H2O中所含键角
C. [CuCl2]-中Cu+提供孤电子对与Cl-形成配位键
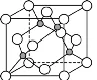
D. CuCl晶胞(如右图所示)中距离每个Cl-最近的Cu+有2个
6. 关于Cu催化CO2制CH3OH的反应,下列说法正确的是
A. 该反应在任意条件下均能自发进行
B. 该反应的平衡常数表达式为K=c(CH3OH)c(CO2)·c3(H2)
C. 反应物所含的键能总和小于生成物所含的键能总和
D. 使用Cu作催化剂可以提高CO2的平衡转化率
7. 下列化学反应表示正确的是
A. Cu在Cl2中燃烧:2Cu+Cl2点燃2CuCl
B. Cu与浓硫酸反应:Cu+H2SO4(浓)===CuSO4+SO2↑+H2O
C. CuCl在潮湿的空气中被氧化:4CuCl+O2+3H2O===2Cu2(OH)3Cl+Cl2
D. CuSO4混合溶液与Cu反应制Na[CuCl2]:Cu2++Cu+4Cl-△2[CuCl2]-
8. 双极膜是一种能将中间层中产生的H+和OH-分离的离子交换膜。一种用双极膜电解法制取NaBrO3和丁二酸的装置如图所示。下列说法正确的是
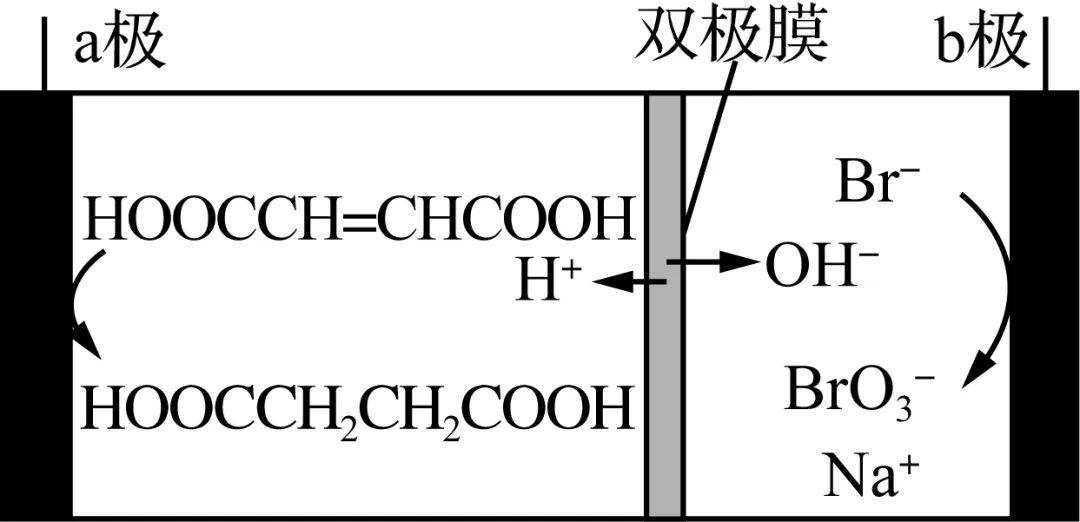
A. b极应与直流电源的负极相连
B. a极上的电极反应为HOOCCH=CHCOOH+2H+-2e- === HOOCCH2CH2COOH
C. 外电路中每转移1 mol电子,双极膜中有1 mol水解离
D. 电解一段时间后,若溶液中Br-不足,则b极处可能有H2产生
9. 化合物Z是一种药物的重要中间体,部分合成路线如下:
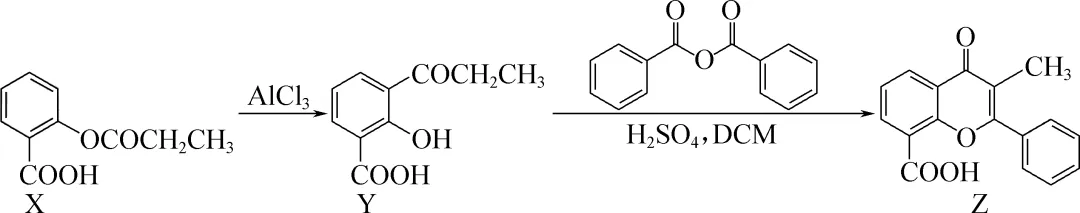
下列说法正确的是
A. X中所有碳原子一定共平面
B.Y、Z可用FeCl3溶液鉴别
C. 1 mol Z最多能与7 mol H2发生加成反应
D. Y能与甲醛发生缩聚反应
10.在给定条件下,下列制备过程涉及的物质转化均可实现的是
A. HCl制备: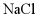 溶液
溶液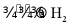 和
和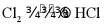
B. 金属Mg制备: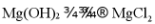 溶液
溶液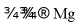
C. 纯碱工业: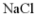 溶液
溶液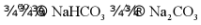
D. 硫酸工业: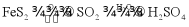
11. 室温下,下列实验探究方案能达到探究目的的是
选项 | 探究方案 | 探究目的 |
A | 将铁锈溶于浓盐酸,滴入KMnO4溶液,观察溶液颜色变化 | 检验铁锈中是否含有Fe2+ |
B | 向K2CrO4溶液中缓慢滴加硫酸,观察溶液颜色变化 | 探究H+浓度对CrO2-4和Cr2O2-7相互转化的影响 |
C | 向NaBr溶液中滴加过量的氯水,再加入淀粉KI溶液,观察溶液颜色变化 | 比较Cl2、Br2和I2的氧化性强弱 |
D | 分别测定浓度均为1.0 mol·L-1 NaHCO3和CH3COONH4溶液的pH | 比较HCO-3与CH3COO-的水解常数大小 |
12.水体中的重金属离子如Cu2+可以通过转化为CuS沉淀除去。已知:室温下Ka1(H2S)=9×10-8,Ka2(H2S)=1×10-12。下列说法正确的是
A. 0.1 mol·L-1Na2S溶液中:c(OH-)=c(H2S)+c(HS-)+c(H+)
B. 0.1 mol·L-1NaHS溶液中:c(Na+)<c(HS-)+2c(S2-)
C.向10 mL 0.001 mol·L-1CuSO4溶液中加入10 mL 0.001 mol·L-1Na2S溶液,有沉淀析出。忽略混合时溶液体积的变化,说明Ksp(CuS)>2.5×10-7
D.当n(CuCl2):n(NaHS)=1:2时,CuCl2溶液与NaHS溶液发生的反应为Cu2++2HS-===CuS↓+H2S↑
13. CO2加氢转化为二甲醚(CH3OCH3)的主要反应(忽略其他副反应)为:
Ⅰ. CO2(g)+3H2(g) CH3OH(g)+H2O(g)ΔH1=-49.1 kJ·mol-1
CH3OH(g)+H2O(g)ΔH1=-49.1 kJ·mol-1
Ⅱ. CO2(g)+H2(g) CO(g)+H2O(g)ΔH2=+41.2 kJ·mol-1
CO(g)+H2O(g)ΔH2=+41.2 kJ·mol-1
Ⅲ. 2CH3OH(g) CH3OCH3(g)+H2O(g)ΔH3=-23.4 kJ·mol-1
CH3OCH3(g)+H2O(g)ΔH3=-23.4 kJ·mol-1
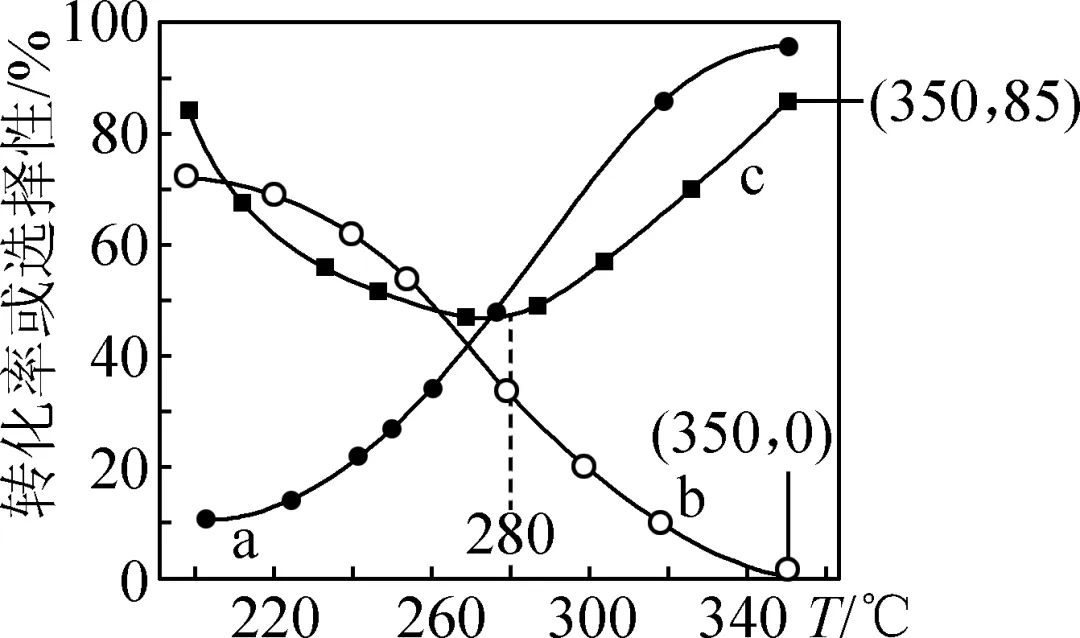
在3.0 MPa的恒压密闭容器中充入5.4 mol H2和2 mol CO2发生上述反应,CO2的平衡转化率、CH3OCH3和CO生成物的选择性随温度变化如图所示。已知:生成物R的选择性=R 物质含有的碳原子数×n(R)参加反应的n(CO2)×100%。下列说法不正确的是
A. 曲线b表示CH3OCH3的选择性
B. 高于280 ℃后,温度对反应Ⅱ的影响程度大于反应Ⅰ
C. 350 ℃,达到平衡时,容器内H2O的物质的量小于1.7 mol
D. 为提高二甲醚的产率,需要研发在低温区的高效催化剂
二、非选择题:共4题,共61分。
14.钪(Sc)是一种在国防、航空航天、核能等领域具有重要作用的稀土元素。以钛白酸性废水(主要含TiO2+、Fe2+、Sc3+)为原料制备Sc及TiO2的工艺流程如下图所示。
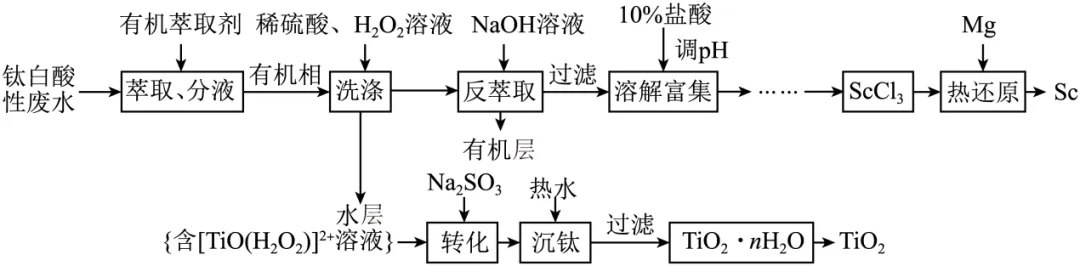
已知:钪与铝元素性质相似,Sc3+易形成配位数为6的配离子。25℃时,Ksp[Sc(OH)3]=1.0×10-30。
(1)基态Ti原子的价层电子排布式为▲。
(2)“洗涤”时,加入H2O2的目的是▲。
(3)“反萃取”时,如果加入的NaOH溶液过量,生成的沉淀会部分溶解,对应的化学方程式为:▲。

通过网盘分享的文件:试卷9
链接: https://pan.baidu.com/s/1Q66FVoGqbl247e5Z218jVQ?pwd=4321 提取码: 4321
--来自百度网盘超级会员v8的分享






