化学中考一轮复习:单元+微专题(Word版)(免费下载)

非常重要:因为微信推荐规则变化,如果不加星标★,慢慢就看不到我们文章推送了。为避免错过好文,请点击上方蓝字“化学阳光驿站”,再点击右上角“……”,将本号设为星标★和“关注”,以后就可以第一时间收到我们的重磅干货文章了(只要星标和关注后就可以看到所有过去的文章啦),分享给更多需要的朋友,供参考交流。
 如:微专题 溶解度曲线及溶解度表分析
如:微专题 溶解度曲线及溶解度表分析
考向一溶解度曲线分析

1、解答此类题目的关键
(1)明确溶解度曲线上点的含义(某点是在某温度时某物质的溶解度是多少g。交点是在某温度时,两物质的溶解度相等。线上方的点表示是饱和溶液,下方的点表示不饱和溶液);
(2)明确物质的溶解度随温度变化的趋势(线越陡,表示该物质溶解度受温度影响较大);
(3)明确饱和溶液中溶质的质量大小的判断方法;
(4)明确判断溶质的质量分数大小关系的方法。
2、溶解度曲线:线的含义:三线:
①“陡升型” :大多数固体物的溶解度随温度升高而升高。如KNO3;
② “缓升型”:少数固体物质的溶解度受温度的影响很小。如NaCl;
③“下降型”:极少数物质溶解度随温度升高而降低。如Ca(OH)2。
3、点的含义:四点:
①曲线上的点:所示某温度下某物质的溶解度是多少(该温度下饱和状态)。
②两曲线的交点:表示在该点所示的温度下,两种物质的溶解度相等。
③线上方的点表示:在该温度下,该溶液是饱和且有部分晶体;
④线下方的点表示:该温度下,该溶液是不饱和溶液。

1. 甲、乙两种物质的溶解度曲线如图所示,下列有关说法错误的是()
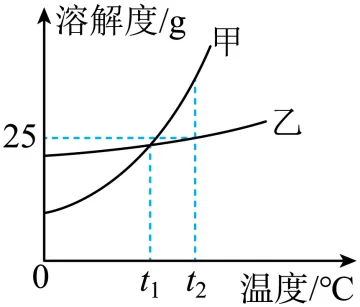
A. 两种物质的溶解度都随温度升高而增大
B. t1°C时,甲、乙两物质的溶液中溶质质量分数一定相等
C. 通常采用蒸发结晶的方法从乙的溶液中获得晶体
D. t2°C时,在100g水中加入25g甲,可形成甲的不饱和溶液
【答案】B
【解析】A. 由溶解度曲线可知,两种物质的溶解度都随温度升高而增大,此选项正确;
B. t1°C时,甲、乙两物质的溶解度相等,则t1°C时,甲、乙两物质的饱和溶液中溶质质量分数一定相等,此选项错误;
C. 乙的溶解度受温度影响不大,对于溶解度受温度影响不大的物质,一般采用蒸发结晶法从溶液中获取晶体,此选项正确;
D. 由溶解度曲线可知,t2°C时,甲的溶解度大于25g,则在100g水中加入25g甲,可形成甲的不饱和溶液,此选项正确。
故选B
2. 气体的溶解度通常指压强为101 kPa和一定温度时,在1体积水里溶解达到饱和状态时的气体体积。如图是甲、乙两种气体在101 kPa时的溶解度曲线,下列说法正确的是
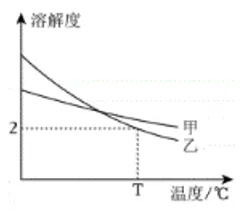
A. 甲的溶解度大于乙的溶解度B. 两种气体的溶解度都随温度升高而增大
C. 甲气体的溶解度受温度的影响小于乙D. T℃时,气体乙的溶解度为2 g
【答案】C
【解析】A、溶解度比较,应指明温度,否则无法比较,不符合题意;
B、由图可知,两种气体的溶解度都随温度升高而减小,不符合题意;
C、由图可知,两种气体的溶解度都随温度升高而减小,且甲的溶解度受温度影响比乙小,符合题意;
D、气体的溶解度通常指压强为101 kPa和一定温度时,在1体积水里溶解达到饱和状态时的气体体积,单位不是“g”,不符合题意。
故选C。
3. 甲、乙、丙三种固体物质的溶解度曲线如下图所示。回答下列问题:
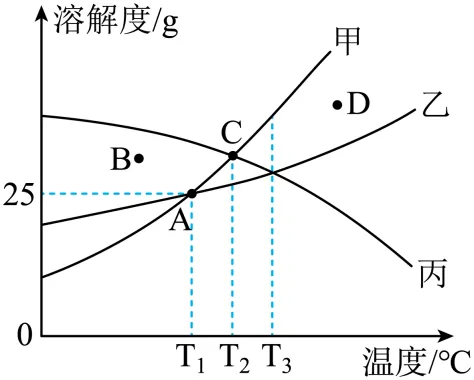
(1)T3℃时,甲、乙、丙的溶解度由大到小的顺序是_______。
(2)甲和乙溶解度相同时,对应的温度是_______。
(3)图中表示甲不饱和溶液的点是_______。
(4)图中与气体溶解度变化规律相似的曲线是_______。
(5)T1℃时,将50g甲放入100g水里,充分溶解,所得溶液的质量为_______g。
【答案】(1)甲>乙=丙
(2)T1℃
(3)D
(4)丙物质的溶解度曲线
(5)125
【解析】(1)据图可知,T3℃时,甲、乙、丙的溶解度由大到小的顺序是甲>乙=丙。
(2)据图可知,T1℃时,甲和乙溶解度相同。
(3)A点、C点位于甲物质溶解度曲线上,表示甲物质溶液恰好饱和;B点位于甲物质溶解度曲线的上方,表示甲物质溶液已经达到饱和,且还有未溶解的固体;D点位于甲物质溶解度曲线的下方,表示的是甲物质的不饱和溶液。故填:D。
(4)气体溶解度随温度升高而减小,据图可知,丙物质的溶解度随温度升高而减小,所以图中与气体溶解度变化规律相似的曲线是丙物质的溶解度曲线。
(5)据图可知,T1℃时,甲物质溶解度是25g,即100g水里最多溶解甲物质25g。所以T1℃时,将50g甲放入100g水里,充分溶解,只能溶解甲25g,所得溶液的质量=100g+25g=125g。
考向二溶解度表分析

1、固体的溶解度
概念 | 固体物质溶解度指的是在 一定温度下 ,某固态物质在 100g溶剂里达到饱和状态时所溶解的质量。 | ||
四要素 | ①、条件:一定温度 ②、标准: 100g溶剂③、状态: 饱和状态 ④、单位:g 。 | ||
影响因素 | 内因 | 溶剂种类、溶质种类; | |
外因 | 温度。 | ||
变化规律 | 大多数固体物质的溶解度随温度升高而升高。 | 如KNO3。 | |
少数固体物质的溶解度受温度的影响很小。 | 如NaCl。 | ||
极少数固体物质的溶解度随温度升高而降低。 | 如Ca(OH)2。 | ||
2、气体的溶解度
概念 | 气体的溶解度是指气体物质在_一定压强_、一定温度下一体积水最多溶解气体的体积分数来表示。 | ||
影响 因素 | 内因 | 溶剂种类、溶质种类; | |
外因 | 温度。 | 在一定压强下,温度越高气体的溶解度越小,温度越低气体的溶解度越大; | |
压强。 | 在一定温度下,压强越大气体的溶解度越大,压强越小气体的溶解度越小 | ||

1. 已知:温度超过35℃时,NH4HCO3开始分解,其溶解度表如下。下列说法正确的是()
温度/℃ | 0 | 10 | 20 | 30 |
NH4HCO3溶解度(g/100g水) | 11.9 | 15.8 | 21.0 | 27.0 |
A. 用NH4HCO3晶体配制浓溶液时,可加热煮沸以加快溶解
B. NH4HCO3是铵态复合肥料,与其它肥料都可以混合使用
C. 20℃时,50.0g蒸馏水就能使11.0g NH4HCO3晶体完全溶解
D. 127.0g NH4HCO3饱和溶液,由30℃降至20℃可析出6.0g晶体
【答案】D
【解析】A、温度超过35℃时,NH4HCO3开始分解。所以用碳酸氢铵晶体配制浓溶液时,不能加热煮沸,以防止碳酸氢铵受热分解,故A错误;
B、复合肥中含有氮、磷、钾元素中的两种及以上的营养元素,而碳酸氢铵中所含有的营养元素只有氮元素,故碳酸氢铵属于氮肥,不是复合肥;铵态氮肥和碱性物质混用时,会有氨气移出,从而降低铵态氮肥肥效,故碳酸氢铵不能和碱性物质混用,故B错误;
C、20℃时碳酸氢铵的溶解度为21.0g,即该温度下100g水中最多溶解碳酸氢铵的质量为21.0g,所以该温度下50g水中对多溶解的碳酸氢铵质量为10.5g<11.0g,故碳酸氢铵晶体不能完全溶解,故C错误;
D、30℃时127.0g 碳酸氢铵饱和溶液中,含有溶质碳酸氢铵质量为27.0g,溶剂水的质量为100g。该饱和溶液由30℃降至20℃时,碳酸氢铵溶解度由27.0g降低到21.0g,所以30℃时127.0g的碳酸氢铵饱和溶液降温到20℃时,可析出6.0g晶体,故D正确;
故选D。
2.化学兴趣小组探究碳酸氢钠、氯化钾、氯化钠和氯化铵的溶解性时,查阅资料如下:
表1物质在不同温度时的溶解度
温度/℃ | 0 | 10 | 20 | 30 | |
溶解度/g | NaHCO3 | 6.9 | 8.2 | 9.6 | 11.1 |
KCl | 27.6 | 31.0 | 34.0 | 37.0 | |
NaCl | 35.7 | 35.8 | 36.0 | 36.3 | |
NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 |
表2溶解度的相对大小(20℃)
溶解度/g | 一般称为 |
<0.01 | 难溶 |
0.01~1 | 微溶 |
1~10 | 可溶 |
>10 | 易溶 |
回答下列问题:
(1)10℃时,NaCl的溶解度为______。
(2)根据20℃时上述四种物质的溶解度,判断其中属于“可溶”的物质是______。
(3)将30℃时上述四种物质的饱和溶液各ag分别降温到0℃,析出同体质量最大的物质是______。
(4)20℃时,将氯化钠和氯化铵各mg分别放入两只烧杯中,再分别加入ng水,充分搅拌。下列说法正确的是______。(填标号)
A. 若两只烧杯中均无固体剩余,则所得氯化铵溶液一定是不饱和溶液
B. 若两只烧杯中均有固体剩余,则所得溶液中溶质的质量分数:氯化铵>氯化钠
C. 若m≤0.36,则所得溶液中溶质的质量分数:氯化铵=氯化钠
D. 若所得溶液中只有一种是饱和溶液,则0.36n≤m≤0.372n
【答案】(1)35.8g
(2)碳酸氢钠或NaHCO3
(3)氯化铵或NH4Cl
(4)AB
【解析】(1)由表1知,10℃时,NaCl的溶解度为35.8g;
(2)20℃时,固体物质的溶解度为1~10g,为可溶,由表1可知,20℃时,NaHCO3的溶解度为9.6g,为可溶;
(3)由表1可知,0℃~30℃氯化铵的溶解度受温度影响最大,所以将30℃时上述四种物质的饱和溶液各ag分别降温到0℃,析出同体质量最大的物质是NH4Cl;
(4)A、20℃时,氯化铵的溶解度比氯化钠的溶解度大,若两只烧杯中均无固体剩余,则所得氯化铵溶液一定是不饱和溶液,故选项说法正确;
B、20℃时,氯化铵的溶解度比氯化钠的溶解度大,若两只烧杯中均有固体剩余,则所得溶液中溶质的质量分数:氯化铵>氯化钠,故选项说法正确;
C、若m≤0.36,由于20℃时,氯化铵的溶解度大于36.0g,氯化钠的溶解度为36.0g,只给了ng水,但不知道具体的量,如果固体全部溶解溶质质量分数相等,但无法判断是否全部溶解,故选项说法错误;
D、20℃时,氯化铵的溶解度为37.2g,氯化钠的溶解度为36.0g,若所得溶液中只有一种是饱和溶液,则饱和溶液一定是氯化钠饱和溶液,氯化铵不饱和,则0.36n≤m<0.372n,故选项说法错误;
故选:AB。

1. 甲、乙两种物质的溶解度曲线如下图所示。下列说法正确的是()
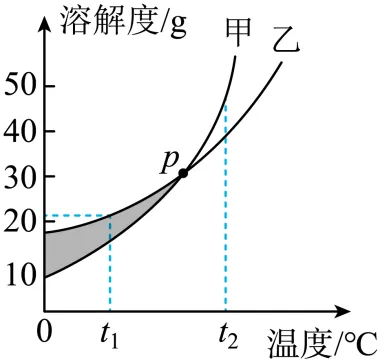
A. 阴影部分的任意点表明甲、乙两种溶液都是饱和溶液
B. P点时,甲、乙两种溶液的溶质质量分数相等
C. t2℃时,在100g水中加入60g甲,形成不饱和溶液
D. t1℃时,甲、乙的饱和溶液升温至t2℃,溶液的溶质质量分数甲>乙
【答案】B
【解析】A、图中阴影部分中的点在甲曲线的上部,是甲的饱和溶液,在乙曲线的下部,是乙的不饱和溶液,故选项说法不正确;
B、由图可知,t1℃时,甲、乙两物质相交于P点,因此P点时,甲、乙两种溶液的溶解度相等,P点表示两溶液的饱和状态,则P点时,甲、乙两种溶液的溶质质量分数相等,故选项说法正确;
C、t2℃时,甲的溶解度为60g,则t2℃时,在100g水中加入60g甲,只能溶解50g甲,形成饱和溶液,故选项说法不正确;
D、甲、乙的溶解度都温度的升高而增大,t1℃时,乙的溶解度大于甲的溶解度,此时溶质的质量分数:乙>甲,将t1℃时,甲、乙的饱和溶液升温至t2℃,溶液都变成不饱和溶液,溶液组成不变,溶质的质量分数不变,则升温至t2℃,溶液的溶质质量分数乙>甲,故选项说法不正确。
故选B。
2. 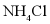 和
和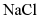 的溶解度曲线如图所示。下列说法中正确的是()
的溶解度曲线如图所示。下列说法中正确的是()

A. 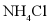 的溶解度比
的溶解度比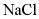 的大
的大
B. 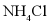 的溶解度受温度的影响比
的溶解度受温度的影响比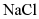 的大
的大
C. 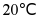 时
时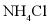 的饱和溶液,升温到
的饱和溶液,升温到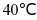 时仍是饱和溶液
时仍是饱和溶液
D. 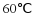 时,在100g水中加入
时,在100g水中加入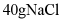 ,形成不饱和溶液
,形成不饱和溶液
【答案】B
【解析】A、由于没有确定温度,不能比较两种物质的溶解度大小,错误;
B、根据溶解度曲线可知,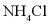 的溶解度曲线较陡,受温度的影响较大,正确;
的溶解度曲线较陡,受温度的影响较大,正确;
C、根据溶解度曲线可知,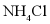 溶解度随温度升高而增大,
溶解度随温度升高而增大,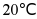 时
时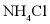 的饱和溶液,升温到
的饱和溶液,升温到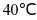 时变成不饱和溶液,错误。
时变成不饱和溶液,错误。
D、根据溶解度曲线可知,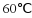 时,NaCl溶解度小于40g,根据溶解度概念可知,
时,NaCl溶解度小于40g,根据溶解度概念可知,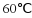 时,在100g水中最多溶解的NaCl质量小于40g,在100g水中加入
时,在100g水中最多溶解的NaCl质量小于40g,在100g水中加入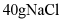 ,形成饱和溶液,错误。
,形成饱和溶液,错误。
故选B。
3. 我国著名化学家侯德榜先生创立了侯氏制碱法,促进了世界制碱技术的发展。 和NaCl的溶解度曲线如下图所示。下列叙述中,不正确的是()(双选)
和NaCl的溶解度曲线如下图所示。下列叙述中,不正确的是()(双选)
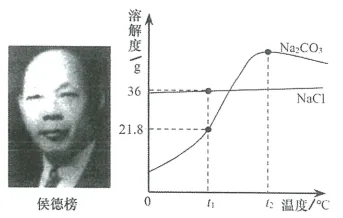
A.  时,NaCl饱和溶液的溶质质量分数为30%
时,NaCl饱和溶液的溶质质量分数为30%
B. 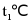 时,将10g
时,将10g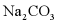 固体放入50g水中,充分溶解后得到溶液的质量为60g
固体放入50g水中,充分溶解后得到溶液的质量为60g
C. 将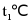 时
时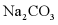 的饱和溶液升温到
的饱和溶液升温到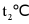 时,溶液的溶质质量分数变大
时,溶液的溶质质量分数变大
D. 当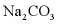 中混有少量NaCl时,可采用冷却热饱和溶液的方法提纯
中混有少量NaCl时,可采用冷却热饱和溶液的方法提纯
【答案】AC
【解析】A、由图可知,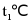 时,NaCl的溶解度为36g,则
时,NaCl的溶解度为36g,则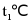 时,NaCl饱和溶液的溶质质量分数为
时,NaCl饱和溶液的溶质质量分数为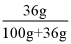 ×100%≈26.5%,故选项说法不正确;
×100%≈26.5%,故选项说法不正确;
B、由图可知,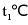 时,
时,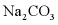 的溶解度为21.8g,则
的溶解度为21.8g,则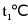 时,将10g
时,将10g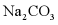 固体放入50g水中,10g
固体放入50g水中,10g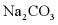 固体全部溶解,所得溶液的质量为50g+10g=60g,故选项说法正确;
固体全部溶解,所得溶液的质量为50g+10g=60g,故选项说法正确;
C、由图可知,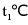 到
到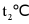 时,
时,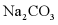 的溶解度随温度的升高而增大,因此将
的溶解度随温度的升高而增大,因此将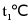 时
时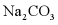 的饱和溶液升温到
的饱和溶液升温到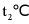 时,溶液变为不饱和溶液,但溶液组成不变,则溶液的溶质质量分数不变,故选项说法不正确;
时,溶液变为不饱和溶液,但溶液组成不变,则溶液的溶质质量分数不变,故选项说法不正确;
D、由图可知,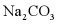 的溶解度受温度影响较大,而NaCl的溶解度受温度影响较小,当
的溶解度受温度影响较大,而NaCl的溶解度受温度影响较小,当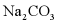 中混有少量NaCl时,可采用冷却热饱和溶液的方法提纯
中混有少量NaCl时,可采用冷却热饱和溶液的方法提纯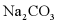 ,故选项说法正确。
,故选项说法正确。
故选AC。
4. 碳酸钠和氯化钠的溶解度曲线如图所示,下列说法错误的是()
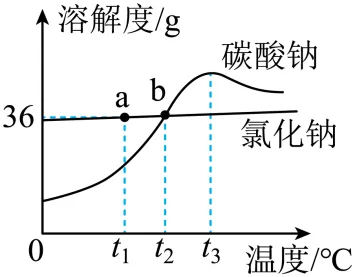
A. 氯化钠的溶解度随温度升高而增大
B. b点表示t2℃时碳酸钠和氯化钠的溶解度相等
C. t1℃时,将20g氯化钠放入50g水中,充分溶解后得到70g溶液
D. t3℃时,可通过升高温度的方法使接近饱和的碳酸钠溶液变为饱和溶液
【答案】C
【解析】A、根据溶解度曲线图分析可知氯化钠的溶解度随温度升高而增大,故选项说法正确;
B、b点为两物质溶解度曲线的交点,则b点可以表示t2℃时碳酸钠和氯化钠的溶解度相等,故选项说法正确;
C、t1℃时,NaCl的溶解度为36g,则此温度下100g水中最多可溶解36gNaCl,50g水中最多可溶解18gNaCl,所以t1℃时,将20g氯化钠放入50g水中,NaCl不能完全溶解,溶液的质量=50g+18g=68g,故选项说法错误;
D、根据溶解度曲线图分析可知当温度高于t3℃时,碳酸钠的溶解度随温度的升高而减小,则t3℃时,可通过升高温度的方法使接近饱和的碳酸钠溶液变为饱和溶液,故选项说法正确。
故选C。
5. 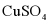 和NaCl的溶解度曲线如图所示。下列说法正确的是()
和NaCl的溶解度曲线如图所示。下列说法正确的是()
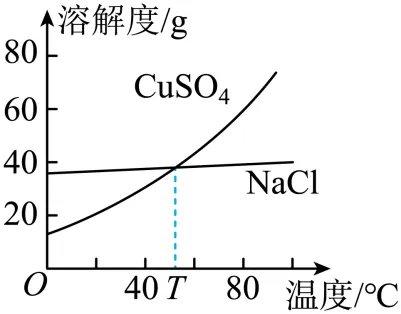
A. 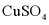 的溶解度一定小于NaCl的溶解度
的溶解度一定小于NaCl的溶解度
B. 升高温度可以降低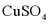 的溶解度
的溶解度
C. T℃时,NaCl和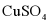 两种饱和溶液溶质的质量分数相等
两种饱和溶液溶质的质量分数相等
D. 分别将等质量80℃的NaCl和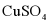 饱和溶液降温至20℃,析出晶体质量NaCl大
饱和溶液降温至20℃,析出晶体质量NaCl大
【答案】C
【解析】A、在0-T℃,NaCl的溶解度大于CuSO4 ,在高于T℃,CuSO4的溶解度大于NaCl,选项错误;
B、CuSO4 的溶解度随温度的升高而增大,选项错误;
C、T℃时,NaCl和 CuSO4的溶解度相等,所以T℃时, NaCl和 CuSO4两种饱和溶液溶质的质量分数相等,选项正确;
D、分别将等质量80℃的NaCl和 CuSO4 饱和溶液降温至20℃,CuSO4溶解度降低更多,析出晶体质量CuSO4大,选项错误;
故选:C。
6. 浓度为10%的氯化钠溶液对葡萄球菌具有明显的抑制效果。下图为配制氯化钠杀菌液的过程,结合图表信息,有关分析正确的一项是()
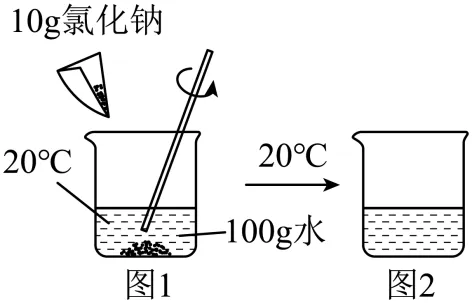
NaCl在不同温度时的溶解度
温度/°C | 0 | 10 | 20 | 30 | 40 | 60 | 80 | 90 | 100 |
氯化钠溶解度/g | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.3 | 38.4 | 39.0 | 39.8 |
A. 图1中搅拌可增大氯化钠的溶解度
B. 图2中溶液为20℃氯化钠的不饱和溶液
C. 图2中溶液对葡萄球菌有明显的杀菌效果
D. 从氯化钠溶液中得到氯化钠均可采用降温结晶的方法
【答案】B
【解析】A、溶解过程中玻璃棒的作用是搅拌,只能加快溶解速率,不能增大氯化钠的溶解度,故选项说法错误;
B、由表中数据可知,20℃时,氯化钠的溶解度是36g,所以该温度下,将10g氯化钠溶解在100g水中得到的是氯化钠的不饱和溶液,故选项说法正确;
C、图2中溶液的浓度为: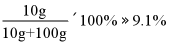 小于10%,所以对葡萄球菌没有明显的杀菌效果,故选项说法错误;
小于10%,所以对葡萄球菌没有明显的杀菌效果,故选项说法错误;
D、氯化钠的溶解度受温度影响变化不大,可以采用蒸发结晶的方法把氯化钠从它的饱和溶液中结晶出来,故选项说法错误。
故选B。
7. 学会从图表中获取关键信息是学习化学的一种重要能力。甲、乙、丙三种固体物质在水中的溶解度曲线如图所示。请据图回答下列问题。
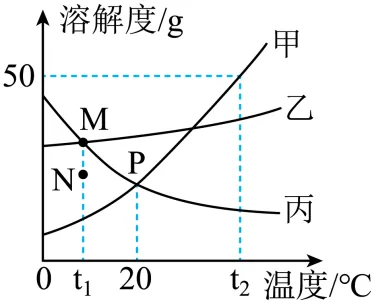
(1)图中P点表示的含义是______。
(2)t1℃时,将丙溶液由N点转化到M点的方法是______。
(3)t2℃时,将30g甲物质加入到50g水中充分溶解后,所得溶液的质量为______g。
(4)t2℃时,甲、乙、丙三种物质的饱和溶液同时降温至t1℃时,所得溶液中溶质质量分数由大到小的顺序为______。
【答案】(1)在 20℃时,甲和丙物质的溶解度相同
(2)加入丙物质(或恒温蒸发溶剂)
(3)75
(4)乙˃丙˃甲
【解析】(1)P点是甲、丙溶解度曲线的交点,表示在 20℃时,甲和丙物质的溶解度相同;
(2)N在丙溶解度曲线下为丙的不饱和溶液,M在丙的溶解度曲线上,表示丙的饱和溶液,对应温度相同则不考虑改变温度。将丙的不饱和溶液变为饱和溶液可以加入丙物质或恒温蒸发溶剂水。
(3)t2℃时甲的溶解度为50g,则50g水最多溶解甲25g,所以将30g甲物质加入到50g水中充分溶解后,所得溶液的质量为50g+25g=75g。
(4)甲、乙溶解度随温度的降低而降低,降温后饱和溶液有晶体析出,仍为饱和溶液。丙溶解度随温度的降低而升高,降温后变为不饱和溶液,溶质质量分数不变。因为t1℃乙的溶解度>t2℃丙的溶解度>t1℃甲的溶解度,所以所得溶液中溶质质量分数由大到小的顺序为乙˃丙˃甲。
8. 如图是硝酸钾、氯化钠固体的溶解度曲线。
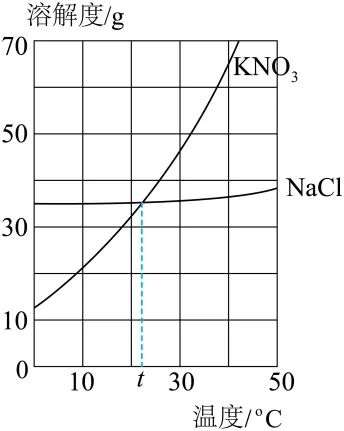
(1)两种物质的溶解度相等时的温度是_____℃;30℃时,30g氯化钠固体加入到100g水中充分溶解,可得到该温度下氯化钠的_____(填“饱和溶液”或“不饱和溶液”)。
(2)10℃时,分别将等质量的硝酸钾、氯化钠的饱和溶液升温到30℃,硝酸钾溶液中溶质的质量_____(填“大于”“等于”或“小于”)氯化钠溶液中溶质的质量。
【答案】(1)①. t②. 不饱和(2)小于
【解析】(1)溶解度曲线的交点表示该温度下,固体物质溶解度相等,由硝酸钾、氯化钠固体的溶解度曲线可知:两种物质的溶解度相等时的温度是t℃;30℃时,氯化钠的溶解度大约36g,该温度下,30g氯化钠固体加入到100g水中充分溶解,可得到该温度下氯化钠的不饱和溶液;
(2)10℃时,硝酸钾的溶解度小于氯化钠的溶解度,且两种物质的溶解度随温度的升高而增大,分别将等质量的硝酸钾、氯化钠的饱和溶液升温到30℃,该过程中溶剂质量不变,溶质质量不变,硝酸钾溶液中溶质的质量小于氯化钠溶液中溶质的质量。
9. 下图是两种固体物质的溶解度随温度变化的曲线图,据图回答:
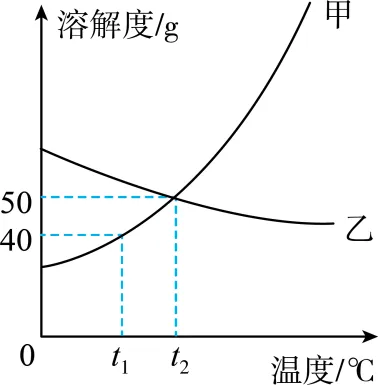
(1)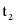 ℃时乙的溶解度是______g。
℃时乙的溶解度是______g。
(2)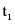 ℃时把30 g物质甲加入到50 g水中充分搅拌,形成的是______溶液(填“饱和”或“不饱和”),升温到
℃时把30 g物质甲加入到50 g水中充分搅拌,形成的是______溶液(填“饱和”或“不饱和”),升温到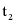 ℃时,溶液的质量是______g。
℃时,溶液的质量是______g。
(3)分别将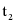 ℃时100 g甲、乙饱和溶液降温到
℃时100 g甲、乙饱和溶液降温到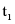 ℃,下列叙述正确的是______。
℃,下列叙述正确的是______。
A. 甲、乙仍是饱和溶液B. 溶剂质量:甲等于乙
C. 溶液质量:甲大于乙D. 溶质质量分数:甲小于乙
【答案】(1)50(2)①. 饱和②. 75(3)BD
【解析】(1)由溶解度曲线图可知,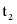 ℃时乙的溶解度是50g,故填:50。
℃时乙的溶解度是50g,故填:50。
(2)由溶解度曲线图可知,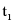 ℃时物质甲的溶解度为40g,℃时50 g水中最多能溶解20g甲物质,所以
℃时物质甲的溶解度为40g,℃时50 g水中最多能溶解20g甲物质,所以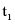 ℃时把30 g物质甲加入到50 g水中充分搅拌,形成的是饱和溶液;物质甲的溶解度随温度的升高而增大,升温到℃时,溶解度为50g,50g水中最多能溶解25g甲物质,一共加入30g甲物质,则溶液质量为:25g+50g=75g。故填:饱和;75。
℃时把30 g物质甲加入到50 g水中充分搅拌,形成的是饱和溶液;物质甲的溶解度随温度的升高而增大,升温到℃时,溶解度为50g,50g水中最多能溶解25g甲物质,一共加入30g甲物质,则溶液质量为:25g+50g=75g。故填:饱和;75。
(3)A.由溶解度曲线图可知,物质甲的溶解度随温度的降低而减小,物质乙的溶解度随温度的降低而增大,分别将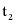 ℃时100 g甲、乙饱和溶液降温到
℃时100 g甲、乙饱和溶液降温到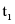 ℃,甲仍是饱和溶液,乙变为不饱和溶液,故A错误;
℃,甲仍是饱和溶液,乙变为不饱和溶液,故A错误;
B.降温过程中,甲、乙溶液中溶剂的质量不变,与 ℃时饱和溶液中溶剂的质量相等,由溶解度曲线图可知,
℃时饱和溶液中溶剂的质量相等,由溶解度曲线图可知,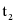 ℃时,甲、乙的溶解度相等,等质量的饱和溶液中所含的溶剂质量相等,分别将
℃时,甲、乙的溶解度相等,等质量的饱和溶液中所含的溶剂质量相等,分别将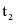 ℃时100 g甲、乙饱和溶液降温到
℃时100 g甲、乙饱和溶液降温到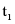 ℃,溶剂质量:甲等于乙,故B正确;
℃,溶剂质量:甲等于乙,故B正确;
C.甲溶液中有晶体析出,溶液质量减小,乙溶液中无晶体析出,溶液质量不变,所以分别将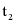 ℃时100 g甲、乙饱和溶液降温到
℃时100 g甲、乙饱和溶液降温到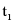 ℃,溶液质量:甲小于乙,故C错误;
℃,溶液质量:甲小于乙,故C错误;
D.由溶解度曲线图可知,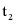 ℃时,甲、乙的溶解度相等,根据饱和溶液溶质质量分数=
℃时,甲、乙的溶解度相等,根据饱和溶液溶质质量分数=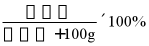 ,可知
,可知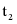 ℃时甲、乙饱和溶液溶质的质量分数相等,分别将
℃时甲、乙饱和溶液溶质的质量分数相等,分别将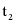 ℃时100g甲、乙饱和溶液降温到
℃时100g甲、乙饱和溶液降温到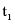 ℃,甲溶液中有晶体析出,溶质质量分数减小,乙溶液中无晶体析出,溶质质量分数不变,所以
℃,甲溶液中有晶体析出,溶质质量分数减小,乙溶液中无晶体析出,溶质质量分数不变,所以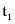 ℃时溶质质量分数:甲小于乙,故D正确。
℃时溶质质量分数:甲小于乙,故D正确。
故选:BD。
10. 下表是硝酸钾和氯化钠在不同温度时的溶解度。根据此表回答:
温度/℃ | 0 | 20 | 40 | 60 | 80 | |
溶解度/g |
| 13.3 | 31.6 | 63.9 | 110 | 169 |
NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 |
(1)两种物质的溶解度受温度变化影响较大的是___________。
(2)40℃时,向两只各盛有100g蒸馏水的烧杯中分别加入50g NaC1和50gKNO3固体,充分溶解,能达到饱和状态的是___________溶液。此时NaCl的溶质质量分数___________ KNO3的溶质质量分数(填“>”“=”或“<”)。
【答案】(1)KNO3##硝酸钾(2)①. NaCl##氯化钠②. <
【解析】(2)由表中数据可知,硝酸钾的溶解度受温度影响比较大。
(2)40℃时,硝酸钾和氯化钠的溶解度分别为63.9g和36.6g,则向两只各盛有100g蒸馏水的烧杯中分别加入50g NaC1和50gKNO3固体,氯化钠能形成饱和溶液,但硝酸钾不能;
但由于形成的氯化钠溶液中,溶质质量只有36.6g,而硝酸钾溶液中,溶质质量为50g,则氯化钠的溶质质量分数小于硝酸钾。
11. 下面是NH4Cl、KNO3在不同温度时的溶解度以及相应的溶解度曲线。
温度/℃ | 10 | 20 | 30 | 40 | 60 | 80 | |
溶解度/g | NH4Cl | 33.3 | 37.2 | 41.4 | 45.8 | 55.2 | 65.6 |
KNO3 | 20.9 | 31.6 | 45.8 | 63.9 | 110 | 169 |
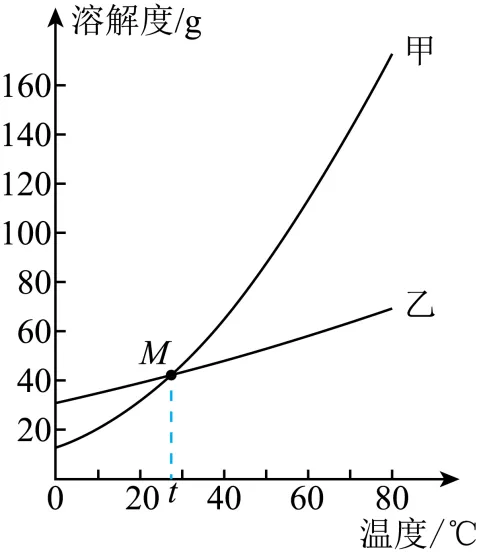
请回答:
(1)图中甲表示_____(填化学式)的溶解度曲线;
(2)M点表示的含义为_____。
(3)20℃时,将20gNH4C1加入到50g水中,充分搅拌后所得溶液为_____(填“饱和”或“不饱和”)溶液;
(4)70℃时,KNO3的溶解度_____(填“大于”“小于”或“等于”)NH4Cl的。
【答案】(1)KNO3
(2)t℃时,NH4Cl和KNO3的溶解度相等
(3)饱和
(4)大于
【解析】(1)图中甲的溶解的随温度变化大,结合表中数据可知,甲表示KNO3的溶解度曲线;故填:KNO3;
(2)由图知,M点表示的含义为t℃时,NH4Cl和KNO3的溶解度相等;故填:t℃时,NH4Cl和KNO3的溶解度相等;
(3)由表知,20℃时,氯化铵的溶解度为37.2g,即100g水最多溶解氯化铵37.2g,20℃时,50g水中最多溶解NH4C1的质量为18.6g,故20℃时,将20gNH4C1加入到50g水中,充分搅拌后所得溶液为饱和溶液;故填:饱和;
(4)由图可知,70℃时,KNO3的溶解大于NH4Cl;故填:大于。
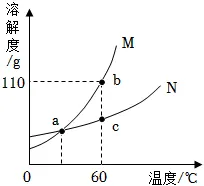
12.如表是KNO3和NH4Cl分别在不同温度时的溶解度。
温度/ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | |
溶解度/g | KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 |
NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.2 |
根据数据,绘制二者的溶解度曲线如图所示,a点为曲线的交点。回答下列问题:
(1)下列说法错误的是 (填标号)。
A.二者的溶解度均随温度升高而增大
B.曲线M为KNO3的溶解度曲线
C.a点对应的温度在30℃与40℃之间
D.a点对应的溶解度在37.2g与41.4g之间
(2)60℃时,处于c点的KNO3溶液 (填“饱和”或“不饱和”)。欲将处于c点的KNO3溶液转变为b点,可以采取 (填“蒸发溶剂”“降低温度”或“增加溶质”)的措施。
(3)60℃时,饱和KNO3溶液中混有少量的NH4Cl,应采用 (填“蒸发溶剂”或“降温结晶”)、过滤的方法提纯KNO3。
(4)若不改变溶剂的质量,将60℃时的155.2g饱和NH4Cl溶液降温至10℃,能析出NH4Cl晶体的质量为
g。
【答案】(1)C;
(2)不饱和;增加溶质;
(3)降温结晶;
(4)21.9。
【解答】解:(1)A.二者的溶解度均随温度升高而增大正确;
B.曲线M为KNO3的溶解度曲线正确,因为硝酸钾的溶解度随温度的升高变化比氯化铵大;
C.a点对应的温度在30℃与40℃之间错误,应该在20℃与30℃之间;
D.a点对应的溶解度在37.2g与41.4g之间正确;
故答案为:C;
(2)60℃时,处于c点是KNO3的不饱和溶液,因为c是硝酸钾溶解度曲线的线下点;欲将处于c点的KNO3溶液转变为b点,可以采取增加溶质;故答案为:不饱和;增加溶质;
(3)60℃时,饱和KNO3溶液中混有少量的NH4Cl,应采用降温结晶、过滤的方法提纯KNO3,因为硝酸钾的溶解度随温度的升高变化比氯化铵大;故答案为:降温结晶;
(4)若不改变溶剂的质量,将60℃时的155.2g饱和NH4Cl溶液降温至10℃,60℃时氯化铵的溶解度是55.2g,10℃时,氯化铵的溶解度是33.3g,能析出NH4Cl晶体的质量=55.2g﹣33.3g=21.9g;故答案为:21.9。
13.下表是碳酸钠和氯化钠在不同温度时的溶解度。请回答下列问题。
温度/℃ | 0 | 10 | 20 | 30 | 40 | |
溶解度/g | NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 |
Na2CO3 | 7.0 | 12.5 | 22.0 | 40.0 | 48.8 |
(1)40℃时,将16g氯化钠溶解在50g水中,得到______(填“饱和”或“不饱和”)溶液。
(2)取30℃时碳酸钠和氯化钠的饱和溶液各100g,降温至20℃,析出碳酸钠的质量______(填“大于”或“小于”)氯化钠的质量。
(3)海水晒盐是利用______的方法获得晶体。
(4)将接近饱和的碳酸钠溶液变为饱和溶液,可采用的方法是______(写出一种即可)。
【答案】(1)不饱和(2)大于(3)蒸发结晶(4)加碳酸钠固体
【解析】(1)据表格可知,40℃时氯化钠的溶解度为36.6g,其涵义是40℃时,100g水中最多溶解36.6g氯化钠,溶液达到饱和状态,即该温度下,50g水中最多能溶解氯化钠18.3g。所以40℃时,将16g氯化钠溶解在50g水中,得到不饱和溶液。故填:不饱和。
(2)降温后溶解度减小的多的析出的晶体就多,由表格可知将30℃时碳酸钠和氯化钠的饱和溶液各100g,降温至20℃,碳酸钠的溶解度减小的多,所以析出的多。即析出碳酸钠的质量大于氯化钠的质量。故填:大于。
(3)食盐的溶解度受温度变化的影响较小,从食盐溶液中获得食盐主要利用阳光和风力蒸发水分,使海水中的水分蒸发掉,使氯化钠结晶出来,利用的是蒸发溶剂的方法。即海水晒盐是利用“蒸发结晶”的方法来得到食盐晶体的。故填:蒸发结晶。
(4)据表格可知,碳酸钠的溶解度随着温度的升高而增大,将接近饱和的碳酸钠溶液转化为饱和溶液,可采用增加碳酸钠、蒸发溶剂、降低温度等方法,其中增加碳酸钠是最可靠的方法。故填:加碳酸钠固体。
【温馨提醒】因为资料篇幅长文件大,无法一起发布出来,本资料的电子档和答案在:请看(过去,资料上传到QQ,但是空间有限,敬请网友理解,所以现在资料上传到夸克网盘、百度网盘(空间大);
(1)请点击链接和提取码:下载并且安装夸克网盘或百度网盘(电脑端或者手机端均可),方便下载资料和转存留用,
(2)跟着“化学阳光驿站”随时储存并且积累宝贵资料:教学资料库+试题库):
文章末尾点击链接下载!
做有料、前瞻、有灵魂的化学公众号!
编辑整理不易,希望大家在最下方帮忙点个赞,点个在看,谢谢!
欢迎您光临:名师堂化学金牌教师精品店
(点击下方图片直接进入店面 长按下方图片二维码直接进入资料页面)

【直接点击下面链接,可以快速查看01至1547号文章】
一、879化学阳光驿站总目录(一):可以方便查看序号01至879的文章
二、1040化学微信公众号:快速查看《化学阳光驿站》文章的总目录(二):可以方便查看序号879至1041的文章
学阳光驿站》文章的总目录(三)【快速看编号01至1199
号文章】
四、1427 (速看:免费下载):快速查看化学微信公众号《化学阳
光驿站》文章的总目录(四):快速查看1200至1426号文章
五、1547 (速看:免费下载):快速查看化学微信公众号《化学阳光驿站》
文章的总目录(五)快速查看1427至1547号文章
补加:
1547 (速看:免费下载):快速查看化学微信公众号《化学阳光驿站》文章的总
1548 2025年秋季九年级化学各种版本月考试卷收心卷(免费下载)
1549 2025年秋季九年级第一次月考考卷含答案(第一~二单元)(免费下载)(共4份)
1550 2025年秋季九年级第一次月考考卷含答案(第一~二单元)(免费下载)(共4份)
15512025年秋季九年级第一次月考考卷含答案(第一~二单元)(免费下载)(共3份+初中各学科答题卡模板)
15532025年秋季九年级化学第一阶段创新作业4套 (含答案)
15562025年秋季九年级(1-3单元)第一阶段化学试卷01(含答案)
15572025年秋季九年级(1-3单元)第一阶段化学试卷02(含答案)
1558九年级化学上册《第三单元物质的奥秘》知识考点清单与讲解
15592025年秋季九年级(1-3单元)第一阶段化学试卷03(含答案)
15602025年秋季九年级(1-3单元)第一阶段化学试卷04(含答案)
1561 2025年秋季九年级化学沪教版第三章《物质构成的奥秘》知识点汇总+习题训练(免费下载)
1562 九年级化学第三单元《物质构成的奥秘》易错知识点强化
15642025年秋季假期作业九年级化学第三单元《元素》 (免费下载上册下册全册作业设计)
1565 九年级化学教学质量阶段检测表彰总结分析暨迎接期中动员鼓励励志会
1566 九年级化学《物质组成的表示》 教学设计(免费下载)
1567 九年级化学第四单元《自然界的水》随身携带记忆知识卡片
1568 九年级化学学霸笔记《 第三单元 物质构成的奥秘》(免费下载)
1569 九年级化学学霸笔记《 第四单元 自然界的水》(免费下载)
1571 2025年秋季迎接九年级化学期中:《化合价与化学式》的背记归纳与假期作业
1572 最新最美姓氏头像——陈(62张任你选)(免费下载)
1574 九年级化学2025年秋季期中模拟试题1(放心下载)
15752025年秋季九年级化学期中专项复习化学式的计算题(选择题+计算题)(免费下载)
1580黄冈市九年级化学2024年秋季期中真题与答案(免费下载)
1581 湖北省2024年至2025年上册期中期末好试题汇聚(含答案)
1582 湖北省九年级化学下册2024年至2025年中考调考模考好题好卷(含答案)
1583值得一看:全国第十届初中化学实验说课比赛视频汇总(免费下载)
1586 九年级化学《化学反应的定量关系》复习课件+上册课时同步讲练(免费下载)
1587 九年级化学第五单元《化学反应的定量关系》复习巩固(免费下载)
1588 初中语文数学英语物理化学道法历史中考同步教学复习资料(免费下载)
1589九年级化学第五单元《化学反应的定量关系》重难点突破教学设计(免费下载)
1590 (化学兴趣活动)九年级化学重要基础:化学用语知识竞赛试题.
1591高中语文数学英语物理化学道法历史高考同步教学复习资料(免费下载)
15922025年秋季九年级化学第一~五单元月考卷(含详细答案)
1593九年级同学中考必看视频:为什么要好好读书(百万人关注者)
1594九年级化学《 二氧化碳的实验室制取》(视频+讲义+分层作业+校本作业+攻关复习)(免费下载)
15962025年秋季九年级化学新中考第一至七单元期末考卷(有详细答案)
1597 九年级化学第七单元课题一《燃料的燃烧》第1课时(新课标·课件)(免费下载)
15982025年秋季九年级化学12月月考试题(含详细答案)
16002025年秋季九年级语文期末复习专题知识清单+考题猜想+模拟试卷(免费下载)
1601九年级化学《探究燃烧的条件》全国讲课比赛视频+教学设计+分层作业(免费下载)
1602最新2026版本九年级化学下册8-11单元【课件+单元检测+分层作业】
1603九年级化学2025年秋季期末考第一~七单元考卷(免费下载)
16042025年秋季九年级化学期末模考考卷(第一~七单元含详细答案)
1605孩子的荣耀时刻,请家长留存:化学优秀学子分享学习经验演讲
16062025年秋季九年级化学期末试卷(考查1至7单元内容)
1607九年级化学下册课件:金属活动性顺序课件(8至11单元最新全套课件含跨学科实践活动课件)
1608九年级化学上册全套精品课件(含视频):降低化石能源的利用对环境的影响课件(免费下载)
1610九年级化学第八单元《 金属和金属材料》的5节全国讲课比赛视频
1611九年级化学下册第八单元《 金属和金属材料》同步教学资源(免费下载)
1612湖北省黄冈市部分学校2025年秋季12月联考化学数学等7科试卷2套(含答案)(免费下载)
16132025年全国初中化学讲课比赛视频 《金属的化学性质》
16152025年全国初中化学讲课比赛视频: 下册部分汇聚1(八至十一单元)
1616湖北省2024年秋季期末2024年中考2025年中考试题9科全套含答案
1617化学教研:2025年全国初中化学优质课视频: 下册部分汇聚2(八至十一单元)(免费下载)
1618化学教研:2025年全国初中化学优质课视频: 下册部分汇聚3(八至十一单元)(免费下载)
1619九年级化学2025年秋季期末考卷(第一~八单元)含详细答案
1620九年级化学下册鲁教版《第八单元 海洋化学资源的利用《(课件+作业+知识笔记)(免费下载)
16222025年全国初中化学优质课视频: 下册部分汇聚4(八至十一单元)(免费下载)
1624九年级化学下册课本(2025年春季人教版本)及化学知识点提纲(按课题编写)
1626 语文九年级下册2025春部编版教学资源包(课件+教案+说课+练习+写 作)
1627九年级化学下册人教版最新 课件PPT(学案+作业+重难点+单元复习)
1628湖北省重点学校九年级化学2025年12月联考(含答案免费下载)
1633九年级化学2025年12月阶段测试化学试题含详细答案(1-8单元)
1635九年级化学人教版下册实用教学资源包(课件导学案作业教学设计)
1637 九年级化学第1–8单元期末常考化学方程式+实验现象+易错考点
1638九年级化学上册下册知识点+化学用语每日默写天天练+知识清单(免费下载)
16392025年秋季九年级化学上学期期末教学检测试题(1至8单元)
16402025年秋季九年级化学上学期期末教学检测试题含答案(1至7单元)
16422025年秋季九年级化学期末模拟考试1-9单元(人教版)
1643 新版高中化学教师用书(必修1+必修2+选择性必修123)(免费下载)
1644 高中化学高考一轮复习+二轮复习+选择性必修123(免费下载)
1645人教版化学九年级下册《第八单元 金属和金属材料》:课本+教师教学用书+课后习题+PPT等备课完整资料
1646人教版化学九年级下册第9单元《溶液》教师教学用书+课后习题+PPT等备课资料
1647人教版化学九年级下册《第10单元酸碱盐》课本课后习题+教师教学用书+PPT等备课完整资料
1651更正1604号文章下载地址 2025年秋季九年级化学期末模考考卷(第一~七单元含详细答案)
1652 湖北省九年级化学2025年秋季期末模拟卷1(黄冈市)含答案
1653 广东省2025年秋季九年级期末考试化学试卷1含答案
16552025年秋季湖北省襄阳市九年级化学期末模考考卷含答案
16562025年秋季湖北省武汉市九年级化学期末考卷1含答案
16572025年秋季湖北省武汉市九年级化学期末模考考卷2含答案
16592025年秋季湖北省孝感市九年级化学期末模考考卷含答案
16602025年秋季湖北省九年级化学期末考卷含详细答案(第1~7单元)
16612025年秋季湖北省九年级化学期末考卷含详细答案(第1~7单元)
16622025年秋季湖北省荆州市九年级化学期末模考卷含答案
16632025年秋季湖北省襄阳市九年级化学期末模考卷含答案
16642025年秋季湖北省武汉市九年级化学期末模考卷含答案
1671 九年级化学上学期期末工艺流程图真题专题备考(含详细答案)
1672湖北省黄冈市2024年秋季九年级期末物理化学考卷含答案(免费下载)
1674 九年级化学上学期期末易错点《 实验方案评价》复习备考含答案
16762026年春季教学周历表(含工作安排记录表)(免费下载)
16772026版《物理中考试题研究》含课件+分层作业(word)(免费下载)
1679 2026版高中9科全科同步《解题技巧》教材同步版(高一高二专用)
1680 高中英语同步教学和高考英语复习大全资料(免费下载)
1681 高考英语复习:2026年高考英语终极对决锦囊·三年真题解读(免费下载)
1682 高考物理复习:【强基计划】“双一流”高校自主招生物理好题精选(word版)(免费下载)
16832026年高一数学寒假作业+巩固培优讲义(word版)(免费下载)
16842026年高二数学寒假作业+巩固培优讲义(word版)(免费下载)
1685 高中数学五本书全套系列2(必修第一册+必修第二册+选择性必修第一册+选择性必修第二册+选择性必修第三册)(免费下载)
1686 高考数学复习:备战2026年高考数学专题检测含答案 word版(免费下载)
1687 2026高考备考全科:9科全套试题(含答案) (免费下载)
1688 高考英语复习:2026版高中英语学习资料包 (知识点+教辅+试卷)(免费下载)
1689 高中英语:高一至高三全套(课件+教案+讲义+习题+音频)(免费下载)
1690 2026年春季九年级化学人教版下册实用教学资源包(课件导学案作业教学设计+复习)
1691 中考最新复习:2026版《中考9科第一轮复习专项优选题》(含答案)
1697 初中文综中考:道法历史地理同步教学和中考复习资料(好好珍惜)
1700 高中物理历史政治地理生物同步教学和高考复习资料(好好珍惜)
1701 高考化学二轮复习+课时作业高中全套(Word版+课件)
1702 高考数学复习:二轮复习(Word版+课件)+史上最全高考数学原卷.
1703 高考复习:语文 英语 物理 二轮复习(Word版+课件)
1704 高考复习:2026版高中【课时作业】9科全科 语文 数学 英语 物理 化学 政治 历史 地理 生物(Word版)
1705 人教版初中九年级化学上下册47讲专题单元复习(Word版)和七年级八年级下册中考各科复习
1706 【中考化学】二轮专项复习·核心考点讲解与必刷题型(Word版)
【最新资料】:
2026年重点高中自主招生(理科实验班)提前预录考试化学模拟试题: https://www.zxxk.com/docpack/3616454.html
九年级上册化学各阶段考卷-2025-2026学年九年级化学人教版:https://www.zxxk.com/docpack/3548365.html
【好题汇编】备战2025-2026学年九年级化学上学期期末真题分类汇编(湖北专用):https://www.zxxk.com/docpack/3590434.html
2025年中考化学重点题型专题备考讲义(附学案十解题模板):https://www.zxxk.com/docpack/3479057.html
化学中考压轴微题满分必刷(全国通用):https://www.zxxk.com/docpack/3208548.html
重点高中2024年自主招生(理科实验班)提前预录考试化学模拟试题:https://www.zxxk.com/docpack/3187686.html
发福利了1 【2026年中高考资料】
【资料一直在更新,留心以往文章下载过去资料】
1588 初中语文数学英语物理化学道法历史中考同步教学复习资料(免费下载)
1591高中语文数学英语物理化学道法历史高考同步教学复习资料(免费下载)
夸克网盘分享了「16762026年春季教学周历表(含工作安排记录表).xlsx」,点击链接即可保存。链接:https://pan.quark.cn/s/d982a3c30a58
声明:本公众账号分享的电子书版权属于原出版机构或影像公司或者原作者,传播分享仅限于学生家长或老师下载预览,资料仅供交流心得、参考;好的内容值得分享,如有侵权请联系删除。本页面广告内容、产品、服务均由公众号系统智能发布、本公众号不承担任何责任。
化学阳光驿站:交流化学教研,分享化学经验,提供化学资料,在化学
驿站上一起愉快轻松共同成长。
“设为星标”是为了您随时能找到我;
“点赞/在看”是为了您能第一时间收到推送;感谢您的支持和鼓励!
【温馨提醒】本资料的电子档和答案在:请看(请点击链接下载,只要一次性安装夸克网盘或百度网盘,就能方便下载所有资料和转存留用(放心使用),跟着“hxygyzh2021” “化学阳光驿站”随时储存并且积累宝贵资料:教学资料库+试题库):
夸克网盘给你分享了「化学中考一轮复习:单元+微专题(Word版).rar」,点击链接或复制整段内容,打开「夸克APP」即可获取。
/~fdb63LodO0~:/
链接:https://pan.quark.cn/s/b63d9d146f5a