关注我们,了解更多连云港教育资讯
1.(24-25九上·江苏扬州江都区·期中)小组同学想探究用不同物质在空气中燃烧测定氧气含量方法的优劣。他们用足量的蜡烛、红磷和白磷分别在相同体积与状态的空气中燃烧(红磷与白磷燃烧产物均为五氧化二磷),用氧气探测器测定容器中剩余氧气与时间的关系如图。下列说法错误的是
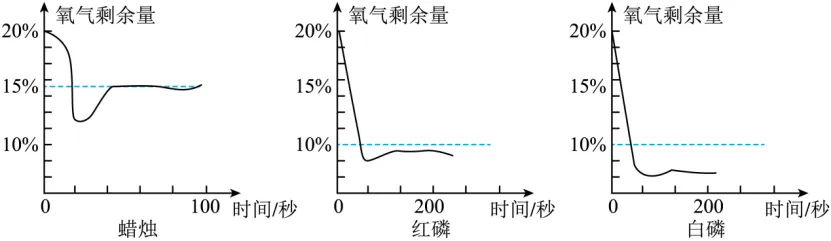
A.该实验证明氧气浓度小于一定值时,蜡烛无法燃烧
B.三个实验中测定空气中氧气的含量效果最好的是白磷燃烧实验
C.根据图像对比可知,三种物质中,白磷能在更低浓度的氧气中燃烧
D.若将足量蜡烛和白磷放在同一密闭容器中燃烧,氧气的体积分数可降至0%
【答案】D
【详解】A、由图可知,蜡烛熄灭后仍含有氧气,则说明氧气浓度小于一定值时,蜡烛无法燃烧,该选项说法正确;
B、三个实验中,熄灭后,白磷实验中剩余氧气最少,则含量效果更好,该选项说法正确;
C、由于白磷实验中剩余氧气最少,则说明三种物质中,白磷能在更低浓度的氧气中燃烧,该选项说法正确;
D、由图可知,白磷与蜡烛燃烧均不能将氧气消耗完,故若将足量蜡烛和白磷放在同一密闭容器中燃烧,氧气的体积分数不可降至0%,该选项说法不正确;
故选D。
2.(24-25九上·江苏南京鼓楼区·期中)为探究铜的化学性质,某同学借助氧气传感器在密闭装置中进行如图所示实验,观察实验现象并分析氧气含量随时间变化的曲线图。下列说法不正确的是
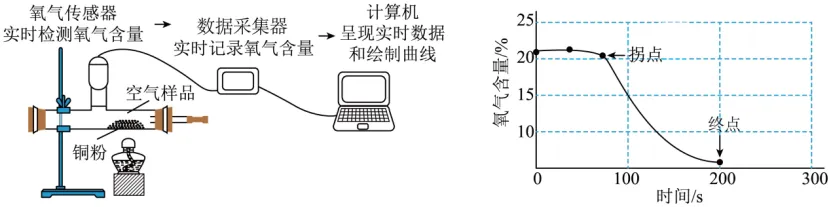
A.铜在加热条件下能与氧气反应
B.实验过程中,固体由红色逐渐变黑
C.拐点至终点所对应的时间范围内,装置内物质的总质量逐渐减少
D.实验过程中,装置内固体中铜元素的质量分数减小
【答案】C
【详解】A、加热过程中氧气含量减少,说明铜在加热条件下能与氧气发生化学反应,故选项说法正确;
B、铜在加热条件下与氧气反应生成氧化铜,实验过程中,固体由红色逐渐变黑,故选项说法正确;
C、在密闭装置中进行实验,化学反应遵循质量守恒定律。拐点 C 至终点 D 所对应的时间范围内,铜与氧气发生反应生成氧化铜,但装置内物质的总质量不变,故选项说法错误;
D 、由质量守恒定律可知,实验过程中,装置内固体中铜元素的质量不变,但铜与氧气反应生成氧化铜,固体质量增加,则固体中铜元素的质量分数减小,故选项说法正确;
故选:C。
3.(24-25九上·江苏镇江外国语学校·期中)如图把氧气、二氧化碳、水蒸气(测湿度)探头放入食品保鲜袋中,开始采集数据,然后向袋内吹入气体,采集的数据经处理如图,下列说法错误的是
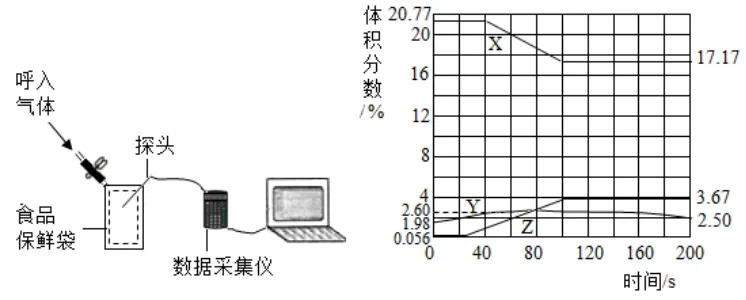
A.曲线X表示二氧化碳,曲线Y表示的是氧气
B.通过实验探究,呼出气体中氧气的含量比吸入空气中的氧气含量降低
C.200s时没有被测定的气体所占的总体积分数为76.66%
D.Y的体积分数在60s之后逐渐减小的原因是水蒸气冷凝
【答案】A
【详解】A、呼吸作用是消耗氧气,呼出二氧化碳和水蒸气,因此氧气的含量减小,二氧化碳的含量增多,所以曲线X表示氧气,曲线Y表示的是二氧化碳,选项错误;
B、如图所示,曲线X表示氧气曲线逐渐下降,说明呼出气体中氧气的含量比吸入空气中的氧气含量降低,选项正确;
C、由图示可知:200s时未采集数据的所有气体,总体积分数为1−17.17%−3.67%−2.50%=76.66%,选项正确;
D、水蒸气遇冷会液化成水,气体减少体积变小,Y的体积分数在60s之后逐渐减小的原因是水蒸气冷凝,选项正确;
故选:A。
4.图1所示装置可用于测定空气中氧气的含量,其中与集气瓶相连的压强传感器等电子设备能将集气瓶内气体压强精确地记录并保存下来.图2、图3是用该装置测得的红磷和木炭分别在集气瓶中燃烧的压强﹣时间关系图(该装置气密性良好,p0是集气瓶内初始气压,p和p′分别是反应结束后恢复到室温时集气瓶内的气压).下列说法正确的是
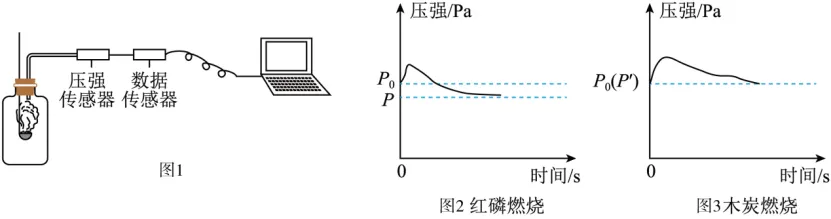
A.燃烧匙内所装红磷或木炭的多少对实验结果无影响
B.反应开始时集气瓶中压强瞬间变大的是由燃烧放热造成的
C.p=0.79p0,p′=p0是因为红磷的着火点比木炭低
D.由图3可推出空气中氧气的含量
【答案】B
【详解】试题分析:A.若所用药品过少,就不会将装置内的氧气耗尽,会导致实验结果出现误差,错误;B.反应开始时,物质燃烧放出大量的热,气体体积受热膨胀,所以集气瓶中压强瞬间变大的是由燃烧放热造成的,正确;C.压强不同的原因主要是木碳燃烧生成了二氧化碳气体,与可燃物的着火点无关,错误;D.由于碳与氧气反应生成二氧化碳,虽然都消耗了氧气,但又生成了气体,装置内气体压强保持不变,无法测定,错误。
考点:考查空气组成的测定的知识。
5.(24-25九上·江苏苏州吴中、吴江、相城、高新·期中)某学习小组开展“测定空气中氧气的体积分数”的探究活动。
Ⅰ.史料研究
18世纪70年代,化学家拉瓦锡设计了如图-1所示装置,将少量的汞放在曲颈甑内,连续加热12天后,汞表面有红色粉末(氧化汞HgO)产生,同时曲颈甑内的空气体积约减少五分之一。拉瓦锡再将所得红色粉末收集放入另一较小容器里,强热,得到汞和一种气体,该气体能使带火星木条复燃,充分反应后,所得气体体积恰好等于原来密闭容器里所减少的那部分空气体积,进而计算得出空气中氧气的体积分数。
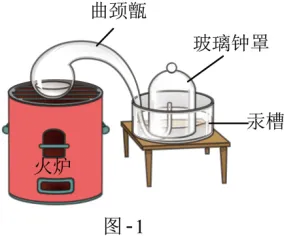
(1)连续加热12天的主要目的是。
(2)曲颈甑内汞表面产生红色粉末时,钟罩内液面上升,产生该现象的原因是。
(3)红色粉末加强热分解反应的化学方程式为。
Ⅱ.实验测定
学习小组设计图-2装置利用红磷燃烧粗略测定空气中氧气的体积分数。实验过程中发现,水面均未上升到刻度“1”。
已知:
①红磷的着火点是240℃,白磷的着火点是40℃。
②相同温度下,气体的压强比和体积比相同。
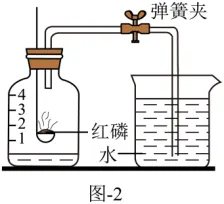
经讨论后,分别取足量红磷、白磷采用如图-3装置进行实验,测得红磷实验中的氧气含量、白磷实验中压强随时间变化的结果分别如图-4(红磷实验)、图-5(白磷实验)所示
(4)红磷(P)与氧气反应的化学方程式为。
(5)图-4中,氧气含量从8.05%。上升到9.26%,上升的原因可能是。
(6)图-5中,BC段压强增大,原因是。据该图中数据计算白磷消耗的氧气占空气体积的%(精确到0.1%)。
【答案】(1)使氧气充分反应
(2)汞与氧气反应,钟罩内气体减少,压强减小
(3)
(4)
(5)反应结束后,温度下降,气体逐渐混合均匀(或温度下降后,水蒸气变成液态)
(6) 白磷燃烧放热,瓶内温度升高,压强增大;白磷燃烧消耗氧气,瓶内气体减少,压强减小,前者程度大于后者,压强增大 19.4
【详解】(1)连续加热12天的主要目的是使氧气充分反应,使实验结果更准确,故填:使氧气充分反应;
(2)汞与氧气反应生成氧化汞,导致钟罩内气体减少,气压减小,玻璃钟罩内汞液面上升,故填:汞与氧气反应,钟罩内气体减少,压强减小;
(3)氧化汞在加热的条件下生成汞和氧气,反应的化学方程式为,故填:;
(4)红磷燃烧生成五氧化二磷,反应的化学方程式为,故填:;
(5)红磷燃烧消耗氧气并放出热量,而其他气体不变,氧气的含量逐渐减小,但反应结束后,温度下降,气体逐渐混合均匀或温度下降水蒸气变成液态,导致氧气的含量逐渐增大,故填:反应结束后,温度下降,气体逐渐混合均匀(或者温度下降后,水蒸气变成液态);
(6)白磷燃烧放热,瓶内温度升高,压强增大;白磷燃烧消耗氧气,瓶内气体减少,压强减小,前者程度大于后者,所以BC段压强增大;用如图所示数据计算,用这种方法测得的空气中氧气的体积分数是:,故填:19.4%。
推荐阅读:详解初中英语语法
需要完整电子版的家长,转发本文章到朋友圈一天以后,然后截图直接私信下方青山老师
为防止走失,请关注以下公众号,并加上星标,我们持续输出更多学习资料,敬请保持关注!






