Electrosynthesis
化学万事屋live
今天分享2025年福建卷和2025年浙江6月卷中对电化学的考查,它们的共同点是体系中不止包含两个电极反应,还有后续的协同反应。一旦有了后续反应,从科研的角度来说,可拓展性就高了,与此同时,命题的空间也会开阔起来,题目也会变得更加综合。因此,这篇文章的目的是结合这两个实例,来把对“后续反应”的关注度提上来(与其说它是解题技巧,不如说是思考上的全面性)。
11 浙江6月卷 | 电极反应→后续氧化
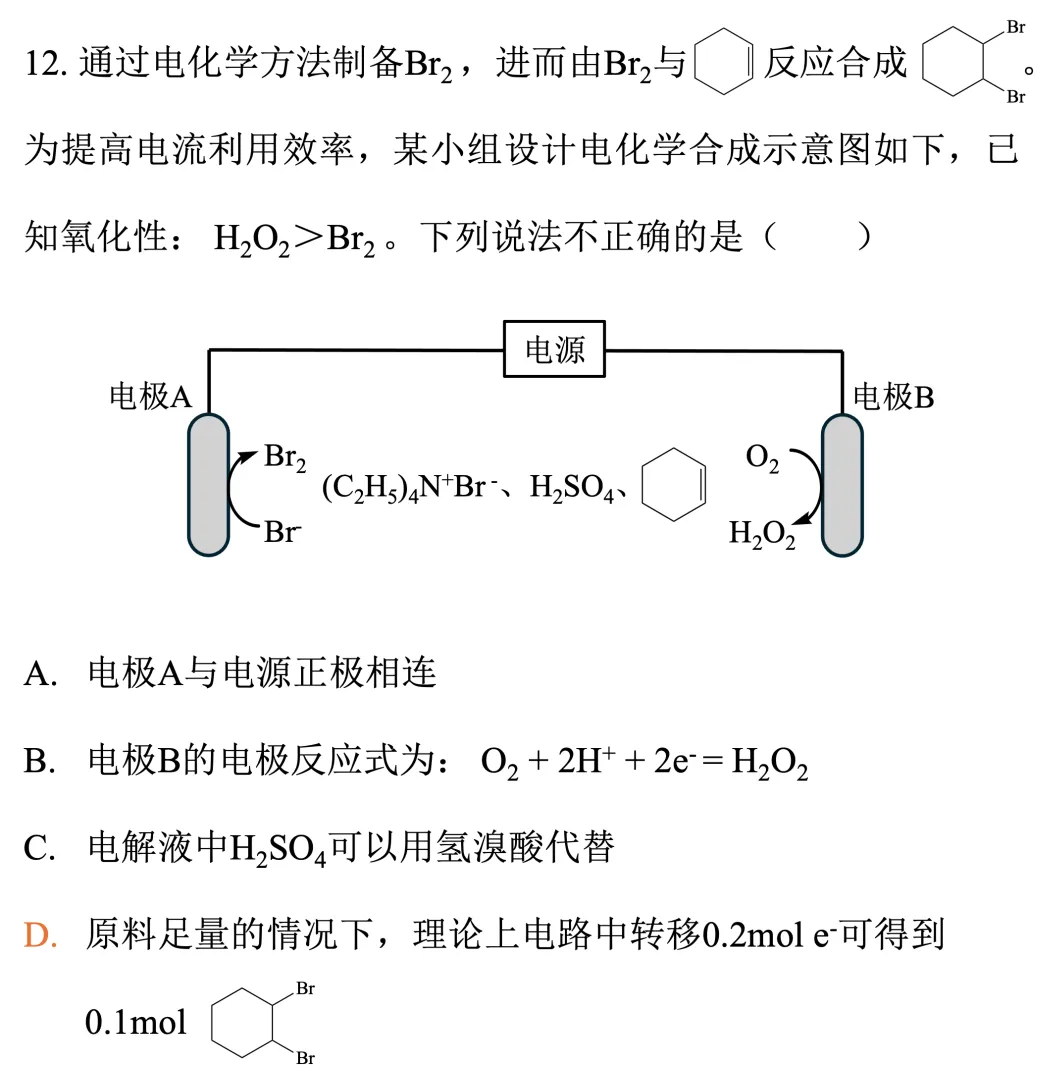
电极A:Br-→Br2,发生氧化反应,作阳极,接电源正极。电极B:O2→H2O2,O从0价降至-1价,发生还原反应,作阴极,接电源负极。注:O2→H2O2属于「氧还原反应」中的2电子途径,与之相对的是O2→H2O的4电子途径(见广东卷)。
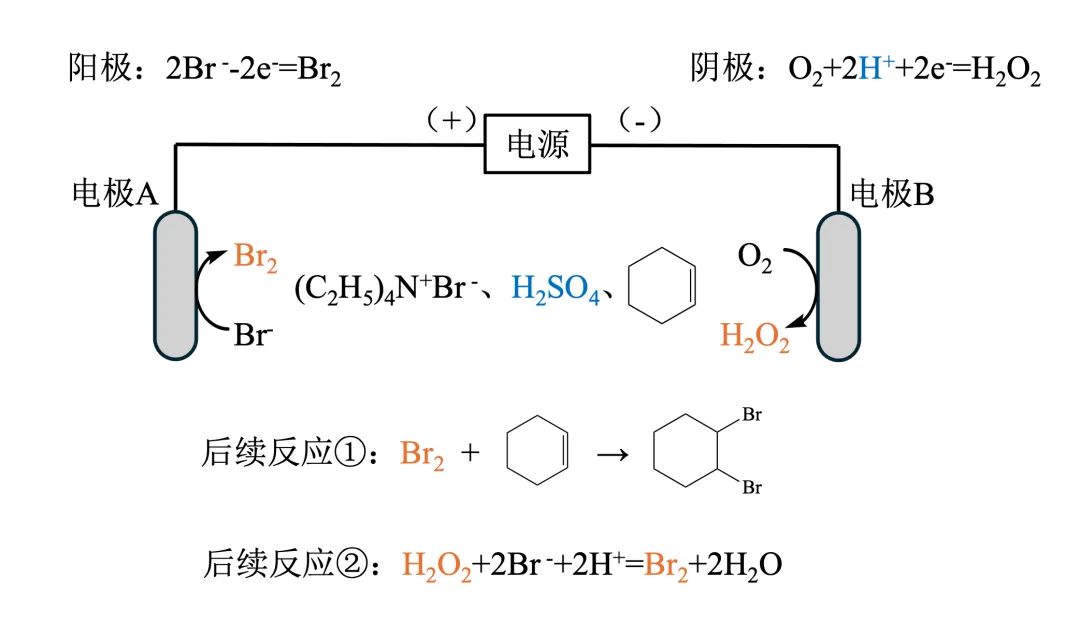
D选项:需要注意该电合成体系中不只包含两个电极反应,还有两个后续反应:① Br2和环己烯的加成;② 根据“氧化性:H2O2>Br2”,阴极生成的H2O2能氧化Br-发生后续反应②。
基于以上,当电路中转移0.2mol电子时,根据电极反应,可以生成0.1mol Br2和0.1mol H2O2;根据反应②,0.1mol H2O2可以氧化Br-生成0.1mol Br2;因此,总的来说可以生成0.2mol Br2。最后根据反应①,0.2mol Br2对应0.2mol 加成产物。
12 福建卷 | 无膜电合成碳酸乙烯酯
这是一个无膜电解池装置,无膜,刚好省成本了,同时OH-也自由了。
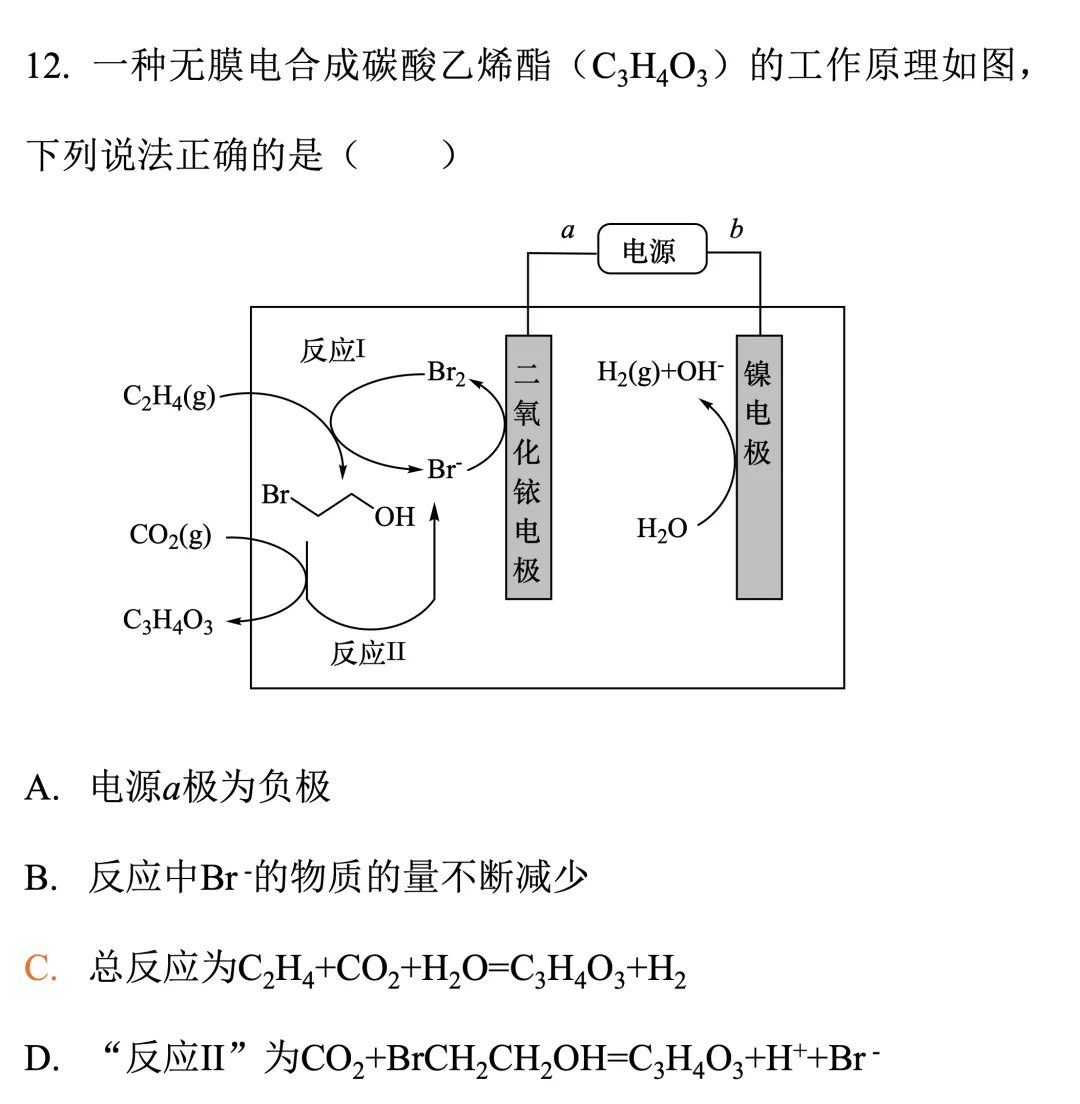
二氧化铱电极:Br-→Br2,发生氧化反应,作阳极,接电源正极a。镍电极:H2O→H2+OH-,发生还原反应,作阴极,接电源负极b。电极反应,以及反应I和II如下:
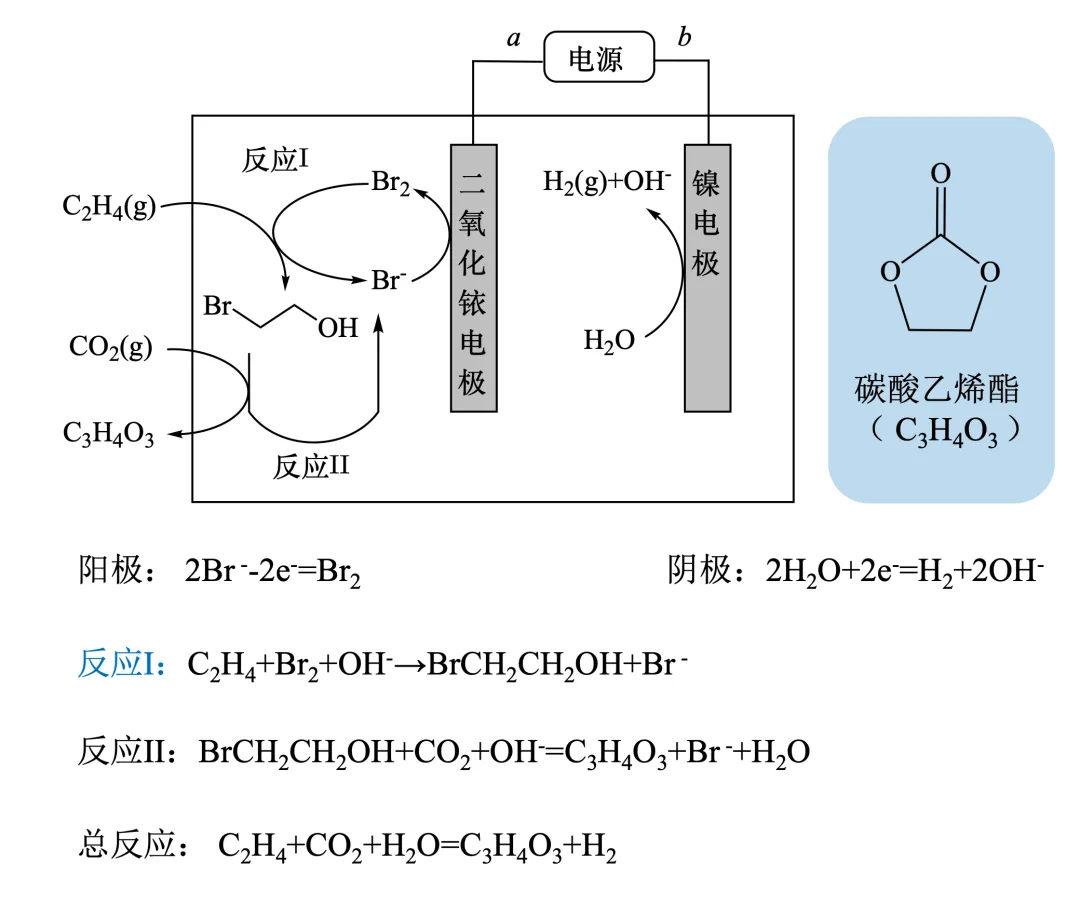
Br-的物质的量变化:二氧化铱电极上消耗Br-,反应I和II生成Br-。根据计量关系:2Br-~Br2~(I)Br-+(II)Br-,Br-的物质的量不变,主打一个介导作用,即bromide-mediated。D选项,图中明确阴极产物有OH-,可理解为体系环境为弱碱性,D中产物里出现H+不合适。
文献溯源:这道题的命题来源为浙江大学莫一鸣研究团队的科研成果,文章标题如下:

针对反应I,它其实不止一步反应,具体如下:
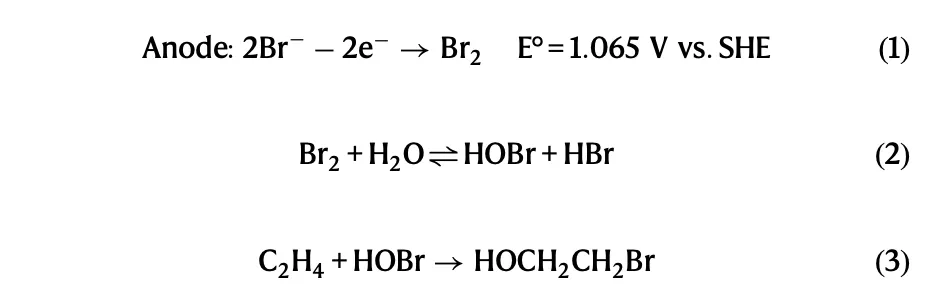
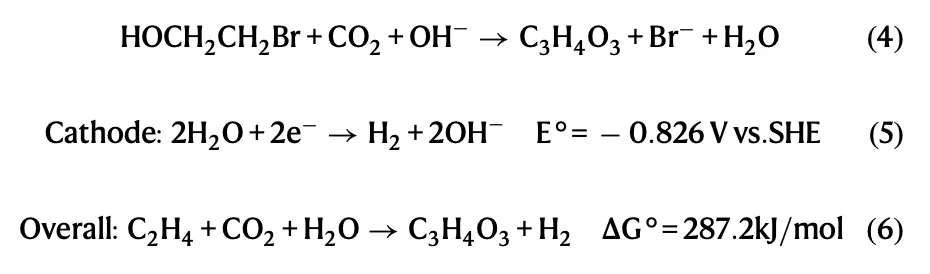
注:考虑到碱性环境,我在写反应I时直接以OH-为反应物了,与文献有所差别。
针对反应II,即从BrCH2CH2OH→C3H4O3,该研究提出了两条反应路径:HCO3-和CO2,CO2可以和阴极生成的OH-反应转化为HCO3-。
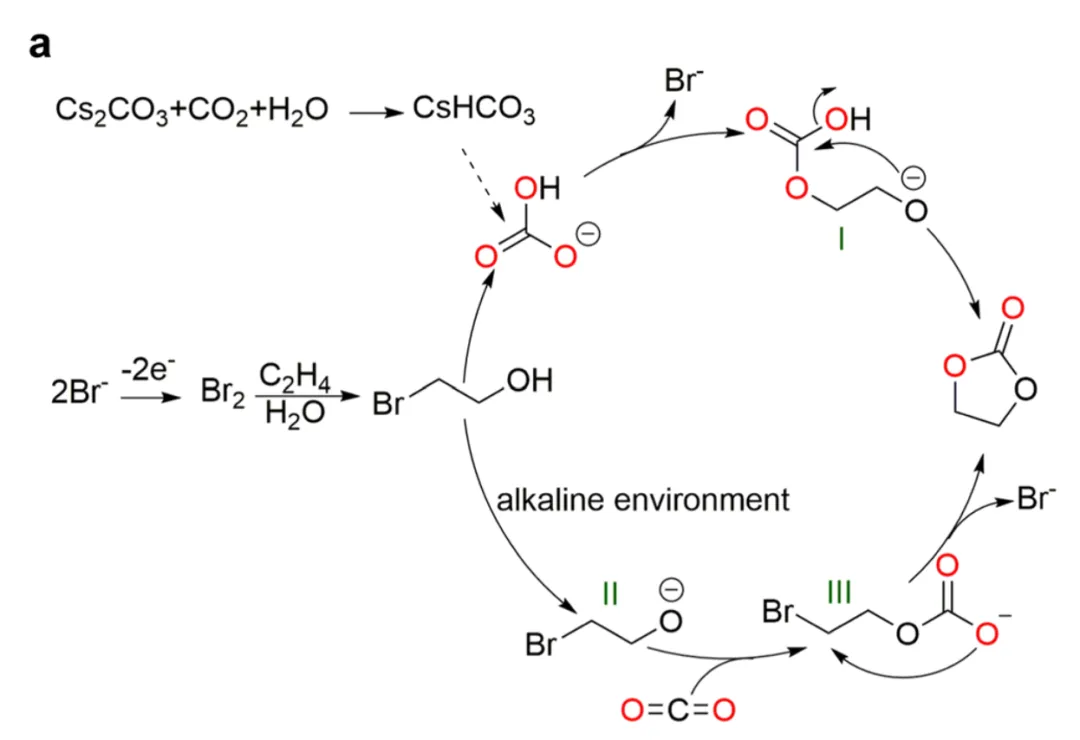
特别说明:最后三张截图以及文章标题右图皆来自以上参考文献,如有其它疑问,可参考原文献(开源的)。
🐳敬上~~~






