阅读链接:2026年4月初中学业水平测试化学试题及答案;
一、单项选择题(本大题共20小题,每小题2分,共40分。在每小题列出的四个备选项中,只有一项符合题目要求,错选、多选或未选均不得分。)
1.“绿水青山就是金山银山”。下列做法不符合该主题的是
A.使用一次性餐具B.垃圾分类回收
C.使用太阳能热水器D.乘坐公交出行
2.规范的操作是实验成功的保证。下列实验操作正确的是
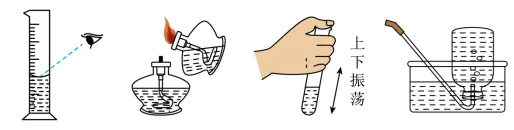
A.读取液体体积B.点燃酒精灯C.振荡试管D.收集氢气
3.“壮族三月三”是国家级非物质文化遗产,是广西人民的盛大节日,下列节庆活动中,属于化学变化的是
A.抛绣球B.织布丝 C.扁担舞D.酿米酒
4.广西空气因负氧离子含量高、生态环境优越,被誉为“天然氧吧”和“长寿之乡”,下列物质不属于空气污染物的是
A.二氧化碳B.二氧化硫 C.PM2.5D.臭氧
5.下列可用于配制无土栽培营养液的物质中,属于氮肥的是
A.KNO3B.NH4NO3
C.MgSO4D.Ca(H2PO4)2
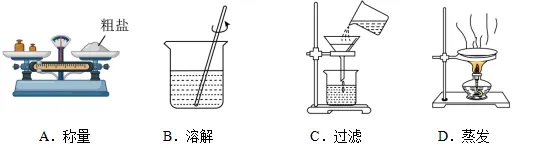
6.实验1《粗盐中难溶性杂质的去除》。通过观察可以发现,四幅画面中操作规范的是
7.下列物质属于金属材料的是
A.陶瓷B.塑料 C.玻璃D.铝合金
8.随着科技的发展,空气中各成分的应用越来越广泛。下列用途主要利用物理性质的是
A.氮气——充氮防腐 B.二氧化碳——气体肥料
C.氧气——医疗急救 D.稀有气体——激光技术
9.了解化学安全知识,增强安全防范意识。下列做法不符合安全要求的是
A.携带酒精喷雾乘坐高铁
B.油锅着火时用锅盖盖灭
C.点燃可燃性气体前,先检验气体纯度
D.家中燃气胶管泄漏着火,立即关闭燃气阀门
10.我国首台万瓦级氮制冷机首次公之于众,该装备能够在极端低温环境下稳定运行,为液氮的生产及储存提供了技术支持。液氮可由氮气冷却液化而成,该过程中氮分子
A.种类改变B.数目改变 C.大小改变D.间隔改变
11.把下列少量厨房调味品分别放入水中,充分搅拌,不能得到溶液的是
A.食盐B.香油 C.蔗糖D.白醋
12.《本草纲目》载药1 892种,其中记载有升丹(其成分含HgO)。HgO中Hg的化合价是
A.-1 B.0 C.+1 D.+2
13.下列各组中的两种物质,在溶液中不能发生复分解反应的是
A.H2SO4与BaCl2B.KNO3与NaCl
C.Na2CO3与HCl D.NaOH与CuSO4
14.我国“鹊桥二号”中继卫星使用镀金钼丝天线,搭建了地面与“嫦娥六号”的通信桥梁。下图是钼元素在元素周期表中的相关信息,下列说法正确的是
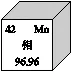
A.钼原子的中子数为42
B.钼属于金属元素,反应中易得电子
C.钼的相对原子质量为95.96 g
D.一个Mo2+中含有的电子数为40
15.科学家使用普通氧分子和带电的氧离子得到了新型氧分子(O4)。下列叙述正确的是
A.O4是不带电的分子
B.1个O4分子含有2个O2分子
C.O4与O2的性质完全相同
D.O4和O2混合形成的是纯净物
16.有X、Y、Z三种金属,X和稀盐酸不反应,Y和稀盐酸反应有气泡产生,X放入AgNO3,溶液中表面有银白色固体出现,Z与AgNO3溶液无明显现象,则X、Y、Z三种金属的活动性由弱到强的顺序是
A.X<Z<Y B.Z<Y<X
C.Z<X<Y D.Y<X<Z
17.分类是认识和研究问题的重要方法之一,下列物质分类不正确的是
A.混合物:河水、空气
B.氧化物:高锰酸钾、二氧化碳
C.单质:氢气、铁
D.化合物:水、氧化镁
18.下列实验方案中不能达到实验目的的是
选项 | 实验目的 | 实验方案 |
A | 鉴别碳酸钠固体和硫酸钠固体 | 分别取样,滴加稀盐酸,观察现象 |
B | 分离NaCl和BaSO4的固体混合物 | 加水溶解,过滤、蒸发结晶,清洗滤渣并晾干 |
C | 除去盐酸中含有的少量硫酸 | 加入适量的BaCl2溶液后过滤 |
D | 除去Cu(NO3)2溶液中混有的AgNO3 | 加入足量的铝粉,过滤 |
19.t1℃时,将相同质量的KNO3和KCl分别加入盛有100 g水的甲、乙烧杯中,充分搅拌后现象如图Ⅰ所示,图Ⅱ为两物质的溶解度曲线。以下说法正确的是
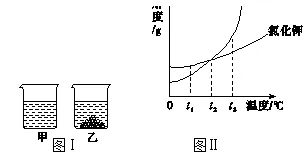
A.甲烧杯中的溶质为KNO3
B.将温度升高到t2℃时,乙烧杯中仍然有固体剩余
C.若KNO3中混有少量KCl,可采用蒸发结晶的方法提纯KNO3
D.若取t3℃时KNO3和KCl的饱和溶液各100 g,降温至t2℃,析出晶体较多的是KNO3
20.热水瓶用久后瓶胆内壁常附着一层水垢,其成分是碳酸钙、氢氧化镁。实验室现有一瓶水垢样品,为测定其中各成分的质量分数,某化学兴趣小组的同学利用如图所示装置进行实验(该装置气密性良好,A、C、D中所装试剂足量)。已知:碱石灰是氧化钙和氢氧化钠的固体混合物,在高温的条件下,氢氧化镁也发生分解,生成氧化镁和水蒸气。
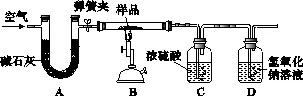
部分实验步骤如下:①将质量为m的水垢样品装入装置B的玻璃管中,按图连接好装置,关闭弹簧夹,给样品加热;②待样品完全反应,先打开弹簧夹通入空气,再熄灭酒精喷灯,直到玻璃管冷却;③实验完毕,测得装置C、D中的液体质量分别增大了m1、m2,计算水垢中各成分的质量分数。则下列说法正确的是
A.B装置中发生反应的基本类型是分解反应
B.m2是样品完全反应后产生的二氧化碳的质量
C.若没有装置A,会导致氢氧化镁的测定结果偏小
D.若装置C和装置D位置颠倒,不会影响碳酸钙的测定结果
二、填空与简答题(本大题共6小题,每个化学方程式2分,其余每空1分,共38分。)
21.(6分)化学用语是简明扼要、信息丰富、国际通用的语言。请用化学用语填空。
(1)氖气;(2)人体中含量最多的金属元素;
(3)铵根离子;(4)氧化铁;
(5)硫酸铜;(6)标出氧化铝中铝元素的化合价。
22.(6分)请用下列物质对应的序号填空。
①石墨 ②氢氧化钠 ③酒精 ④熟石灰 ⑤石灰石 ⑥小苏打
(1)用作建筑材料的是;(2)可用作燃料的是;
(3)广泛应用于肥皂、石油、造纸等工业的是;
(4)可用于制作铅笔芯的是;
(5)可用于制作面包发酵剂的是;
(6)可用于改良酸性土壤的是。
23.(6分)在航空航天领域,对CO2的处理尤为重要。
(1)早期的飞船是利用超氧化钾(KO2)吸收CO2,反应的化学方程式为4KO2+2CO2===2K2CO3+3R,则R的化学式为。
(2)后来科学家采用LiOH吸收CO2,该反应的化学方程式为。
(3)现代空间站采用分子筛技术吸附CO2后再排入太空,该吸附过程属于(填“物理变化”或“化学变化”)。
(4)CO2直接排入太空,对物质循环来说是一种损失。科学家开发出CO2循环利用的反应示意图如图所示。
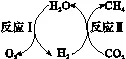
①反应Ⅰ消耗水的质量与反应Ⅱ生成水的质量比为。
②该方案的优点是。
24.(6分)阅读短文,回答问题。
全球汽车产业迎来了一场颠覆性的技术革命——固态电池。这项被誉为“电动车续航救星”的技术,预计将在2026年实现量产。固态电池主要由正极、负极、固态电解质等组成,正极材料与传统锂离子电池类似,负极材料常见的有石墨、硅基材料、锂金属等。锂金属因具有极高的理论比容量,是固态电池负极的理想材料之一,金属锂的熔点低、密度小、质地软,能与水反应生成氢氧化锂和氢气。固态电解质通常以聚氧化乙烯等为基体,添加锂盐形成。与传统锂电池相比,固态电池具有更好的安全性、更高的能量密度和更长的使用寿命。
(1)固态电池充电过程中,电能主要转为能。
(2)石墨作为固态电池的负极材料,主要利用了石墨的性。石墨与金刚石的物理性质差异较大的原因是。
(3)金属锂与水反应可生成氢气。氢气在空气中燃烧的化学方程式是。
(4)与传统锂电池相比,固态电池的优点有(写一种即可)。
25.(7分)由菱铁矿(主要成分为FeCO3,含少量SiO2等杂质)制备铁粉的一种流程如图所示:
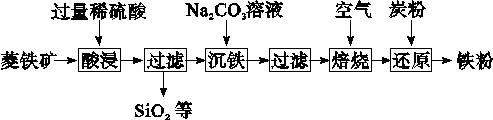
(1)“酸浸”时,为使反应充分,可采取的一种措施是,分析得知二氧化硅(填“能”或“不能”)与稀硫酸反应。
(2)过滤用到的三种玻璃仪器:烧杯、。
(3)“沉铁”时,FeSO4转化为FeCO3沉淀,该反应的基本反应类型是。“焙烧”时,在高温条件下,FeCO3与O2反应生成Fe2O3与CO2的化学方程式为。
(4)“还原”时,在高温条件下,利用炭粉可将铁从氧化铁中还原出来;若向氧化铁与炭粉的混合物中添加适量的CaCO3,更利于还原氧化铁,其原因是。
26.(7分)我国古代文献记载中蕴含着丰富的化学知识。
(1)在《吕氏春秋》中有“金(即铜单质)柔锡(即锡单质)柔,合两柔则刚(即坚硬)”。这句话说明铜锡合金相较于铜、锡的特性是。
(2)我国是最早生产钢铁的国家之一,“百炼成钢”是指将生铁转化为钢,其主要原理是降低生铁中(填元素符号)元素的含量;
(3)“真金不怕火炼”,用化学的知识分析,意思是。
(4)《天工开物》中有“煤饼烧石成灰”的记载,“烧石成灰”指高温下碳酸钙转化为生石灰。
Ⅰ.“石”转化为“灰”的反应属于 (填基本反应类型)
Ⅱ.“灰”遇水成“浆”,该过程(填“放出”或“吸收”)热量。
Ⅲ.“浆”可用于粉刷墙壁,干燥后墙面变硬,发生反应的化学方程式为。
三、实验探究题(本大题共2小题,每个化学方程式2分,其余每空1分,共16分。)
27.(8分)实验探究是学习化学的重要方法。请根据下列实验装置图回答问题。
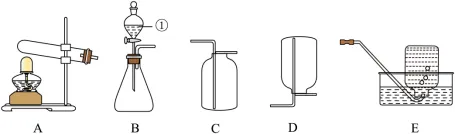
(1)装置B中仪器①的名称是。
(2)实验室用大理石和稀盐酸制取CO2,应选用的发生装置是(填字母序号,下同),实验室加热高锰酸钾固体制取O2,应选用的发生装置是。
(3)实验室制取CO2和O2,均不能选用的收集装置是。
(4)兴趣小组用图甲所示装置探究不同催化剂对过氧化氢分解的催化效果。取大小相同的新鲜土豆块和新鲜猪肝块作催化剂,分别加入10mL相同浓度的过氧化氢稀溶液后,用传感器测量装置中气压的变化,如图乙中曲线a、b所示。
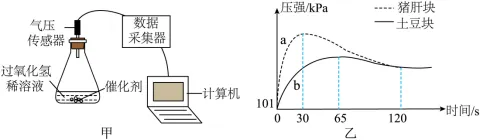
①结合实验和曲线a、b分析,两种催化剂中催化效率更高的是。
②从曲线a、b的变化可以看出,过氧化氢分解的反应是(填“放热”或“吸热”)反应,加猪肝块催化的过氧化氢完全反应所用的时间大约是s(填“30”“65”或“120”)。
③曲线a、b最终达到相同的压强,说明。28
任务一:了解海盐的生产
【查阅资料】海盐分为原盐和精制盐。海盐生产一般采用日晒法,通过纳潮、扬水,将海水引入盐田,经过风吹日晒使水分蒸发,变成饱和卤水,再晒,晶体析出,得到原盐。
【交流讨论】
(1)海水风吹日晒使水分蒸发变成饱和卤水过程中发生改变的是。
任务二:探究海盐的成分
【信息检索】海盐热敷用的是原盐。原盐的主要成分是NaCl,可能含有MgCl2、CaCl2、Na2SO4等物质。
【教师指导】BaSO4、BaCO3、Mg(OH)2均为不溶于水的白色沉淀。
【实验准备】取少量热敷包中的海盐于烧杯中,加足量水充分溶解、过滤,留无色溶液备用。
【进行实验】
(2)为探究海盐成分,小组同学设计如下实验方案,并完成了实验。
实验步骤 | 实验现象 | 实验结论 |
①取少量溶液于试管中,加入过量BaCl2溶液 | 含有Na2SO4 | |
②取步骤①上层清液于试管中,加入过量NaOH溶液 | 产生白色沉淀 | |
② 取步骤②中上层清液于试管中,加入 几滴 | 产生白色沉淀 | 含有CaCl2 |
【反思评价】
(3)步骤③中发生反应的化学方程式为。
(4)小明认为上述步骤③得出的结论不严谨,理由是。
任务三:认识海盐热敷的作用
【咨询专家】海盐热敷是古老的中医疗法。热敷能将热量渗透进体内,驱除体内的病气、寒气,同时海盐内的微量元素,在热敷时更容易进入人体,达到强身健体的效果。
【共同研讨】
(5)热敷时海盐内的微量元素能更快进入人体,从微观角度解释其原因是。
四、计算题(6分)
29.明代科技著作《天工开物》中有关于“火法”冶炼金属锌的工艺记载,主要反应原理为ZnCO3+2C高温Zn+3X↑,现用300 kg炉甘石(主要成分为ZnCO3)与足量碳充分反应,产生锌的质量与加热时间的关系如图所示。
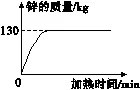
(1)化学方程式中X的化学式为。
(2)计算此炉甘石中ZnCO3的质量分数。(写出计算过程,计算结果精确到0.1%)






