考点1 化学变化和化学性质
1.劳动教育贯穿义务教育阶段,小明的以下家务劳动,发生了化学变化的是( )
A.扫地抹灰 B.摘菜洗菜 C.淘米下锅 D.烧火做饭

2.中国古籍文房四宝指的是“笔、墨、纸、砚”,其中“墨”的主要成分是炭黑。炭黑的下列性质属于化学性质的是( )
A.可燃性 B.常温下呈固态 C.难溶于水 D.熔点高
3.物质的性质决定用途,下列物质的用途主要由其化学性质决定的是( )
A.石墨作电极 B.用熟石灰(显碱性)改良酸性土壤
C.稀有气体作电光源 D.金属铜作导线
4.诗歌是中华文明皇冠上的璀璨明珠。下列诗句与化学变化有关的是( )
A.千锤万凿出深山,烈火焚烧若等闲。《石灰吟》
B.欲渡黄河冰塞川,将登太行雪满山。《行路难》
C.飞流直下三千尺,疑是银河落九天。《望庐山瀑布》
D.八月秋高风怒号,卷我屋上三重茅。《茅屋为秋风所破歌》
考点2 质量守恒定律的应用
5.(2023湖南衡阳中考)实验后试管中残留的硫,常用热的NaOH溶液清洗,发生了如下反应:3S+6NaOH(热) 2SO3+3H2O,则X的化学式为( )
2SO3+3H2O,则X的化学式为( )
A.H2S B.SO2 C.Na2S D.Na2SO4
6.中国计划在2060年前实现“碳中和”,彰显了大国担当。资源化利用CO2是实现“碳中和”的重要途径。如图是CO2转化为甲醇(CH3OH)的微观示意图,关于该反应的说法错误的是()
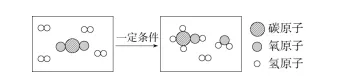
A.该反应体系中共有4种化合物
B.该反应体现了无机物在一定条件下可以转化为有机物
C.参加反应的CO2、H2分子个数比为1∶3
D.参加反应的CO2与H2的总质量等于生成的CH3OH与H2O的总质量
7一定条件下,下列物质在密闭容器内反应一段时间,测得反应前后各物质质量关系如下表。根据表中信息判断,下列说法不正确的是( )
物质 | X | Y | Z | W |
反应前质量/g | 5 | 2.2 | 16.2 | 0.9 |
反应后质量/g | a | 4.4 | 8.1 | 1.8 |
A.a=10
B.该反应属于置换反应
C.Z为化合物
D.反应中Y、W两种物质发生改变的质量比为22∶9
8.密闭容器内有甲、乙、丙、丁四种物质,在一定条件下充分反应,测得反应前后各物质的质量分数如图所示。下列说法正确的是( )
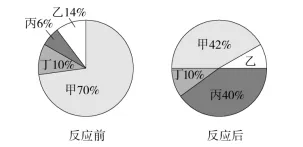
A.物质甲是生成物
B.反应后乙物质的质量分数是18%
C.该化学反应中甲、乙两物质的质量比是14∶3
D.物质丁一定是该反应的催化剂
考点3 化学方程式的书写
9.下列变化的化学方程式书写不正确的是( )
A.红磷在空气中燃烧:P+O2 2O5
2O5
B.碳酸分解:H2CO3 H2O+CO2↑
H2O+CO2↑
C.铁和稀硫酸反应:Fe+H2SO4 FeSO4+H2↑
FeSO4+H2↑
D.硫酸钠溶液与氯化钡溶液混合:Na2SO4+BaCl2  BaSO4↓+2NaCl
BaSO4↓+2NaCl
10.现有O2、Fe、CO、稀硫酸、KOH溶液、CaCO3、MgCl2溶液七种物质,请选择适当的物质按照要求书写化学方程式(每种物质只能选用一次):
(1)化合反应:。
(2)分解反应:。
(3)置换反应:。
(4)复分解反应: 。
11.写出下列反应的化学方程式。
(1)硫在氧气中燃烧:;
(2)铜与硝酸银溶液反应: ;
(3)大理石与稀盐酸反应: 。
考点4 利用化学方程式的计算
12.自贡因盐设市,誉称“盐都”。
电解食盐水能够制得可用于环境消毒的次氯酸钠(NaClO),反应的化学方程式为:NaCl+H2O NaClO+H2↑。试利用化学方程式计算:要制取14.9 g次氯酸钠,理论上需要NaCl的质量。
13.现有碳酸钠和氯化钠的固体混合物10.9 g,加入93.5 g水,固体完全溶解,向该溶液中加入稀盐酸,所得溶液质量与加入稀盐酸质量的关系如图所示。请计算:
(1)恰好完全反应时,生成二氧化碳的质量是g。
(2)恰好完全反应时,所得溶液中溶质的质量分数是多少?(要求写出计算过程)
答案全解全析
1.D 2.A 3.B 4.A 5.C 6.A
7.B 根据质量守恒定律,化学反应前后,物质的总质量不变,则5 g+2.2 g+16.2 g+0.9 g=a g+4.4 g+8.1 g+1.8 g,a=10;反应后,X、Y、W的质量增加,是生成物,Z的质量减小,是反应物,该反应符合“一变多”的特点,属于分解反应;Z是分解反应的反应物,一定是化合物;反应中Y、W两种物质发生改变的质量比为(4.4 g-2.2 g)∶(1.8 g-0.9 g)=22∶9。
8.C 反应后甲的质量分数减少了70%-42%=28%,甲是反应物;反应后乙的质量分数为1-42%-40%-10%=8%;该化学反应中甲、乙两物质的质量比是28%∶6%=14∶3;丁反应前后质量分数不变,可能是该反应的催化剂,也可能不参与反应。
9.A 10.(1)2CO+O2 2CO2(2)CaCO3
2CO2(2)CaCO3 CaO+CO2↑
CaO+CO2↑
(3)Fe+H2SO4 FeSO4+H2↑ (4)2KOH+MgCl2
FeSO4+H2↑ (4)2KOH+MgCl2 Mg(OH)2↓+2KCl
Mg(OH)2↓+2KCl
11.(1)S+O2 SO2(2)Cu+2AgNO3
SO2(2)Cu+2AgNO3 Cu(NO3)2+2Ag (3)CaCO3+2HClCaCl2+H2O+CO2↑
Cu(NO3)2+2Ag (3)CaCO3+2HClCaCl2+H2O+CO2↑
12.解:设理论上需要NaCl的质量为x。
NaCl+H2ONaClO+H2↑
58.574.5
x14.9g
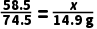 x=11.7g
x=11.7g
答:理论上需要NaCl的质量为11.7g。
13.(1)4.4
(2)解:设恰好完全反应时生成氯化钠的质量为x,原固体混合物中碳酸钠的质量为y。
Na2CO3+2HCl2NaCl+H2O+CO2↑
10611744
yx4.4g
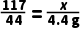 x=11.7g
x=11.7g
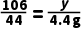 y=10.6g
y=10.6g
恰好完全反应时所得溶液中溶质的质量分数是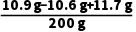 ×100%=6%。
×100%=6%。
答:恰好完全反应时,所得溶液中溶质的质量分数是6%。





