
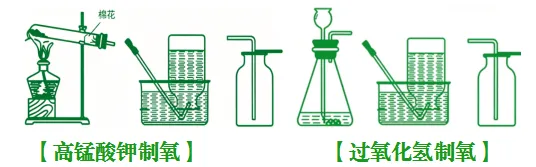
1、发生装置的选择依据:反应物的状态和反应条件(固体加热型或固液常温型)。
2、收集装置的选择依据:氧气的密度比空气大(可用向上排空气法)和不易溶于水(可用排水法)。
3、若用高锰酸钾制取氧气,试管口要放一团棉花,防止加热时高锰酸钾粉末进入导管。
4、加热高锰酸钾制取氧气时,试管口要略向下倾斜,防止冷凝水回流到热的试管底部,使试管炸裂。
5、用排水法收集氧气时,当气泡连续均匀冒出时再开始收集,否则收集的氧气不纯。
6、实验结束时,应先将导管移出水面,再熄灭酒精灯,防止水槽中的水倒吸进入试管,使试管炸裂。
7、氧气的验满方法:用带火星的木条放在集气瓶口,若木条复燃,则氧气已收集满。
8、氧气的检验方法:将带火星的木条伸入集气瓶内,若木条复燃,证明是氧气。
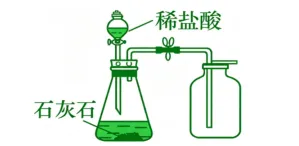
1、反应原理:用大理石或石灰石(主要成分是碳酸钙)与稀盐酸反应制取二氧化碳。
2、化学方程式为CaCO₃+ 2HCl = CaCl₂+ H₂O + CO₂↑。
3、发生装置的选择:属于固液常温型,因为反应物是固体和液体,且反应不需要加热。
4、收集装置的选择:二氧化碳的密度比空气大,能溶于水且与水反应,所以用向上排空气法收集。
5、长颈漏斗的下端要伸入液面以下,形成液封,防止生成的二氧化碳从长颈漏斗口逸出。
6、二氧化碳的验满方法:将燃着的木条放在集气瓶口,若木条熄灭,则二氧化碳已收集满。
7、二氧化碳的检验方法:将气体通入澄清石灰水中,若石灰水变浑浊,证明是二氧化碳。
8、不能用浓盐酸制取二氧化碳,因为浓盐酸具有挥发性,会使制得的二氧化碳中混有氯化氢气体。
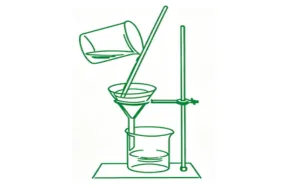
1、过滤是将不溶于液体的固体与液体分离的一种方法。
2、过滤操作需要的仪器有铁架台(带铁圈)、漏斗、玻璃棒、烧杯。
3、过滤时要注意“一贴、二低、三靠”。“一贴”是指滤纸要紧贴漏斗内壁;“二低”是指滤纸边缘要低于漏斗边缘,液面要低于滤纸边缘;“三靠”是指倾倒液体的烧杯口要紧靠玻璃棒,玻璃棒下端要紧靠三层滤纸处,漏斗下端管口要紧靠承接滤液的烧杯内壁。
4、过滤后滤液仍浑浊的原因可能有:滤纸破损、液面高于滤纸边缘、仪器不干净等。
5、过滤操作中玻璃棒的作用是引流,防止液体洒出。
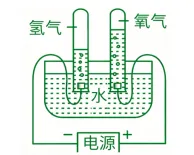
1、实验原理:水在通电的条件下分解生成氢气和氧气。
2、化学方程式为2H₂O 通电2H₂↑ + O₂↑。
3、实验现象:与电源正极相连的试管内产生的气体体积少,是氧气;与电源负极相连的试管内产生的气体体积多,是氢气,且氢气和氧气的体积比约为2:1。
4、实验结论:水是由氢元素和氧元素组成的。
5、在电解水实验中,通常向水中加入少量氢氧化钠溶液或稀硫酸,目的是增强水的导电性。
6、电解水实验中,正极产生氧气,负极产生氢气,说明氧气是由氧元素组成,氢气是由氢元素组成,从而进一步证明水是由氢、氧两种元素组成的。
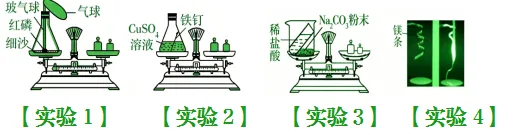
1、质量守恒定律:参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和。
2、红磷燃烧实验中,红磷燃烧的现象是产生大量的白烟,放出热量。
3、红磷燃烧实验要在密闭容器中进行,目的是防止生成的五氧化二磷逸散到空气中,导致天平不平衡,从而验证质量守恒定律。
4、红磷燃烧的化学方程式为:4P + 5O₂点燃2P₂O₅
5、通过红磷燃烧实验可以得出,化学反应前后原子的种类、原子的数目、原子的质量都不变,所以质量守恒。
6、质量守恒定律只适用于化学变化,对于物理变化不适用。

来源 | 网络。文章内容贵在分享,版权归原作者及原出处所有。如涉及版权等问题,请在文末或后台留言联系。


点分享

点收藏

点点赞

点在看







