【考纲要求】
1.掌握化学计算题的常见类型并能综合运用:有关化学式的计算、有关化学方程式的计算、有关溶液的计算等。
2.了解化学计算的一些方法:图像表格分析法、差量法、极值法、守恒法等。

【考点梳理】
考点一、有关化学式、化学方程式、溶液的计算运用
1.有关化学式的计算:
常用的计算公式(以化合物AmBn为例)
(1)相对分子质量=A的相对原子质量×m + B的相对原子质量×n
(2)A元素的质量分数=×100%
(3)A、B元素的质量比:
(4)A元素的质量 ==化合物(AmBn)的质量×A元素的质量分数
(5)混合物中 某物质的质量分数(纯度)=
某物质的质量分数(纯度)=

2. 有关化学方程式的计算:
(1)根据题意设未知数。
(2)根据题意正确书写有关的化学方程式。
(3)根据题意找出有关物质的相对分子质量、已知量和未知量。
(4)按正确比例关系,列出比例式,计算未知数的值。
(5)检验答案是否正确后,简明地写出答案。
3.有关溶液的计算:
(1)溶液中溶质的质量分数
溶质的质量分数=溶质的质量/溶液的质量*100%
(2)溶解度与溶质质量分数的比较
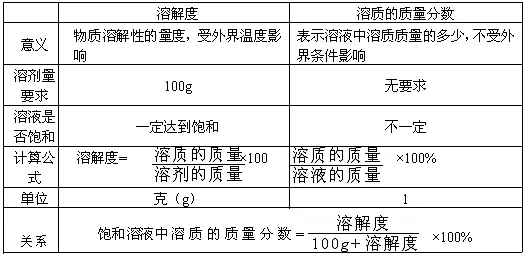
(3)溶质质量分数计算的类型
①溶质、溶剂、溶液的质量与溶质的质量分数的相会换算
②溶质的质量分数与溶液体积、密度的有关换算
溶液的质量=溶液的体积×溶液的密度
溶质的质量分数=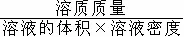 ×100%
×100%
3.溶液的稀释与浓缩的计算
稀释(浓缩)前后溶质的质量不变,即: 浓溶液的质量×浓溶液中溶质的质量分数=稀溶液的质量×稀溶液中溶质的质量分数。
浓溶液的质量×浓溶液中溶质的质量分数=稀溶液的质量×稀溶液中溶质的质量分数。
考点二、化学计算的一些方法
1.公式法
公式法是指直接根据化学概念、原理、定律总结归纳出来的有关计算公式进行解题的方法。如化合物中元素质量比、元素的质量分数、溶液中溶质的质量分数的直接计算。
2.关系式法
关系式法是根基化学式、化学方程式等化学用语和溶质质量分数等概念所包含的各种比例关系,找出已知量与未知量之间的比例关系式,直接列出比例式进行计算的方法。这种方法抓住已知量和未知量的内在联系建立关系式,化繁为简,减少计算误差,也是中考化学计算中常用的方法。
3.差量法
根据化学反应前后物质的质量发生的变化,找出质量形成差量的原因,列出比例求解。
4.守恒法
所谓守恒就是以化学反应过程中存在的某些守恒关系,如:质量守恒、元素守恒、溶液中离子的电荷守恒、混合物中的质量比例守恒等,作为依据,寻求解题的基本思路。
5.平均值法
在解决混合物的计算中,根据计算的需要,取两个极限,分析极限间的平均值,或由平均值分析两个极限的取值。
6.分析法(化归转化)
中考化学试题中大部分综合计算题是把一些基本计算与一些变化有机结合。解答这类试题,首先必须用正确简捷的方法分析理解题意,把一个综合复杂的化学问题分成最简单的组成部分,找出这些部分的本质属性和彼此之间的关系,从而找打解题方案,这种方法叫分析法。如试题中的文字信息、图像信息、表格信息等分析。
2.图像题分析需抓住:
(1)一线:趋势。
(2)二标:横、纵坐标含义。
(3)三点:起点、拐点、终点。
3.表格题分析需抓住:
(1)计算出相邻两次实验之间的差量,观察规律,找出恰好完全反应的位置(必要时可以数形结合)。
(2)找出或计算出实验起始时物质的相关量(即第0次实验的数据)。
(3)根据质量守恒,可将数据转化为生成气体或沉淀(即纯净物)的质量,从而更易于发现反应物之间量的关系并进行相关化学方程式的计算。
例1 Fe和FeO的混合物,测得其中铁元素的质量分数为80%.取该混合物7.0g,加足量稀硫酸完全溶解,生成FeSO4的质量为( )
A.7.6gB.15.2gC.20.0gD.40.0g
【答案】B
【解析】由Fe和FeO的混合物质量为7.0g,铁元素的质量分数为80%,解出铁元素质量为:7.0g×80%=5.6g,用铁元素质量除以硫酸亚铁中铁元素的质量分数,算出硫酸亚铁的质量:=15.2g。
例2 称取30克由两种金属组成的混合物,跟足量稀硫酸反应,生成氢气2克,则该金属混合物的组成可能是( )
A.Al和Mg
B.Cu和Mg
C.Mg和Fe
D.Fe和Zn
【答案】BC
【解析】Mg、Al、Fe、Zn分别与稀硫酸反应放出2克氢气,各需要:Al-18克;Mg-24克;Fe-56克;Zn-65克。题中该混合物 30克与稀硫酸反应生成2克的氢气,而Al、Mg小于30克,Fe、Zn、Cu(Cu不与稀硫酸反应,可看做很大)大于30g,这样很容易判断混合物必须是一个大于30克的,一个是小于30克的。
例3 若有某种不纯的金属M,含有不溶于水也不溶于酸的杂质,取该金属样品2克投入10克20%的稀盐酸中恰好完全反应,测得该金属与盐酸反应生成的氯化物中含氯50%,则样品中M的质量分数为( )
A.96%B.92%C.97.25%D.98%
【答案】D
例4 (攀枝花)有铁粉和铜粉的均匀混合物,甲、乙、丙三位同学分别取该混合物与稀硫酸反应,所得数据如下表所示:
甲 | 乙 | 丙 | |
取用金属混合物的质量/g | 10 | 10 | 20 |
取用稀硫酸的质量/g | 100 | 120 | 100 |
反应后过滤,得干燥固体的质量/g | 4 | 4 | 13 |
请分析数据,回答下列问题:
(1)甲所得溶液中含有溶质的是____________________。
(2)根据实验数据分析,若取用金属混合物15g,加入到120g稀硫酸中,充分反应后最终得到固体质量为_____________g。
(3)计算丙同学所得溶液中溶质的质量分数。(写出计算过程,计算结果精确到0.1%)
【答案】(1)H2SO4、FeSO4(2)6.6
(3)由甲、乙两同学实验数据对比知:10g金属混合物中铁已完全反应,剩余4g固体为铜,由此推知20g金属混合物中含铜8g。由于丙同学实验剩余的13g固体中含铁5g,故丙同学实验中硫酸已完全反应,且参加反应的铁为7g。
设生成硫酸亚铁的质量为x,生成氢气的质量为y。
Fe+H2SO4=FeSO4+H2↑
56 152 2
7g x y
x=19g y=0.25 g
反应后溶液质量为:20g-13g+100g-0.25g=106.75 g
反应后溶液中硫酸亚铁的质量分数为:×100%=17.8%。
答:丙同学所得溶液中硫酸亚铁的质量分数为17.8%。
中考化学计算题答题技巧总结
1. 审题技巧
仔细读题,找出已知条件,明确所求问题,注意单位换算,识别隐含条件。
2. 解题思路
先判断属于哪种计算类型,选择合适的计算方法,按步骤规范书写,检查计算结果。
3. 检查要点
化学方程式是否正确,比例式是否列对,计算是否有误,单位是否统一,有效数字是否保留。






