此模拟卷涉及本公众号的相关知识专题链接:
(初高衔接)氧化还原反应与应用【自招/竞赛/培优系列讲解视频】
化学实验探究专题 2/2 物质性质的探究和综合探究【自招/竞赛/培优系列讲解视频】
化学实验探究专题 1/2 物质组成及变化的探究【自招/竞赛/培优系列讲解视频】
此卷电子版需要私信联系索取,答案发在“自招驿站物化交流群”里,感兴趣者进群自取。
(时间:60分钟满分:80分)
可能用到的相对原子质量:H-1C-12N-14O-16Na-23Mg-24S-32Cl-35.5Ca-40Fe-56Zn-65Ba-137Al-27Cu-64Be-9
第Ⅰ卷(共 25 分)
(略)
第Ⅱ卷(共 55 分)
三、非选择题(本题共 4 小题,共 45 分)。
21.(11 分)2025 年 12 月,中国空间站三舱组合体稳定运行,神舟二十一号乘组在轨开展多项科学实验。
(1)空间站氧气供给依靠“氧再生环控生保技术”,核心是通过化学反应电解水制氧,此反应遵循质量守恒定律的本质原因是;空间站需源源不断为呼吸提供O2,备用装置可应急提供O2,其原理是:NaClO3 固体受热分解产生O2,均匀添加于其中的适量金属锰(Mn)在氧气中燃烧生成氧化物,有助于快速产生O2。添加金属Mn的作用分别是、。
(2)偏二甲肼(C2H8N2 )和四氧化二氮(N2O4 )做推进剂,这两种物质有毒,常温下可存储。点燃后反应生成氮气、二氧化碳和水,反应的化学方程式为;目前我国航天选这组燃料的原因除反应能释放大量的能量外,还具有的优点有。
(3)天然橡胶耐温范围窄、抗辐射性差,太空环境下易老化、脆裂,失去密封性。空间站舱外航天服使用特种橡胶作密封材料,该特种橡胶具有的性质有 (填一种)。
(4)空间站开展微重力环境下科学实验,制备新型钛合金材料。钛铁矿(主要成分为FeTiO3)是制备钛的原料之一,FeTiO3可表示为氧化物形式 FeO•TiO2,则钛酸镁(MgTiO3 )的氧化物形式可表示为;
FeTiO3与稀硫酸发生复分解反应的化学方程式为 。
22.(11 分)二氯化二硫(S2Cl2)常温下是一种金黄色液体(沸点 138℃),广泛应用于化工领域。已知 S2Cl2 热稳定性较差,且遇水反应生成 S、SO2 和 HCl,还可被 Cl2 氧化为 SCl2(沸点 59℃)。实验室采用如图所示装置模拟工业生产,把氯气通入熔融硫黄中制备 S2Cl2(A、B 图中加热仪器已略去)。
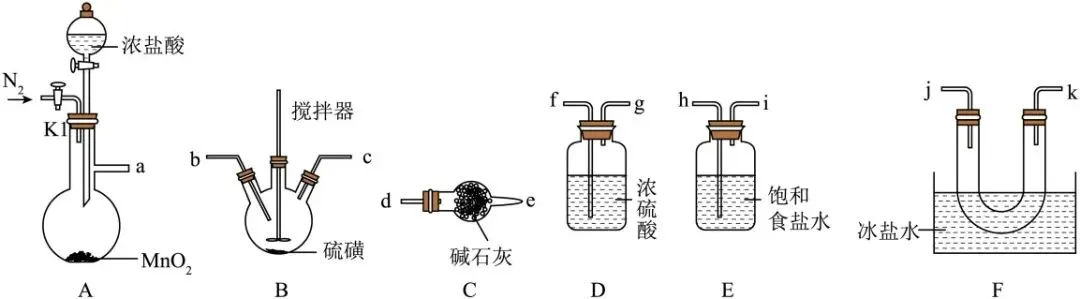
回答下列问题:
(1)请根据 S、Cl 的原子结构,推断 S2Cl2 中 S 元素的化合价为。
(2)装置 A 中制备 Cl2,按接口从左到右,装置的连接顺序为 a→→d(填小写字母)。
(3)装置 C 中所装碱石灰的作用是。观察到 F 中出现(填现象)时,可证明有 S2Cl2生成。
(4)为了提高 S2Cl2 的纯度,实验的关键是控制好温度和。
(5)若拆除装置 D,对产物造成的影响是(填化学方程式)。
(6)测定某市售S2Cl2 纯度(杂质不影响测定):称取 3.0g 样品于烧瓶中,加入足量的蒸馏水充分反应,用水蒸气将生成的 SO2 和 HCl全部蒸出,并用足量的 H2O2 溶液充分吸收;然后向其中加入足量的 BaCl2 溶液,过滤、洗涤、干燥、称量,得到 2.33g 固体。样品中 S2Cl2 的质量分数为。
23.(11 分)碘化钾(KI)保存不当会变质。实验小组进行以下实验探究 KI 变质的因素。
【提出问题】 KI 变质的条件是什么?
【查阅资料】①KI为白色粉末,暴露在空气中或久置会被氧化为碘(I2)而泛黄变质。
② 碘水中含较多 KI 时,滴加淀粉溶液显紫色或蓝紫色
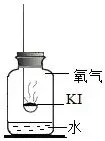
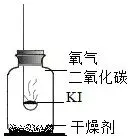
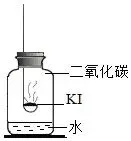
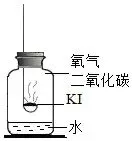
【进行实验】分别取适量 KI 于燃烧匙中,再分别放入盛有不同物质的集气瓶中,塞紧胶塞,若干天后观察。
实验 1 | 实验 2 | 实验 3 | 实验 4 |
|
|
|
|
固体变潮、表面变微黄 | 固体无明显现象 | 固体变潮、无其他明显现象 | 固体变潮、表面变黄 |
【继续实验】取实验 1 中少量微黄固体溶解,加入淀粉溶液,溶液变紫色。取实验 4 中少量黄色固体溶解,加入淀粉溶液,溶液变紫色。
【解释与结论】(1)实验 3 的目的是。
(2)对比实验,可以得出 KI 变质一定与水有关。
(3)从上述实验可推知,KI 变质的条件是。
【提出问题 2】CO2 的作用是什么?
【进行实验】分别取10mL同浓度的KI溶液于3支试管中,再向试管2中通入CO2,向试管3中滴加几滴盐酸;分别测溶液的 pH;几分钟后,观察溶液的颜色;再向试管中滴入淀粉溶液,观察溶液的颜色。记录如下
试管序号 | 1 | 2 | 3 |
溶液 pH | pH=8.5 | pH=6.5 | pH=4.5 |
溶液颜色 | 无色 | 浅黄色 | 黄色 |
滴加淀粉溶液后的颜色 | 无色 | 紫色 | 深紫色 |
较长时间后,观察到试管 1 中溶液变为紫色。
【解释与结论】(4) CO2在 KI 变质过程中的作用是。
(5)碘化钾在空气中久置变质的化学方程式为。
【反思与评价】(6)探究碘化钾变质条件时,同学们直接排除氮气和稀有气体的影响,其原因是。
24.(12分)将ZnSO4 溶液与Na2CO3溶液混合,产生白色固体。对白色固体组成进行下列探究。
探究一:【猜测】白色固体含ZnCO3、Zn(OH)2 、Zn5(OH)8SO4 中的一种或几种。
【资料】Zn(OH)2、ZnCO3加热易分解,生成对应 两种氧化物。Zn5(OH)8SO4不溶于水,能溶于酸。
【实验】(1)取适量白色固体,溶于_________,出现气体,则固体中含ZnCO3;向所得溶液中滴加_________,无明显现象,则固体中不含Zn5(OH)8SO4。
(2)另取适量白色固体,充分加热,产生的气体使无水CuSO4粉末变_________色,则固体中含Zn(OH)2。
探究二:查阅资料得知上述固体应为碱式碳酸锌[Znx(OH)y(CO3)z .mH2O],其受热会分解生成ZnO、H2O和CO2。
取一定量该固体,充分加热,将生成的气体依次用足量的浓硫酸和烧碱溶液充分吸收。
(3)实验测得剩余固体质量2.43g,浓硫酸增重0.72g,烧碱溶液增重0.44g。则x:y:z:m=_________。
(4)若生成的CO2未被烧碱溶液完全吸收,则测得的碱式碳酸锌中的m值____(选填“偏大”、“不变”或“偏小”)。
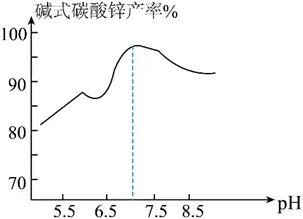
探究三:(5)如图为ZnSO4 和Na2CO3反应时溶液的pH对碱式碳酸锌产率的影响。以含少量CuO的ZnO为原料制备碱式碳酸锌,设计实验方案:向原料中加入稍过量的稀硫酸,搅拌至充分反应,再向其中加入________,搅拌至充分反应,过滤;向滤液中滴入Na2CO3溶液并,充分反应至产生大量固体,、洗涤、干燥。
四、附加题(共 1 小题,共 10 分)
25.(10 分)铍及其氧化物广泛应用于原子能、航天、电子、陶瓷等领域,是重要的战略物资。利用绿柱石(主要成分为Be3Al2Si6O18,还含有一定量的FeO和Fe2O3 )生产 Be 的一种工艺流程如下图。 


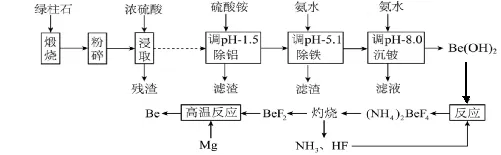
已知:①绿柱石的主要成分写成氧化物的形式为3BeO.Al2O3.6SiO2 。
②Be与Al在元素周期表中的位置符合对角线规则,BeO与Al2O3性质相似,Be(OH)2与Al(OH)3性质相似,Be元素在碱性溶液中的存在形态为[Be(OH)4]2-。
③Fe3+沉淀完全的pH = 3.0,Fe2+沉淀完全的pH = 9.0。回答下列问题:
(1)浓硫酸浸取后所得溶液中的金属阳离子有 ;残渣的主要成分是 。
(2)“浸取”中浓硫酸的作用除了用于溶解矿石外,还起的作用为。
(3)得到(NH4)2BeF4 的化学方程式为。
(4)该流程中能循环使用的物质有 NH3 和 HF 和(填化学式)。
(5)“沉铍”时,用NaOH溶液代替氨水,则产生Be(OH)2的量会减少,请用化学方程式说明原因。
(6)若绿柱石中 BeO 的含量为 a%,1吨绿柱石能生产含铍 2%的合金 b 吨,则Be的利用率为(用含 a、b 的代数式表示)。