一、选择题 (每小题只有一个选项符合题意)
1.(湖南)下列溶液中,能使酚酞试液变化的是()
A.烧碱溶液
B.稀硫酸
C.稀盐酸
D.醋酸溶液

2.下列物质露置在空气中,质量不变的是()
A.汽油
B.浓硫酸
C.氧化钙
D.碳酸钠
3.下列物质中,不需密封保存的是( ) A.浓硫酸
B.氢氧化钠
C.大理石
D.澄清石灰水
4.下列关于盐酸的描述中,错误的是( ) A.盐酸中的溶质是HCl B.盐酸能使石蕊试液变蓝 C.人体胃液中含有盐酸,可以帮助人体消化
D.打开盛有浓盐酸的试剂瓶瓶盖,瓶口处有白雾出现
5.如图所示,已平衡的天平两端放着两个分别盛有浓盐酸和浓硫酸的敞口烧杯。过一段时间后,天平会()
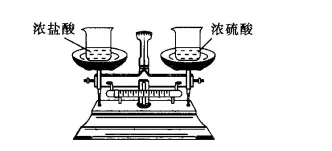
A.左端下沉
B.右端下沉
C.仍然平衡
D.无法判断
6.物质的性质决定其保存方法。固体氢氧化钠具有以下性质:①白色固体;②有腐蚀性;③易吸收水分;④能与空气中的二氧化碳反应。由此可知,氢氧化钠固体必须密封保存的主要原因是()
A.①②B.②③
C.①③D.③④
7.酸具有酸的通性的原因是()
A.酸都能电离出H+
B.酸都含有酸根
C.酸中都含有氢元素
D.酸中都含有氧元素
8.对于反应:X+Ca(OH)2=Y+Cu(OH)2↓,下列分析中正确的是()
A.该反应类型可能是置换反应
B.X和Y的相对分子质量之差为18
C.X可能是CuCl2或Fe2(S04)3
D.X可能是CuCl2或Cu(N03)2
9.下列有关氢氧化钠性质的说法错误的是()
A.氢氧化钠有腐蚀性
B.固体氢氧化钠有挥发性
C.氢氧化钠能吸收二氧化碳而变质
D.固体氢氧化钠能吸收水蒸气而潮解
10在生活、生产和科学研究中,常用pH试纸测定溶液的pH。以下测定操作正确的是()
A.将被测液滴到放在玻璃片上的pH试纸上,显色后,与标准比色卡比较
B.将pH试纸直接投入被测液中,显色后,取出与标准比色卡比较
C.先用少量水湿润试纸,后滴上被测液,显色后,与标准比色卡比较
D.先用蒸馏水清洗滴管,随后吸取被测液滴到试纸上,显色后,与标准比色卡比较
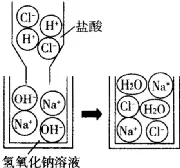
11.如图所示是盐酸滴入氢氧化钠溶液中有关粒子之间反应的示意图,下列说法错误的是()
A.盐酸溶液中含有氢离子和氯离子
B.氢氧化钠溶液中含有钠离子和氢氧根离子
C.两种溶液混合时,氢离子与氢氧根离子结合生成了水分子
D.两种溶液混合时,钠离子与氯离子结合生成了氯化钠分子
12下列各组物质分别加入足量的水中,能得到无色透明溶液的是()A.FeCl3、NaOH、NaCl
B.Na2SO4、HCl、BaCl2
C.CuSO4、KCl、HClD.Na2CO3、NaCl 、Na2SO4
13.下列各组离子在溶液中一定能大量共存的是()
A.H+、OH-、Na+
B.Ca2+、OH-、CO32-
C.Na+、K+、Cl-
D.H+、NO3-、CO3 2-
二、填空题
14..只用H、C、O、Cl、Ca五种元素中的一种或几种,按要求,各写出一个化学式:
(1)可用作食品干燥剂的氧化物是______________;
(2)胃液中的酸是______________;
(3)可用于改良酸性土壤的碱是______________;
(4)敞口放置的石灰水瓶壁上形成的白色物质是______________。
15如图所示,是某同学所做的甲、乙、丙三组实验。
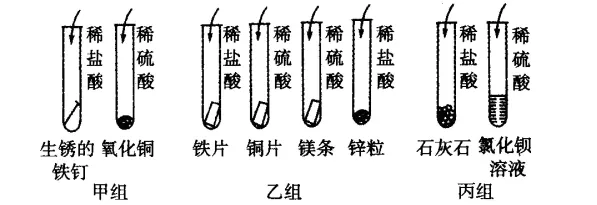
现象:甲组中,铁钉表面的锈消失,溶液显黄色;氧化铜黑色粉末消失,溶液显蓝色。乙组中,铁片、镁条、锌粒表面产生气泡,铜片无变化。丙组中,石灰石表面产生气泡,石灰石溶解;盛有氯化钡的试管中产生白色沉淀。
请你根据实验和现象,运用分析、对比、归纳等方法,归纳总结出酸的几条性质(至少写三条)。
(1)。
(2)。
(3)。
16.化学晚会上,小豆把一张白纸的正反两面向大家展示清楚,然后把白纸用电吹风的热风吹了片刻,白纸上出现了一只小黑猫(如图所示),大家惊奇不已。你知道这是怎么回事吗?请你用学过的化学知识来解释。

(1)小豆事先用________画了一只猫。
(2)使白纸出现黑猫的物质是________,该物质具有________性。
17.生石灰是白色的块状物,应用广泛。
(1)生石灰的主要成分为________(填化学式)。在食品包装中,常用生石灰做干燥剂,其干燥原理是(用化学方程式表示)。
(2)在农村,生白灰常用于畜禽栏舍的消毒。畜禽出栏后,将生石灰用水调成20%的石灰乳,涂刷墙面和地面。某农户误将生石灰直接撒在猪圈中消毒,一段时间后发现猪的蹄部干燥开裂,有的甚至出现灼伤、溃疡,原因是。
(3)上述用于消毒的浆状物要现配现用,放置过久就没有消毒的作用了,其原因是(用化学方程式表示)。
18.小军在一次实验中,将带有铁锈的铁片放入一定量的稀硫酸中,细心观察,发现下列现象:①铁锈逐渐消失,溶液变为黄色;②铁片表面有气泡产生,溶液由黄色逐渐变成浅绿色。回答:
(1)写出现象①中反应的化学方程式:。
(2)写出现象②中产生气泡的反应化学方程式:。
19对牙膏的探究要用到许多化学知识,下表列出了三种牙膏中的摩擦剂。
两面针儿童牙膏 | 珍珠王防臭牙膏 | 中华透明牙膏 | |
摩擦剂 | 氢氧化铝 | 碳酸钙 | 二氧化硅 |
(1)根据你的推测,牙膏摩擦剂的溶解性为________(填“易溶”或“难溶”)。
(2)牙膏中的摩擦剂碳酸钙可以用石灰石来制备,某学生设计了一种制备碳酸钙的实验方案,其流程如图所示:
请写出上述方案中有关反应的化学方程式:
①; ③
(3)检验牙膏中是否含有碳酸盐的实验方法是
。
三、实验探究题
20已知澄清石灰水中存在水分子、钙离子、氢氧根离子。某同学对澄清石灰水进行探究,想知道哪种粒子能使酸碱指示剂变色。
实验步骤及内容 | 实现现象 | 实验结论 |
(1)在一支试管中加入适量蒸馏水,再滴入几滴酚酞试液 | ||
(2)在一支试管中加入适量CaCl2溶液,再滴入几滴酚酞试液 | ||
(3)在一支试管中加入适量澄清石灰水,再滴入几滴酚酞试液 |
21.某化学活动小组以“酸碱盐的性质”为主题进行探究性学习,请你作为该小组成员一起来解决下列问题:
(1)小红同学从农田里取来一份土壤样品,如果检测结果呈酸性,从经济和可行方面考虑,那么要改良此土壤的酸性,应向农田里施加________(填化学式)。
(2)小红同学用下图总结了NaOH的四条化学性质(即NaOH与四类物质能够发生化学反应)。
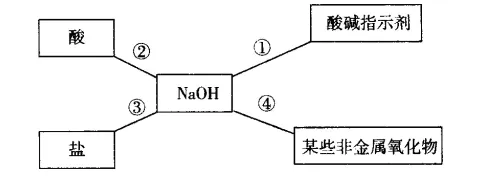
Ⅰ.为了验证反应①,小红将无色酚酞试液滴入NaOH溶液中,溶液由无色变成________。
Ⅱ.依据反应④说明NaOH必须密封保存,否则在空气中要变质,其化学反应方程式为。
Ⅲ.为了验证反应③能够发生,你选择的物质是________。
A.Na2CO3B.HClC.FeCl3D.Ba(NO3)2
22.硫酸是常见的酸,也是常用的化工原料。
由于浓度不同,浓硫酸与稀硫酸在性质上存在较大的差异,如浓硫酸具有脱水性、吸水性和强腐蚀性等。某课外兴趣小组为了探究浓硫酸的某些特性做了如下一些实验。请结合有关实验,按要求回答下列问题:
(1)用玻璃棒蘸取少量浓硫酸在滤纸上写字,过后观察,字迹显黑色,这主要是由于浓硫酸具有________性,使纸中的纤维素碳化的缘故;在洗气瓶中盛放浓硫酸,除去氢气或氧气中水分,利用其________性。
(2)探究浓硫酸的吸水性。兴趣小组把98%的硫酸10 mL和63.3%的硫酸(用10 mL 98%的硫酸与10 mL水配成)约20 mL分别放入两个相同的大表面皿中,称量,观察,记录,分析。
根据室温环境下实验的数据绘成的曲线如图所示:
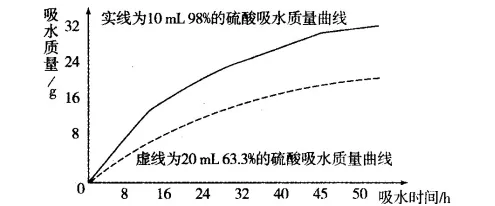
①稀释浓硫酸时,应将______缓缓地注入盛有________的烧杯中并不断搅拌。②由如图曲线你能得到的实验结论有哪些?(写一点)。
(3)探究浓硫酸能否使铁钝化(钝化指在表面形成氧化膜保护层,使内层金属不再发生变化)。
可选用的实验药品有相同铁片若干、浓硫酸、稀硫酸、硫酸铜溶液等。实验仪器任选。
①兴趣小组已经完成下表实验Ⅰ和Ⅱ,请你帮他们将实验报告补充完整。
方案 | 实验假设 | 实验方案 | 实验现象与结论 |
Ⅰ | 能发生钝化 | 取一铁片先插入浓硫酸中,一段时间后取出,再插入硫酸铜溶液中。 | 无明显变化,假设成立。 |
Ⅱ | 能发生钝化 | 取两片相同的铁片,一片放入浓硫酸中,一段时间后取出,再与另一片同时放入硫酸铜溶液中。 | ________,假设成立。 |
你认为方案Ⅱ与方案Ⅰ相比,方案Ⅱ的优点是。
②某同学将一铁片插入盛有98%的浓硫酸的试管中,无明显变化,再给试管加热一段时间后,发现溶液变色并有刺激性气味气体产生,此现象说明。






