中考化学实验基本操作速记手册2
二、重要的实验
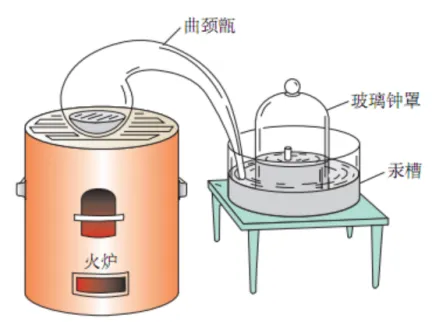
1. 拉瓦锡测定空气成分
| 原理 | 2Hg+O2△=====2HgO |
现象 | 银白色液体表面出现红色粉末 | |
原理 | 2HgO△=====2Hg+O2 | |
现象 | 红色粉末分解,产生气体和银白色液体 | |
结论 | 空气由氧气和氮气组成 |
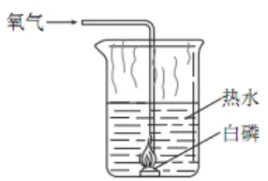
2. 燃磷法测定空气成分
| 原理 | 4P+5O2点燃=======2P2O5 |
现象 | 红磷燃烧产生大量白烟,冷却后打开弹簧夹,烧杯内的水沿导管流入集气瓶,约占瓶内空气体积的1/5。 | |
结论 | 氧气约占空气体积的五分之一 | |
氮气不溶于水、不燃烧、不支持燃烧 | ||
药品的替代注意点 | 能用铁丝代替红磷:铁丝在空气中不能燃烧 | |
不能用木炭代替红磷:木炭燃烧会生成二氧化碳气体,装置中压强不会减小。 | ||
若要用硫粉代替红磷,则要将集气瓶中的水换为氢氧化钠溶液(吸收生成的二氧化硫) | ||
药品的选择原则 | 药品在空气中易燃 | |
药品只能与空气中的氧气反应 | ||
尽可能选择与氧气反应只生成固体的物质,若选择的物质与氧气反应生成气体,则需要用适当的试剂吸收 | ||
误差分析 | 偏小 | 红磷不足 |
装置漏气 | ||
装置未冷却至室温就打开弹簧夹 | ||
偏大 | 红磷点然后伸入集气瓶过慢 | |
止水夹未夹紧或未使用止水夹,造成红磷燃烧时空气受热膨胀溢出。 |
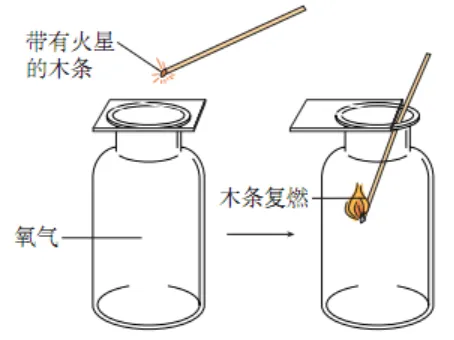
3.氧气的验满和检验
| 验满 | 方法 | 带火星的木条靠近集气瓶口 |
现象 | 带火星的木条复燃 | ||
结论 | 氧气已集满 | ||
检验 | 方法 | 燃着的木条插入集气瓶中 | |
现象 | 木条燃烧更旺 | ||
结论 | 该气体是氧气 |
| 空气 | 现象 | 发出微弱的淡蓝色火焰 | 生成有刺激性气味的气体 |
氧气 | 发出明亮的蓝紫色火焰 | |||
结论 | 氧气支持燃烧,并且氧气浓度越大,燃烧越剧烈 | |||
集气瓶中水的作用 | 吸收产生的二氧化硫气体,防止污染空气。 |
| 空气 | 现象 | 发出红光 | 生成使澄清石灰水变浑浊的气体 |
氧气 | 剧烈燃烧,放出白光 | |||
结论 | 氧气支持燃烧,并且氧气浓度越大,燃烧越剧烈 |
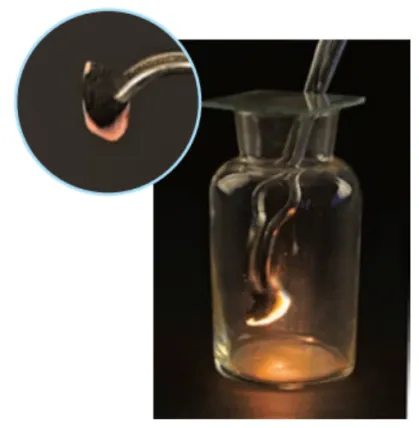
| 空气 | 现象 | 发出红光 |
氧气 | 剧烈燃烧,火星四射,生成黑色固体 | ||
结论 | 氧气支持燃烧,并且氧气浓度越大,燃烧越剧烈 |
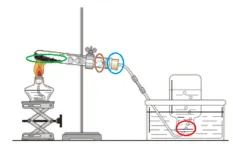
| 装置要点 | 绿椭圆处 | 药品要平铺 |
橙椭圆处 | 试管口要放一团棉花(防治粉末堵塞导管) | ||
蓝椭圆处 | 试管口略向下倾斜(防止冷凝水回流) | ||
红椭圆处 | 导管只要稍深入到集气瓶内(利于排尽水) | ||
步骤 | 茶(查)庄(装)定点收利(离)息(熄) |
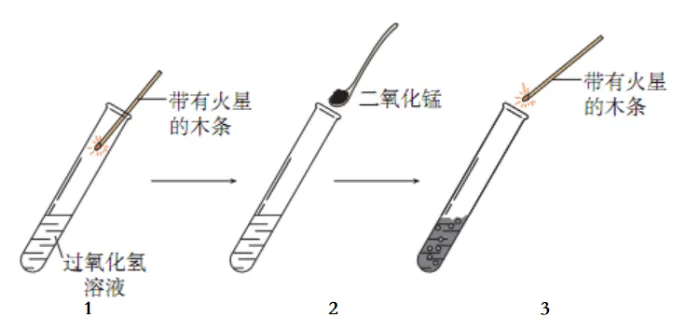
8. 分解过氧化氢制氧气中二氧化锰的作用
| 实验1 | 带火星木条不复燃 |
实验2 | 加入二氧化锰后带火星木条复燃 | |
实验3 | 重新加入过氧化氢溶液,带火星木条复燃 | |
结论 | 二氧化锰能加快过氧化氢分解的速度 | |
催化剂 | 概念 | 在化学反应中能改变其他物质的化学反应速率,而本身的质量和化学性质在反应前后没有发生变化的物质 |
特点 | 一变 | 改变其他物质化学反应速率 |
两不变 | 本身质量、化学性质(在反应前后) |
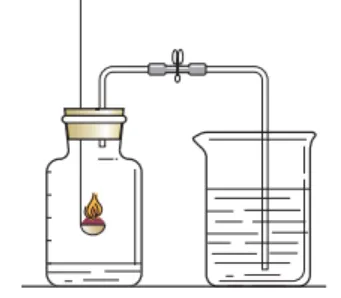
| 烧杯A | 现象 | 无色酚酞溶液变红 |
解释 | 烧杯B中浓氨水挥发出氨气,与A烧杯中的水结合,生成氨水(呈碱性) | ||
烧杯B | 现象 | 无明显现象 | |
解释 | 烧杯A中酚酞分子能运动,但不会挥发,进入烧杯B中。 | ||
结论 | 分子在不断的运动 |
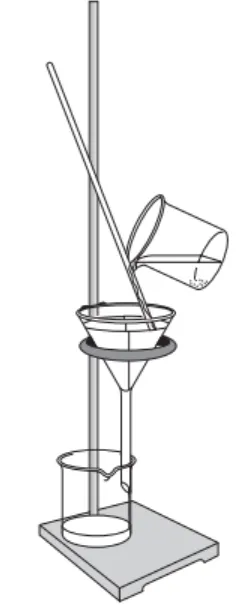
| 作用 | 除去难溶性杂质 |
装置要点 | 一贴 | 滤纸紧贴漏斗内壁,中间不要留有气泡,若有较多气泡会使过滤速率减慢。 |
二低 | 滤纸边缘比漏斗口稍低,防止液体从漏斗外溢出 | |
漏斗内液面比滤纸边缘低,防止液体未经过滤,从滤纸和漏斗间隙中流下。 | ||
三靠 | 玻璃棒斜靠在三层滤纸处,防止玻璃棒捅破润湿的滤纸造成过滤失败; | |
倾倒液体时,烧杯口紧靠玻璃棒,用玻璃棒引流防止液体溅出; | ||
漏斗下端的尖端部分紧靠烧杯内壁,使滤液沿烧杯壁流下,防止滤液向四周飞溅。 | ||
说明 | 经过滤后的液体依然是混合物(含有可溶性杂质) |
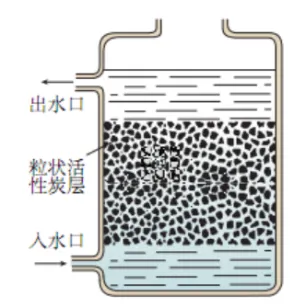
| 作用 | 通过过滤和吸附,除去水中杂质 |
活性炭的作用 | 过滤和吸附,除去水中难溶性杂质、色素和异味 | |
进水方式解释 | 入水口在下,出水口在上,可以延长过滤和吸附的时间,使得水过滤和吸附更充分。 |
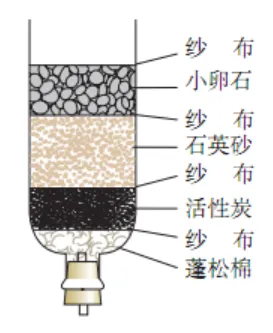
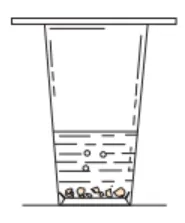
12. 简易净水器
| 作用 | 通过过滤和吸附,除去水中杂质 |
活性炭的作用 | 过滤和吸附,除去水中难溶性杂质、色素和异味 | |
小卵石作用 | 除去大颗粒难溶物 | |
石英砂作用 | 除去小颗粒难溶物 | |
纱布作用 | 分隔各类物质、过滤 | |
蓬松棉作用 | 支撑(防止堵塞出水口)和过滤 |
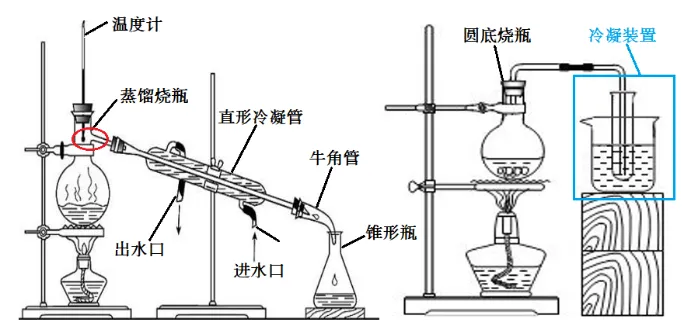
13. 蒸馏装置
| 作用 | 制取蒸馏水 |
温度计的液泡位置 | 蒸馏烧瓶支管出口处 | |
石棉网作用 | 使烧瓶均匀受热 | |
冷凝管作用 | 冷凝水蒸气 | |
简易装置的长导管作用 | 导气和冷凝 | |
沸石的作用 | 防暴沸 | |
蒸馏装置 | 简易蒸馏装置 | 进水方式:下口进水,上口出水(冷凝更充分) |
| 操作 | 把等量的肥皂水分别滴加到盛有等量的两种水样中,并振荡。 |
现象和结论 | 现象 | 结论 |
较少的浮渣较多的泡沫 | 该水样为软水 | |
较多的浮渣较少的泡沫 | 该水样为硬水 |
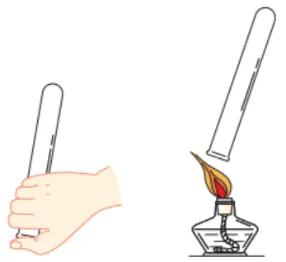
| 操作 | Ⅰ.用拇指堵住集满氢气的试管 Ⅱ.靠近火焰,移开拇指点火 |
现象和结论 | 现象 | 结论 |
若声音微弱 | 氢气纯净 | |
若声音尖锐(爆鸣声) | 氢气不纯净 |
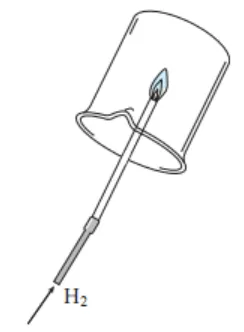
| 操作 | 在带尖嘴的导管口点燃纯净的氢气,并在火焰方罩一个冷而干燥的小烧杯 |
现象和结论 | 现象 | 结论 |
1.火焰为微弱的淡蓝色 2.烧杯内壁出现水滴 3.放出大量的热 | 1.氢气有可燃性 2.水由氢氧元素组成 |
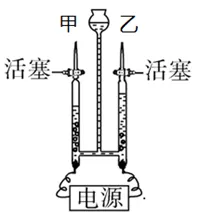
| 原理 | 2H2O通电=======2H2↑+O2↑ |
实验现象 | 现象 | |
两极均产生气泡 | ||
正极 | 负极 | |
正极收集到气体体积大 | 负极收集到气体体积小 | |
产物检验 | 正极 | 负极 |
用燃着的木条靠近玻璃管尖嘴处或试管口,木条燃烧更剧烈,证明是氧气 | 点燃时可以燃烧,燃烧产生淡蓝色火焰,证明是氢气。 | |
结论 | 水是由氢元素和氧元素组成的化合物 | |
加入硫酸钠或氢氧化钠作用 | 增强溶液的导电性 | |
拓展 | 氢氧元素质量比=1:8 |
| 操作 | 将玻璃导管在酒精灯上烧至红热,迅速塞紧橡皮塞,并将红热玻璃与红磷接触 |
现象和结论 | 现象 | 结论 |
1.红磷燃烧,产生白烟 2.气球先膨胀后收缩 3.完全冷却后天平平衡 | 反应前后总质量不变 |
| 操作 | 将打磨干净的铁钉浸没到硫酸铜溶液中 |
原理 | Fe+CuSO4=FeSO4+Cu | |
现象和结论 | 现象 | 结论 |
1.铁钉表面析出红色固体 2.溶液由蓝色变为浅绿色 3.天平依然平衡 | 反应前后总质量不变 |
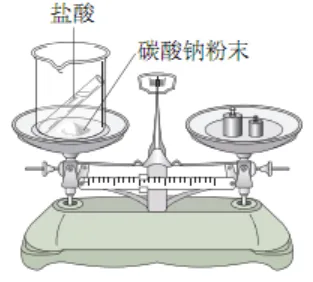
| 操作 | 将小试管倾斜,使小试管中盐酸进入烧杯中。 |
原理 | Na2CO3+2HCl=2NaCl+H2O+CO2↑ | |
现象和结论 | 现象 | 结论 |
1.白色粉末不断溶解 2.产生大量气泡 3.天平左端上升,右端下沉 | 有气体生成的反应,在非密闭容器中进行,反应后总质量减少。 |
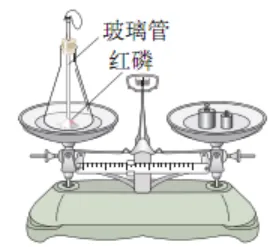
21. 镁条燃烧前后质量的测定
| 操作 | 将打磨干净的长镁条和陶土网一起放在天平上称量,在陶土网上方点燃镁条;再将镁条燃烧产物与陶土网一起放在天平上称量,比较反应前后的质量。 |
原理 | 2Mg+O2点燃=======2MgO | |
现象和结论 | 现象 | 结论 |
1.镁条剧烈燃烧,发出白光 2.生成白色粉末状固体 3.反应后总质量大于反应前总质量 | 有气体参加的反应,在非密闭容器中进行,反应后总质量增加。 |
22. 铜丝表面的氧化铜与氢气加热条件下反应
| |
现象 | 黑色逐渐变成亮红色,试管内有水雾出现。 |
原理 | H2+CuO△=====Cu+H2O |
结论 | 氢气具有还原性 |
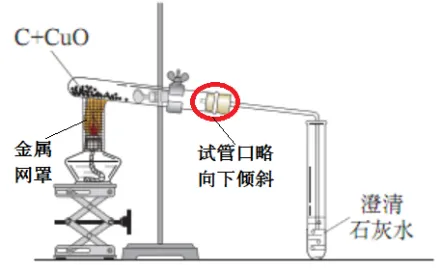
| 操作 | 先预热,再对准药品部位集中加热。 |
原理 | 2CuO+C高温=======2Cu+CO2↑ | |
操作步骤 | 先撤出导气管,待试管冷却再把试管中的粉末倒出。 | |
现象和结论 | 现象 | 结论 |
1.黑色粉末逐渐变红 2.澄清石灰水变浑浊 | 单质碳能与氧化铜在高温下反应,单质碳具有还原性。 | |
金属网罩的作用 | 集中火焰,提高温度。 |
| 操作 | 将一根石墨电极和导线连接在一起,接通电源。 |
现象和结论 | 现象 | 结论 |
灯泡发光 | 石墨具有导电性 |
25. 生成炭黑实验
| 操作 | 点燃一根蜡烛,将冷碟子放在火焰上方 |
现象和结论 | 现象 | 结论 |
冷碟子底出现黑色固体 | 石蜡不完全燃烧有炭黑生成 |
26. 木炭吸附性实验
| 操作 | 向盛有红棕色的二氧化氮气体的集气瓶里投入几小块烘烤过的木炭 |
现象和结论 | 现象 | 结论 |
红棕色消失 | 木炭具有吸附性 | |
解释 | 木炭具有疏松多孔的结构 |
27. 实验室制取二氧化碳
| 原理 | CaCO3+2HCl=CaCl2+H2O+CO2↑ | |
装置要点 | 长颈漏斗下端要插到液面下 | ||
导管要插到集气瓶底部 | |||
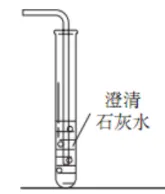
| 检验二氧化碳 | 操作 | 将产生的气体通入到澄清石灰水中 |
现象 | 澄清石灰水变浑浊 | ||
结论 | 该气体为二氧化碳 | ||
| 二氧化碳的验满 | 操作 | 将燃着的木条放在集气瓶口 |
现象 | 木条熄灭 | ||
结论 | 二氧化碳已经集满 |
28. 倾倒二氧化碳实验
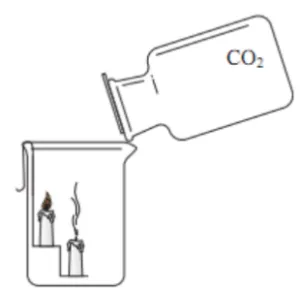
| 操作 | 向烧杯中倾倒二氧化碳气体(高低不同阶梯的上放两支燃着的蜡烛) |
现象和结论 | 现象 | 结论 |
蜡烛自下而上依次熄灭 | 1.二氧化碳密度大于空气 2.二氧化碳不可燃不助燃 | |
解释 | 二氧化碳密度大于空气,故可以像倒水一样,倾倒二氧化碳气体;由于二氧化碳密度大于空气,所以二氧化碳气体自下而上填充烧杯,二氧化碳气体不可燃不助燃,故蜡烛自下而上依次熄灭。 |
操作 | 向一个收集满二氧化碳气体的质地较软的塑料瓶中加入约1/3体积的水,立即旋紧瓶盖,振荡。 | |
现象和结论 | 现象 | 结论 |
软塑料瓶变瘪 | 二氧化碳能溶于水 | |
分析 | 部分二氧化碳溶于水使瓶内气体减少,气压变小,大气压强使瓶子变瘪。 |
| |||||
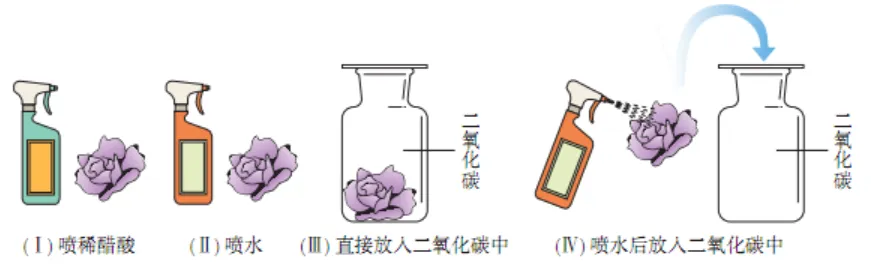
Ⅰ | Ⅱ | Ⅲ | Ⅳ | 烘干第四朵花 | |
现象 | 纸花由紫变红 | 纸花不变色 | 纸花不变色 | 纸花由紫变红 | 纸花由红变紫 |
分析 | 醋酸能使石蕊溶液变红 | 水不能使石蕊溶液变红 | 二氧化碳不能使石蕊溶液变红 | 二氧化碳与水反应生成碳酸,碳酸能使石蕊溶液变红 | 碳酸受热分解,生成二氧化碳和水。 |
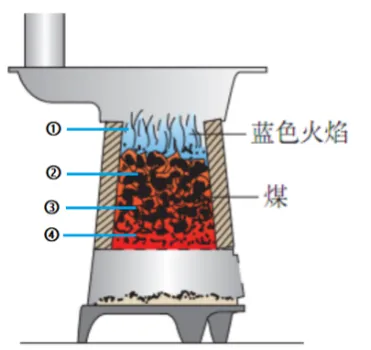
| ① | 2CO+O2点燃=======2CO2 |
② | CO2+C高温=======2CO | |
③ | 2C+O2点燃=======2CO | |
④ | C+O2点燃=======CO2 |
32.鸡蛋壳与醋酸反应的实验
| 操作 | 取一个小玻璃杯,放入洗净的碎鸡蛋壳,然后加入一些醋精(主要成分是醋酸),立即用蘸有澄清石灰水的玻璃片盖住。 |
现象 | 1.鸡蛋壳表面产生气泡 2.玻璃片上的澄清石灰水变浑浊 | |
结论 | 鸡蛋壳能与醋酸发生反应,生成二氧化碳气体。 |
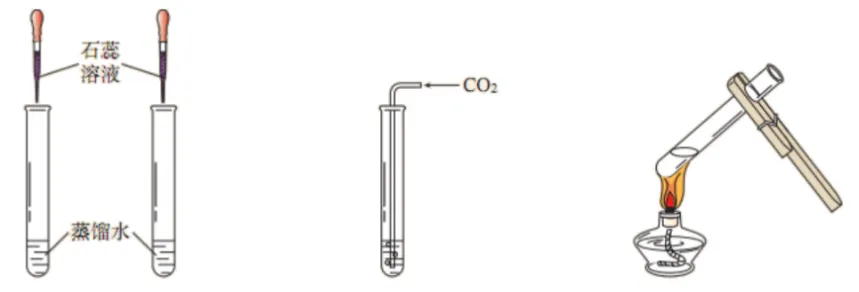
33.二氧化碳与水的反应
| |||
序号 | Ⅰ | Ⅱ | Ⅲ |
操作 | 向蒸馏水中滴入石蕊溶液 | 向试管中通入二氧化碳 | 将通入二氧化碳的试管加热 |
现象 | 溶液呈紫色 | 溶液由紫色变成红色 | 溶液由红色变成紫色 |
分析 | CO2+H2O=H2CO3 | H2CO3△=====H2O+CO2↑ |
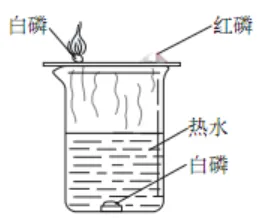
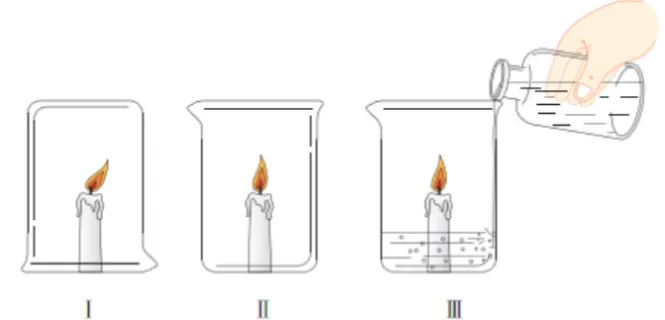
34.燃烧的条件探究
| 条件控制 | 现象及结论 |
对比铜片上白磷和红磷 | 现象 | 燃烧需要达到可燃物的着火点 |
白磷燃烧 | ||
红磷不燃烧 | ||
对比铜片上白磷和水中的白磷 | 现象 | 燃烧需要与氧气(或空气)接触 |
铜片上白磷燃烧 | ||
水中的白磷不燃烧 | ||
| 现象 | 结论 |
水中的白磷燃烧 | 燃烧需要与氧气(或空气)接触 |
| |||
序号 | Ⅰ | Ⅱ | Ⅲ |
现象 | 火焰熄灭 | 正常燃烧 | 溶液由红色变成紫色 |
分析 | 烧杯隔绝空气 | 同时具备燃烧的3个条件 | 生成的CO2不可燃不助燃,密度比空气大,可隔绝空气 |
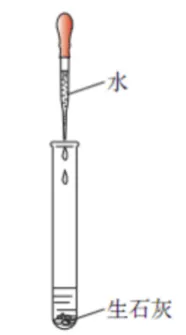
36. 生石灰与水反应
| 操作 | 在一支试管中加入一小匙干燥的生石灰,再加入2mL水,观察现象,并用手轻轻触碰试管外壁。 |
现象 | 1.白色固体膨胀最终变成白色粉末 2.试管外部烫手 | |
化学方程式 | CaO+H2O=Ca(OH)2 |
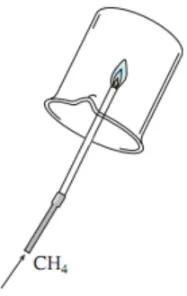
37. 甲烷的燃烧
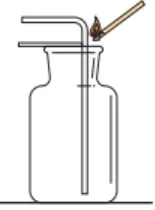
| 操作 | 1.点燃甲烷,在火焰上方罩一个冷而干燥的烧杯 2.迅速将烧杯倒过来,向烧杯中注入少量的澄清石灰水,振荡。 |
现象 | 1.火焰为明亮的蓝色 2.烧杯内壁出现水珠 3.澄清石灰水变浑浊 | |
化学方程式 | CH4+2O2点燃=======CO2+2H2O CO2+Ca(OH)2=CaCO3↓+H2O | |
结论 | 1.甲烷具有可燃性 2.甲烷由碳氢元素组成 |
| 操作 | 1.比较黄铜和铜片、硬铝片和铝片的光泽和颜色 2.将它们相互刻画,比较它们的硬度 | ||
性质比较 | 现象 | |||
黄铜 | 铜 | 硬铝 | 铝 | |
光泽和颜色 | 有光泽,黄色 | 有光泽,紫红 | 有光泽,银白色 | 有光泽,银白色 |
硬度 | 黄铜比铜硬 | 硬铝比铝硬 | ||
结论 | 合金与组分金属物理性质有差异,一般合金的硬度大于其组分金属的硬度。 |
金属之最:
①铝:地壳中含量最高的金属元素;
②钙:人体中含量最多的金属元素;
③铁:目前年产量最多的金属(铁>铝>铜);
④银:导电、导热性最好的金属(银>铜>铝);
⑤铬:硬度最高的金属;⑥钨:熔点最高的金属;
⑦汞:熔点最低的金属;⑧锇:密度最大的金属;
⑨锂:密度最小的金属。
39.金属与盐酸、稀硫酸的反应
| ||||
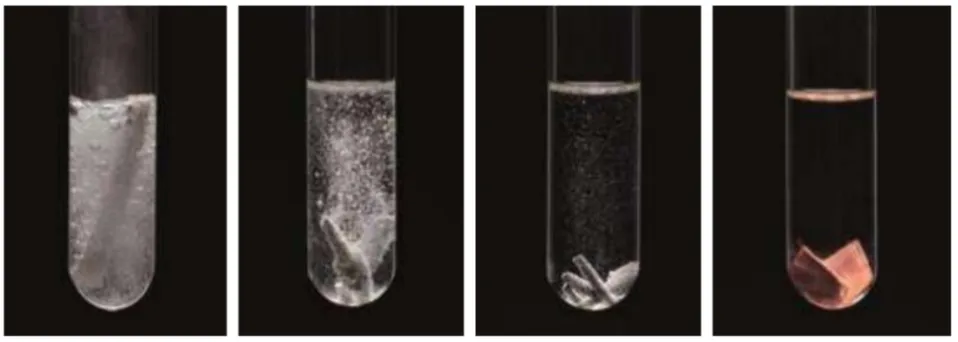
金属 | 现象 | 反应的化学方程式 | ||
稀盐酸 | 稀硫酸 | 稀盐酸 | 稀硫酸 | |
镁 | 剧烈反应,产生大量气泡 | 剧烈反应,产生大量气泡 | Mg+2HCl=MgCl2+H2↑ | Mg+H2SO4=MgSO4+H2↑ |
锌 | 反应较剧烈,有较多气泡产生 | 反应较剧烈,有较多气泡产生 | Zn+2HCl=ZnCl2+H2↑ | Zn+H2SO4=ZnSO4+H2↑ |
铁 | 反应且有少量气泡产生 | 反应且有少量气泡产生 | Fe+2HCl=FeCl2+H2↑ | Fe+H2SO4=FeSO4+H2↑ |
铜 | 无变化 | 无变化 |
|
|
40. 金属活动性顺序探究
| 操作 | 将一根用砂纸打磨过的铝丝浸入硫酸铜溶液中,过一会取出观察现象 |
现象 | 铝丝上附着红色固体,溶液颜色变浅。 | |
原理 | 2Al+3CuSO4=Al2(SO4)3+3Cu | |
结论 | 铝的金属活动性比铜强 | |
| 操作 | 将一根洁净的铜丝浸入硝酸银溶液中,过一会取出观察现象 |
现象 | 铜丝的表面附着黑色的固体,溶液由无色慢慢变成蓝色 | |
原理 | Cu+2AgNO3=Cu(NO3)2+2Ag | |
结论 | 铜的金属活动性比银强 |
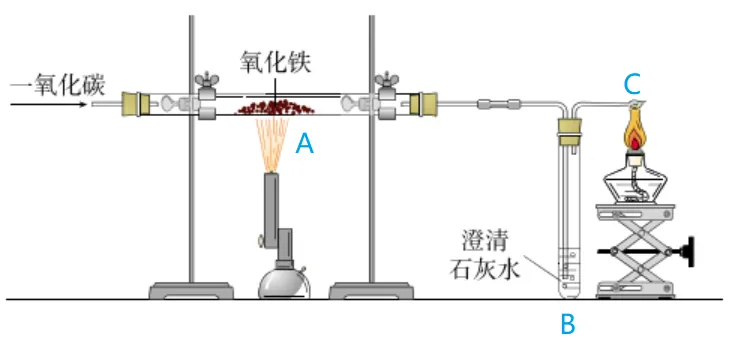
41. 一氧化碳还原氧化铁
| |||
序号 | A | B | C |
现象 | 红棕色固体逐渐变黑 | 澄清石灰水变浑浊 | 气体燃烧,火焰为蓝色 |
原理 | 3CO+Fe2O3高温=======2Fe+3CO2 | CO2+Ca(OH)2=CaCO3↓+H2O | 2CO+O2点燃=======2CO2 |
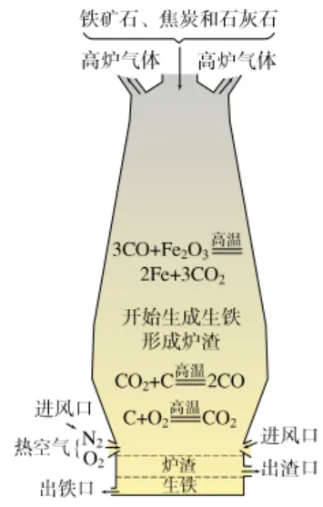
42. 高炉炼铁
| 原料 | 铁矿石 | 氧化铁或四氧化三铁 |
焦炭 | 烧提供热量、产生还原剂一氧化碳。 | ||
石灰石 | 可将矿石中二氧化硅转变为炉渣 | ||
空气 | 提供氧气 | ||
原理 | 在高温下,一氧化碳把铁从铁矿石中还原出来 | ||
设备 | 高炉 | 出铁口低于出渣口:铁水密度大于滤渣密度,有利于炉渣的排出。 |
43. 铁制品锈蚀条件探究
实验装置 |
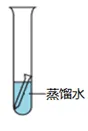
|
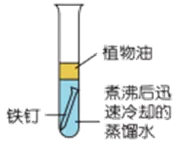
|
|
现象 | 铁钉生锈 | 铁钉不生锈 | 铁钉不生锈 |
现象分析 | 铁钉同时和氧气(或空气)、水接触 | 铁钉只和水接触 | 铁钉只和氧气(或空气)接触 |
结论 | 铁钉生锈的条件:铁和氧气(或空气)、水接触同时接触 |
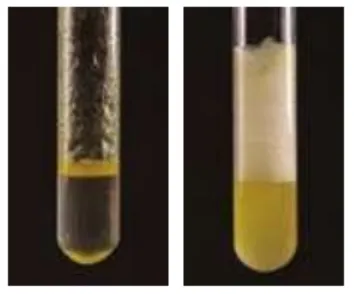
44. 碘和高锰酸钾的溶解性比较
| ||
溶质 | 溶剂 | 现象 |
碘 | 水 | 碘几乎不溶于水 |
碘 | 汽油 | 碘溶于汽油,溶液呈棕色 |
高锰酸钾 | 水 | 高锰酸钾溶于水,溶液呈紫红色 |
高锰酸钾 | 汽油 | 高锰酸钾不溶于汽油 |
结论 | 1.同一物质在不同的溶剂中溶解性不同; 2.不同物质在同一溶剂中的溶解性也不同。 |
45. 乳浊液的形成和乳化现象
| 操作 | 用力振荡有水和植物油的试管 |
现象 | 不加洗涤剂 | 加入洗涤剂 |
静置后依然分层 | 静置后不再分层 | |
解释 | 加入洗涤剂能使植物油在水中分散成无数细小的液滴,而不聚成油珠,从而使油和水不再分成,所形成的乳浊液稳定性增强,这种现象称为乳化。 |
| 操作 | 把少量泥土放入到水中,搅拌,静置一段时间。 |
现象 | 悬浊液分层 | |
解释 | 难溶的固体小颗粒,由于重力作用,小颗粒会沉降下来。 |
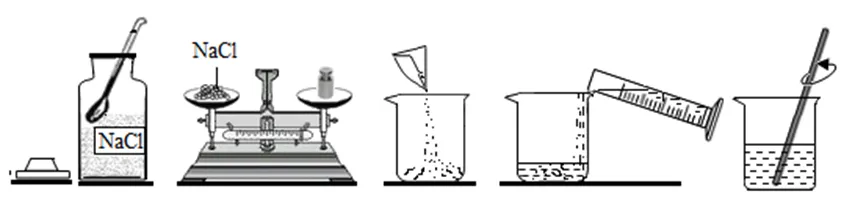
47.一定质量分数的氯化钠溶液的配制(以配制50g质量分数为6%的氯化钠溶液为例)
| |
计算 | 氯化钠质量=50g×6%=3g;水的质量=50g-3g=47g |
称量 | 托盘天平称量所需的氯化钠,放入烧杯中。 |
量取 | 用量筒量取所需水的体积(47g÷1g/mL=47mL),倒入盛有氯化钠的烧杯中。 |
溶解 | 用玻璃棒搅拌,使氯化钠溶解。 |
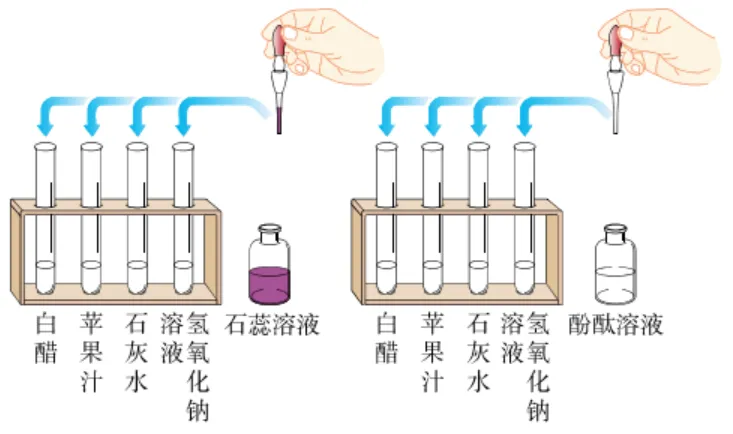
48.向溶液中加入酸碱指示剂
| ||
加入紫色石蕊溶液后的颜色变化 | 加入无色酚酞溶液后的颜色变化 | |
白醋 | 变红色 | 不变色 |
苹果汁 | 变红色 | 不变色 |
石灰水 | 变蓝色 | 变红色 |
氢氧化钠溶液 | 变蓝色 | 变红色 |
①酸碱指示剂遇酸性或碱性溶液时,变色的是指示剂;
②酸的溶液一定显酸性,显酸性的溶液不一定是酸;如硫酸铜溶液显酸性;
碱的溶液一定显碱性,显碱性的溶液不一定是碱;如碳酸钠溶液显碱性;
③酸碱指示剂只能对酸、碱溶液作出定性判断,而不能对酸碱性的强弱程度作出判断;
④难溶性的碱,如Mg(OH)2不能使指示剂变色。
49. 浓硫酸的腐蚀性
| 实验 | 放置一会儿后的现象 |
用玻璃棒蘸浓硫酸在纸上写字 | 纸上显出黑色字迹 | |
用小木棍蘸少量浓硫酸 | 蘸有硫酸的部位变黑 | |
将浓硫酸滴到一小块布上 | 蘸有硫酸的部位变黑甚至形成洞 |
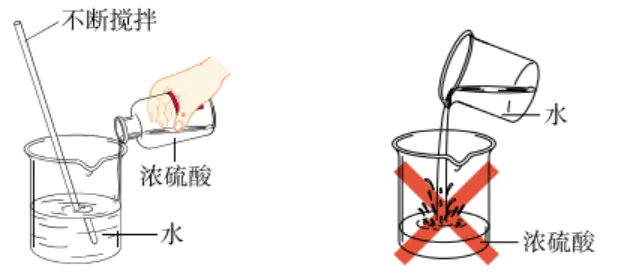
50. 浓硫酸的稀释
| 将浓硫酸沿烧杯壁慢慢地注入到盛有水的烧杯里,用玻璃棒搅拌。切不可将水倒入浓硫酸! |
51. 自制“叶脉书签”
| 操作 | 将外形完整、大小合适、具有网状叶脉的树叶,放在10%的氢氧化钠溶液中煮沸。当叶肉呈现黄色后取出树叶,用水将树叶上的碱液洗净。用牙刷轻轻刷去叶肉,将剩下的叶脉放在水中清洗,稍稍晾干后,夹在书中压平。 |
现象 | 一段时间后得到完整的“叶脉书签” | |
解释 | 氢氧化钠溶液有腐蚀性,将质地较软的叶肉腐蚀。 |
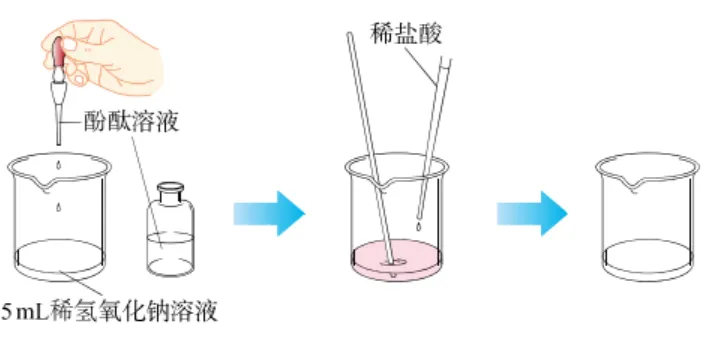
| |
现象 | 滴有酚酞的氢氧化钠溶液由红色变为无色 |
原理 | HCl+NaOH=NaCl+H2O |
实质 | H++OH-=H2O |
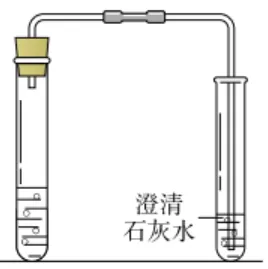
| 操作 | 向盛有0.5g碳酸钠的试管里加入2mL的盐酸,迅速将带导管的橡皮塞塞紧试管口,并将导管的另一端插入盛有澄清石灰水的试管中。 |
现象 | 1.碳酸钠粉末溶解,产生气泡; 2.澄清石灰水变浑浊。 | |
解释 | Na2CO3+2HCl=2NaCl+H2O+CO2↑ CO2+Ca(OH)2=CaCO3↓+H2O |