一、物质由微观粒子构成
1.构成物质的微粒:分子、原子、离子。
分子:由分子构成的物质,分子是保持其化学性质的最小粒子;
原子:原子是化学变化中的最小粒子;
离子:带电荷的原子或原子团。
2.分子的基本性质:
分子的性质 | 举例 |
分子的质量和体积都很小 | 1滴水中大约有1.67×1021个水分子 |
分子在不断地运动; 温度越高,分子运动速率越快 | 酒香不怕巷子深; 湿衣服在太阳下比在阴凉处干得快 |
分子之间有间隔; 加压或降温能使分子间的间隔变小 | 热胀冷缩;给自行车胎打气; 加压可以将6000L的氧气装入40L的氧气瓶中 |
同种分子化学性质相同; 不同种分子化学性质不同 | 水受热变为水蒸气,水的化学性质不变; H2O和 H2O2的分子构成不同,化学性质不同 |
气体分子间隔较大,而固体和液体分子间的间隔较小。
二、分子可以分为原子
1.分子由原子构成。
物质的名称和符号 | 氧气(O2) | 氢气(H2) | 二氧化碳(CO2) | 氨气(NH3) |
构成该物质的分子 | 氧分子 | 氢分子 | 二氧化碳分子 | 氨分子 |
物质的分子模型 |
|
|
|
|
构成该分子的原子 | 氧原子 | 氢原子 | 碳原子、氧原子 | 氮原子、氢原子 |
分子是否由同种原子构成 | 是 | 是 | 否 | 否 |
小结 | 分子可以由同种原子构成,也可以由不同种原子构成 |
2.化学变化的微观实质:在化学变化中,分子可以分成原子,原子又可以结合成新的分子。
3.从宏观和微观角度认识物质的组成及变化实质
物质 | 宏观 | 微观 |
纯净物 | 只含有一种物质 | 物质中含有一种分子 |
混合物 | 含有两种或两种以上物质 | 物质中含有多种分子 |
物理变化 | 没有新物质生成的变化 | 分子不改变,只是分子间隔在改变 |
化学变化 | 有新物质生成的变化 | 分子改变,分子破裂成原子,原子重新组合成新分子 |
三、原子的构成
1. 原子(不)
2. 核电荷数(原子核所带的正电荷数)=质子数=核外电子数=原子序数。
3.不是所有原子核内都有中子;
原子中,质子数=核外电子数(原子不显电性的原因);
质子数不一定等于中子数
四、原子核外电子的排布
1.规律
(1)电子层由内而外总共分为7层,电子分层运动,电子优先排在离核较近的电子层,依次向外排布。
(2)离核近的电子能量较低,离核越远,电子的能量越高。
(3)第1层最多容纳2个电子,第2层最多容纳8个电子。最外层电子数不超过8个(只有1层的,电子不超过2个)
(3)原子结构示意图
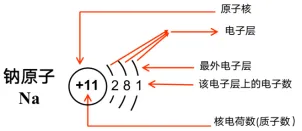
(4)原子结构排布规律
①每一横排,电子层数相同,最外层电子数从左到右依次递增;
②除稀有气体外,每一纵列,最外层电子数相同,电子层数从上到下依次递增。
2.原子结构与性质的关系
(1)相对稳定结构是指最外层为8个电子(氦为2个电子)的粒子的结构。
(2)原子的最外层电子数与其化学性质的关系
原子种类 | 最外层电子数 | 是否相对稳定 | 得失电子的倾向 |
稀有气体原子 | 8个(He为2个) | 是 | 难得失电子 |
非金属原子 | 一般多于4个 | 否 | 易得到电子 |
金属原子 | 一般少于4个 | 否 | 易失去电子 |
(3)金属、非金属的化学性质与其原子的核外电子排布,特别是最外层电子的数目有关。
五、离子
1.概念:带电荷的原子。原子通过得失电子形成离子。
2.分类:带正电的原子叫做阳离子,带负电荷的原子叫做阴离子。
3.离子是构成物质的微观粒子。如氯化钠是由钠离子和氯离子构成。
4.离子符号的书写:在元素符号的右上角标明离子所带的电荷数和电性。电荷数在前(电荷数为1时,1省略不写),电性在后(“+”表示正电,“—”表示负电)。
5.离子符号表示的意义
Mg2+:表示镁离子,其中“2+”表示1个镁离子带2个单位的正电荷;离子符号前面加了数字,只能表示多少个什么离子,如2Mg2+表示2个镁离子。
6.离子和原子的联系与区别
原子 | 阳离子 | 阴离子 | |
结构 | 质子数=核外电子数 | 质子数>核外电子数 | 质子数<核外电子数 |
电性 | 不带电 | 带正电 | 带负电 |
联系 | 原子得到电子变为阴离子,失去电子变为阳离子 |
【失为正,得为负】
六、相对原子质量
1.概念:以一种碳原子质量的1/12为标准,其他原子的质量与它相比,得到相对原子质量(符号为Ar)。
2.两种原子的实际质量之比等于它们的相对原子质量之比。
3.中国科学院院士张青莲教授为相对原子质量的测定作出了卓越贡献。
【易错】(1)相对原子质量( Ar)是一个“比值”,单位为“1”,省略不写。
(2)相对原子质量不等于原子的实际质量,它是个比值;原子的实际质量越大,其相对原子质量就越大。
(3)近似计算:相对原子质量≈质子数+中子数。
七、元素
1.概念:元素是质子数(即核电荷数)相同的一类原子的总称。
2.元素概念理解
(1)不同元素的根本区别是质子数不同;质子数决定元素的种类。
(2)质子数相同,中子数不同的一类原子属于同种元素。
(3)原子得失电子后形成离子,元素种类不变。
(4)元素是一类原子的“总称”,是宏观概念,因此元素只讲种类,不讲个数。
3.地壳中的元素含量前四位:氧O、硅Si、铝Al、铁Fe;地壳中含量最多的金属元素是铝Al。
海水中含量前4位的元素:氧、氢、氯、钠
生物细胞中含量前4位的元素:氧、碳、氢、氮
4.当发生化学变化时,原子的种类不变,元素也不会改变。
5.物质的构成:
由分子构成:
常见气体:O2、H2、N2、CO2、CO、O3、CH4...
部分液体:H2O、H2O2、C2H5OH...
部分固体:P2O5、HgO、Fe3O4
由原子构成:
金属:Hg、Fe、Cu、Al、Zn...
稀有气体:He、Ne、Ar...
部分非金属固体:C、S、P、Si...
由离子构成:NaCl、CuSO4...
八、元素符号
1.元素符号的书写
(1)由一个字母表示的元素符号必须大写。
(2)由两个字母表示的元素符号,第一个字母必须大写,第二个字母必须小写。
2.元素符号表示的意义
(1)宏观:表示一种元素。
(2)微观:表示该元素的一个原子。
例:H:表示氢元素,一个氢原子
(3)特殊:由原子构成的物质还表示物质。(金属、稀有气体、部分固态非金属)
例:Fe:表示铁元素,一个铁原子,铁这种物质。
(4)数字+元素符号,只表示微观意义:几个原子。
例:5H:表示5个氢原子;3Fe:3个铁原子。
九、元素周期表
1.化学史:俄国科学家门捷列夫发现了元素周期律并编制出元素周期表。
2.编排依据:根据元素的原子结构和性质,把元素科学有序地排列起来。
3.元素周期表按元素原子核电荷数递增的顺序给元素编号。
原子序数=质子数=核电荷数=核外电子数
4.横行(周期):元素周期表有7个横行,每一横行元素的电子层数相同,最外层电子数从左到右由1依次增加至8,元素种类从金属元素→非金属元素→稀有气体元素(第一周期除外)。
5.纵列(族):同一纵列元素的最外层电子数相同,电子层数依次增加,共有18个纵列,16个族(8、9、10三个纵列共同组成1个族)。
6.元素周期表每一格包含的信息:










