2026年04月10日
上海初中化学中考趋势 | 2026年04月10日
今日主题
网购“活氧洗衣颗粒”有效成分的定量探究与综合计算 · 小明网购了一款“活氧洗衣颗粒”,说明书称有效成分为过碳酸钠(2Na₂CO₃·3H₂O₂),遇热水分解为碳酸钠和过氧化氢,能强效去污。为测定纯度,小明取20.0g样品于烧杯中,加入50.0g热水和0.5g二氧化锰,待气泡不再产生时,测得烧杯内混合物总质量为68.1g。随后向残留溶液中加入足量氯化钙溶液,过滤、洗涤、干燥后得到10.0g白色沉淀。(假设杂质易溶于水且不参与反应)。
核心知识点
• 信息给予题的化学方程式书写
• 质量守恒定律在定量计算中的应用
• 盐的化学性质与沉淀反应
教育价值
通过网购洗衣产品的真实消费情境,引导学生利用化学知识对商品宣传进行定量验证,培养“宏观辨识与微观探析”及“证据推理”的核心素养,提升解决实际生活问题的综合计算能力。
情景化题型精讲
题目配图
图1:science 化学 20260410 1
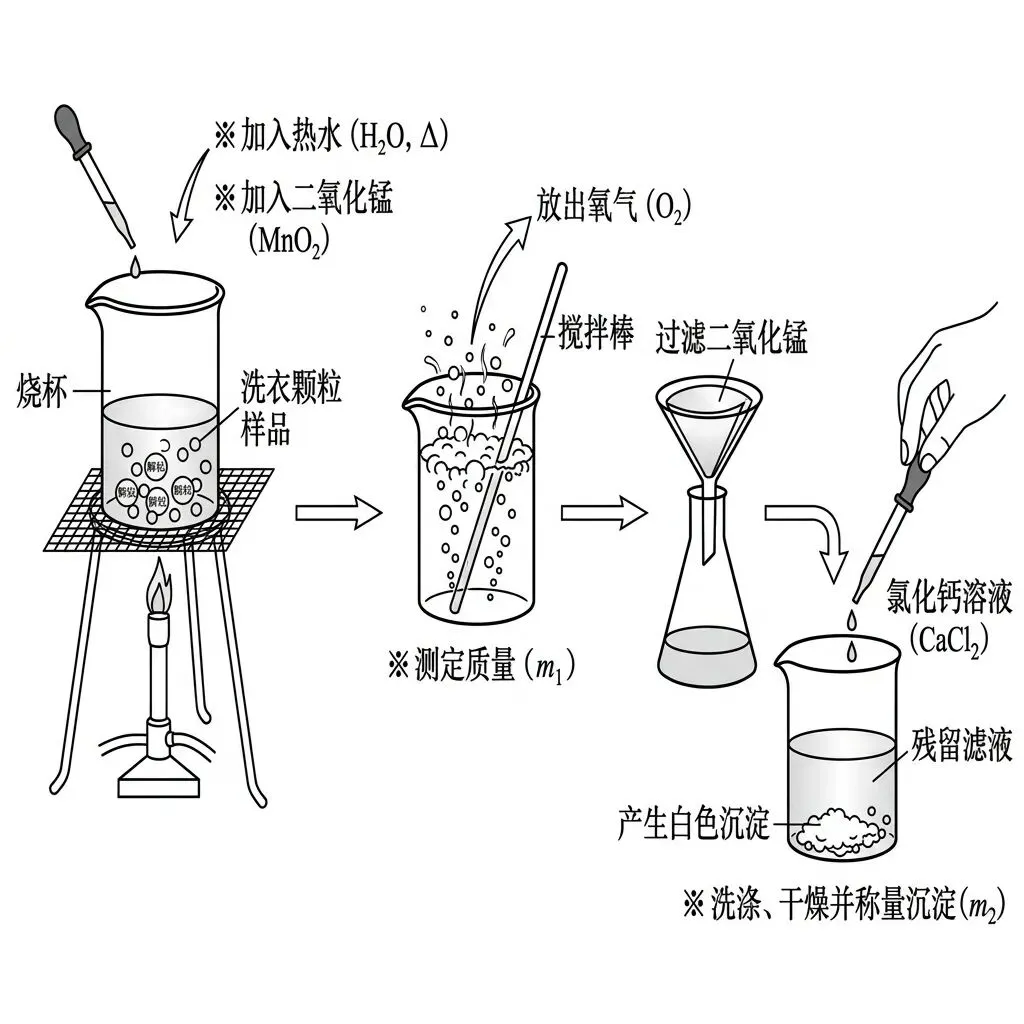
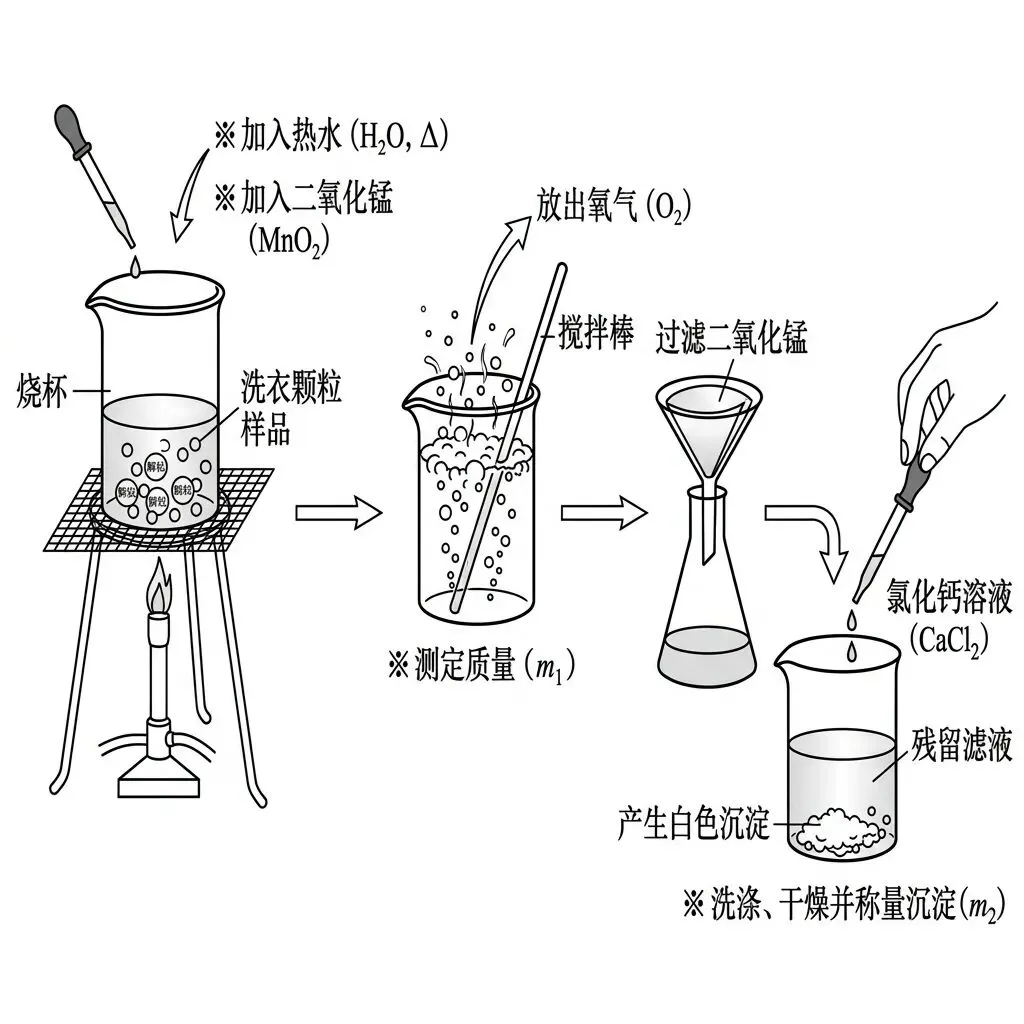
【实验探究与综合计算题】(较难程度,总分14分)
随着生活品质的提升,一款名为“活氧洗衣颗粒”的新型洗涤剂在网购平台上热销。该产品宣称具有强效去污、杀菌漂白双重功效。小明查阅资料得知,其有效成分为过碳酸钠(化学式为 2Na₂CO₃ · 3H₂O₂),外观为白色结晶颗粒。过碳酸钠在常温下较稳定,但遇热水会迅速分解为碳酸钠和过氧化氢。生成的碳酸钠能使水呈碱性,有助于去除油污;而过氧化氢则进一步分解产生氧气,利用“活氧”的强氧化性破坏色素和细菌结构。
为测定该款洗衣颗粒中过碳酸钠的纯度,小明设计了如下定量探究实验(假设样品中的杂质易溶于水,且不与水及其他试剂发生反应):
【步骤一】将 20.0g “活氧洗衣颗粒”样品放入烧杯中。
【步骤二】向烧杯中加入 50.0g 热水,搅拌使其充分溶解并反应。为加快反应速率,小明又加入了 0.5g 二氧化锰粉末。待烧杯内气泡不再产生时,测得烧杯内混合物的总质量为 68.1g。
【步骤三】将烧杯中的混合物过滤,回收二氧化锰。向所得的残留滤液中滴加足量的氯化钙溶液,直至不再产生沉淀。
【步骤四】将步骤三中产生的沉淀再次过滤,经过蒸馏水洗涤、干燥后,准确称量得到 10.0g 白色沉淀。
实验测得的部分数据整理见表1(实验流程见图1)。
| 物质/状态 | 质量/g |
|---|---|
| 洗衣颗粒样品 | 20.0 |
| 加入的热水 | 50.0 |
| 加入的二氧化锰 | 0.5 |
| 反应后烧杯内混合物总质量 | 68.1 |
| 最终干燥后的白色沉淀 | 10.0 |
(1)根据质量守恒定律,步骤二中完全反应后生成的氧气质量为_____g;请写出步骤二中产生氧气的化学方程式:________________________。(4分)
参考答案:
2. 4;2H₂O₂ ₂ 2H₂O + O₂ ↑
解析:
解析:根据质量守恒定律,反应前后物质的总质量不变。反应前烧杯内物质总质量为 20.0g + 50.0g + 0.5g = 70.5g,反应后混合物总质量为 68.1g,减少的质量即为逸出的氧气质量,即 m(O₂) = 70.5g - 68.1g = 2.4g。步骤二中产生氧气的反应是过氧化氢在二氧化锰催化下分解生成水和氧气,化学方程式为 2H₂O₂ ₂ 2H₂O + O₂ ↑。
(2)请利用步骤二中生成的氧气质量,计算该“活氧洗衣颗粒”中过碳酸钠的质量分数。(写出完整的计算过程)(5分)
参考答案:
78.5%
解析:
解析:
解:设生成 2.4g 氧气需要过氧化氢的质量为 x。
2H₂O₂ ₂ 2H₂O + O₂ ↑
68 32
x 2.4g
(68)/(32) = (x)/(2.4g)
解得 x = 5.1g
在过碳酸钠(2Na₂CO₃ · 3H₂O₂)中,整体的相对分子质量为 2 × 106 + 3 × 34 = 314。
其中所含过氧化氢部分的相对质量为 3 × 34 = 102。
设样品中纯过碳酸钠的质量为 y。
y × (102)/(314) = 5.1g
解得 y = 15.7g
该“活氧洗衣颗粒”中过碳酸钠的质量分数为:(15.7g)/(20.0g) × 100% = 78.5%。
答:该“活氧洗衣颗粒”中过碳酸钠的质量分数为 78.5%。
(3)小红认为,步骤四中洗涤白色沉淀的操作非常关键。如果不进行洗涤直接干燥称量,会导致依据沉淀质量计算出的过碳酸钠纯度______(填“偏大”、“偏小”或“不变”)。另外,产品说明书上强调“建议使用 40℃-60℃ 的温热水,切勿使用沸水”,请结合情境信息与化学反应原理,推测不建议使用沸水的原因。(5分,答案不唯一,言之有理即可)
参考答案:
偏大;若使用沸水,过氧化氢会因为温度过高而剧烈分解,产生的氧气迅速逸出到空气中,无法充分与衣物上的污渍发生氧化漂白作用,导致“活氧”利用率降低,去污效果变差。(评分要点:填空2分;原因表述需体现“温度过高导致分解过快”得1分,“氧气迅速逸出”得1分,“未能充分作用于衣物/利用率降低”得1分)
解析:
解析:步骤三中向残留滤液中加入氯化钙,发生反应 Na₂CO₃ + CaCl₂ → CaCO₃ ↓ + 2NaCl。过滤后得到的碳酸钙沉淀表面会附着可溶性的氯化钠以及过量的氯化钙等杂质。如果不洗涤直接干燥,称得的沉淀质量会偏大。根据沉淀质量反推碳酸钠的质量就会偏大,进而导致计算出的过碳酸钠纯度偏大。关于水温,温度越高化学反应速率越快。沸水会导致生成的 H₂O₂ 瞬间剧烈分解,大量氧气直接作为气泡逸散到空气中,没有足够的时间与衣物纤维中的污垢大分子发生氧化反应,从而降低了洗涤剂的有效性。
知识点地图
质量守恒定律(宏观测定) → 化学方程式的书写与计算(定量转化) → 物质组成的质量比计算 → 盐的化学性质及沉淀反应 → 实验误差分析与反应速率控制(联系实际)
本题知识点之间的逻辑关联,帮助学生建立知识网络
思路拓展
1. 拓展问题1:请尝试利用步骤四中产生的 10.0g 白色沉淀,重新计算一遍过碳酸钠的纯度,验证两次计算结果是否一致。(引导学生体会不同化学量之间内在的守恒关系)
2. 拓展问题2:如果将步骤二中的二氧化锰替换为新鲜的猪肝研磨液(含有过氧化氢酶),反应速率会发生什么变化?这说明了酶的什么特性?
拓展问题不要求作答,目的是打开思路,培养发散思维
学习建议
1. 针对“信息给予题”,建议养成“圈画-转化-配平”的三步解题习惯。行动指导:在阅读说明书或题干时,用笔圈出反应物(如2Na₂CO₃·3H₂O₂、热水)、催化剂(MnO₂)和生成物。准备一个错题本,专门收集此类陌生方程式,练习将文字信息转化为化学方程式,例如不仅要写出 2Na₂CO₃·3H₂O₂ = 2Na₂CO₃ + 3H₂O₂,还要紧接着写出H₂O₂在MnO₂催化下的分解反应 2H₂O₂ = 2H₂O + O₂↑,并注意检查反应条件和气体符号。
2. 攻克“质量守恒定律”在多步混合反应中的计算难点,建议采用“画流程图”结合“差量法”进行分析。行动指导:在解答定量探究题时,先画出物质转化流程图,标明每一步加入和剩余物质的质量。计算气体质量时,严格写出质量差的表达式,例如本题中计算氧气质量必须写明 Δm = 20.0g + 50.0g + 0.5g - 68.1g = 2.4g,明确这2.4g即为m(O₂),切忌死记硬背公式,要深刻理解质量减少的本质原因是气体逸出。
3. 针对“盐的化学性质与沉淀反应”,建议通过“逆向推导法”来验证有效成分的含量。行动指导:在复习碳酸钠的性质时,不要只背诵能与钙盐反应,要结合实际数据进行推算。例如,利用题干中生成的10.0g白色沉淀,写出反应 Na₂CO₃ + CaCl₂ = CaCO₃↓ + 2NaCl,通过m(CaCO₃)逆向计算出样品中Na₂CO₃的质量,再将其与通过m(O₂)计算出的Na₂CO₃质量进行对比,以此来检验实验数据的合理性或判断样品是否变质。
4. 培养科学探究思维,建议在日常练习中增加“误差分析”环节,将理论计算与实际操作相联系。行动指导:做完综合计算题后,主动问自己两个“如果”。例如针对本情景提问:“如果加入的CaCl₂溶液不足,会导致测得的纯度偏大还是偏小?”或“如果反应后没有洗涤、干燥沉淀直接称量,对m(CaCO₃)有什么影响?”。通过这种自我提问,将纸面上的化学反应与真实的实验操作细节建立联系,提升解决实际问题的能力。
中考趋势分析
近期上海初中化学中考呈现以下趋势:
• 1. 题目形式的变化:由单一的计算题向'实验探究+综合计算'的复合题型转变。此类'活氧洗衣颗粒'的定量分析通常作为试卷的压轴大题出现,将气体的质量差量法计算与沉淀法计算结合,选择题和填空题中纯计算的比例下降,而包含多步反应和数据处理的综合实验计算题分值比重和出现频率显著上升。
• 2. 知识考查的深度和广度:考查范围从单一反应拓展到多步连续反应。题目要求学生不仅能处理过氧化氢分解产生氧气的反应(2H₂O₂ = 2H₂O + O₂↑),还要处理碳酸钠与氯化钙生成沉淀的反应(Na₂CO₃ + CaCl₂ = CaCO₃↓ + 2NaCl)。深度上要求学生理解复合盐(2Na₂CO₃·3H₂O₂)的拆解,并能通过质量守恒定律求出m(O₂) = 20.0g + 50.0g + 0.5g - 68.1g = 2.4g,进而结合m(CaCO₃) = 10.0g进行纯度等综合计算。
• 3. 情景化、应用性题目的特点:命题素材更加贴近生活实际,如'网购活氧洗衣颗粒'。这种真实情境打破了传统纯物质计算的枯燥感,要求学生在复杂的实际背景(如含有易溶于水的杂质、需要加入催化剂MnO₂等)中剥离出核心的化学反应模型,体现了化学知识在解决生活真实问题中的应用价值。
• 4. 对学生能力要求的变化:对数据处理能力和实验评价能力的要求大幅提高。学生需要具备敏锐的数据提取能力,例如利用反应前后的总质量差计算气体质量;同时,题目中'过滤、洗涤、干燥'等操作细节,考查了学生对定量实验误差分析的逻辑推理能力,要求学生能判断操作不当(如沉淀未洗涤或未完全干燥)对最终测定结果的影响。
• 5. 备考建议和重点:建议在复习中强化'差量法'和'沉淀法'的综合训练,熟练掌握质量守恒定律的应用。重点训练从复杂信息中提取有效数据的能力,规范化学方程式的书写和计算步骤。同时,要夯实基础实验操作(如过滤、洗涤、干燥)的规范性与误差分析,面对陌生化学式(如2Na₂CO₃·3H₂O₂)时要学会将其转化为熟悉的物质(Na₂CO₃和H₂O₂)进行分步计算。
实际应用
评估市售洗涤剂的有效成分含量、指导家庭安全合理使用活氧漂白剂、辨别商品标签的真实性。
每日一题,助力中考
科学备考,稳步提升
更新时间: 2026-04-10 08:00:25
内容说明: 本栏目专注上海初中化学中考趋势分析,每日精选情景化题型,帮助学生掌握核心知识点和解题方法。






