
无明显现象反应的中考命题特点
一些化学反应无明显现象,在反应过程中不发光、不变色、无沉淀和无气体生成,从而不易判断是否发生了化学反应。例如:二氧化碳与水的反应、二氧化碳与氢氧化钠溶液的反应、稀盐酸(或稀硫酸)和氢氧化钠溶液的反应等均无明显现象。如何证明这些物质之间确实发了化学反应呢?此类问题是历年来各地中考的一个热点探究题,考查学生的实验设计和信息迁移能力。
无明显现象反应的中考命题具有以下特点:
情境化设计:常以生活、生产或科技场景为背景,如二氧化碳与氢氧化钠溶液反应在“碳中和”情境中,或酸碱中和反应在医药、环保等领域的应用,考查学生将化学知识与实际情境结合的能力。
注重实验探究:重点考查学生设计实验证明无明显现象反应发生的能力,如通过指示剂变色、压强变化、温度变化、生成物检验等方法,要求学生分析实验原理、设计实验方案并预测现象。
强调科学思维:要求学生运用逻辑推理、归纳总结等科学思维方法,从实验现象中得出结论,或对实验方案的合理性进行评价,如判断实验是否严谨、是否存在干扰因素等。
融合跨学科知识:部分题目会结合物理(如压强、温度测量)、生物(如酸碱平衡在生物体内的作用)等学科知识,考查学生的跨学科综合应用能力。
关注核心素养:不仅考查学生对化学知识的掌握,更注重考查科学探究能力、创新意识、社会责任感等核心素养,如通过实验探究培养学生严谨的科学态度和解决实际问题的能力。
这些特点体现了中考命题对化学学科核心素养的重视,旨在考查学生在真实情境中运用化学知识解决问题的能力。
教学突破
无明显现象的反应设计思路可以从两个角度入手,一是验证有新物质生成,二是验证反应物的减少或消失。同时可以通过温度、压强、pH、电导率等数据的变化将隐性现象转化为显性现象。
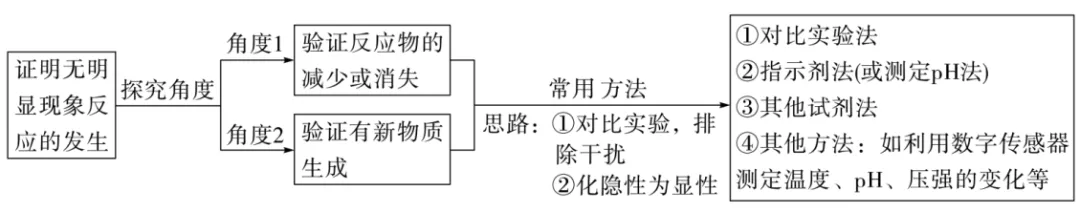
方法归纳:
(1)对比实验法:要注意控制变量,如二氧化碳与氢氧化钠溶液反应。
(2)指示剂法:适用于反应前后溶液酸碱性有变化的反应,如酸碱中和反应、CO2与水反应。
(3)其他试剂法:主要是验证产物的存在,能产生明显现象。
(4)其他方法:数字传感器定量分析(pH、离子浓度、导电率、温度、压强等)
压强差法:适用于有气体参与、反应前后有压强变化的反应,如二氧化碳和氢氧化钠溶液反应。
温差法:适用于反应前后温度有变化的反应,如酸碱中和反应。
CO₂与水反应:借助指示剂法验证是否有新物质生成。根据生成物具有而反应物没有的性质,选择合适的试剂设计实验证明新物质存在。

分别进行图示三个对比实验,观察到干燥的紫色石蕊纸花喷水或直接放入干燥CO₂中不变色,紫色石蕊纸花喷水后放入CO₂中变成红色。
结论:二氧化碳不能使干燥的紫色石蕊纸花变色,湿润的紫色石蕊纸花变红,可知有化学反应发生: CO₂ +H₂O=H₂CO3。
该实验设计原理利用了酸碱指示剂的显色反应,即紫色石蕊溶液遇酸性溶液显红色,二氧化碳与水发生反应生成碳酸,碳酸显酸性。证明二氧化碳与水发生反应。
二氧化碳与氢氧化钠溶液反应:
1.压强差法验证反应物的减少。根据反应前后气体变化引起压强变化,让压强变化显现出特征显现证明反应的发生。
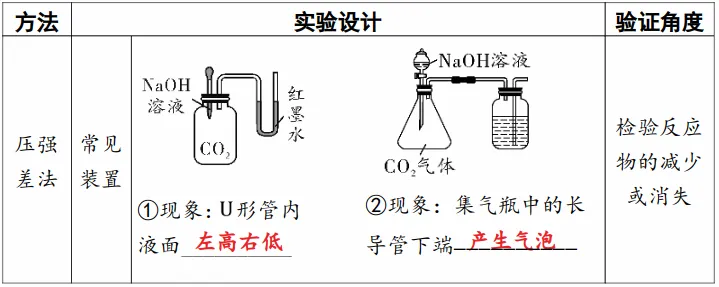
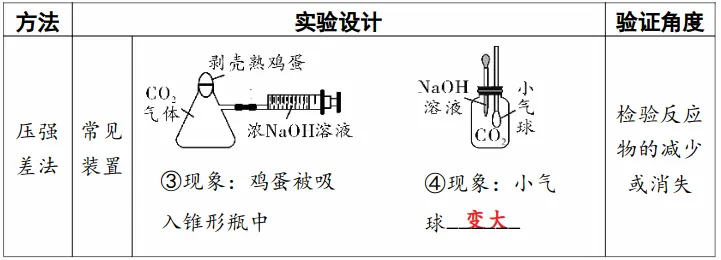
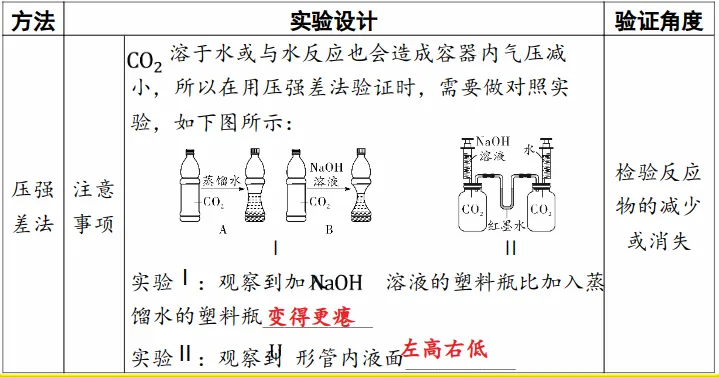
以上实验方案都是通过压强变化来证明二氧化碳的消失,来证明反应的发生。因为二氧化碳能溶于水,也会导致压强减小,所以必须做对比实验排除干扰。
2.其他试剂法验证验证有新物质生成。根据CO₂与NaOH溶液反应生成Na₂CO3和H₂O,即检验新物质Na₂CO3是否存在。

实验方案:取少量反应后的溶液于试管,加入过量的稀盐酸或氯化钙溶液等来证明有新物质生成,从而证明反应的发生
(1)加入盐酸有气泡冒出:2HCl + Na2CO3=2NaCl+ H2O+CO2↑
(2)加入石灰水有沉淀产生:Ca(OH)2 + Na2CO3 = CaCO3↓+2NaOH
(3)加入氯化钙有沉淀产生:Na2CO3 +CaCl2= CaCO3↓+2NaCl
(4)查阅资料:乙醇不与CO2、NaOH、Na2CO3 反应; 25℃时,氢氧化钠易溶于乙醇,碳酸钠微溶于乙醇 ,在乙醇中的溶解度如下表:

一些酸碱中和反应:(以稀盐酸和氢氧化钠的反应为例)
1.指示剂法、其他试剂法

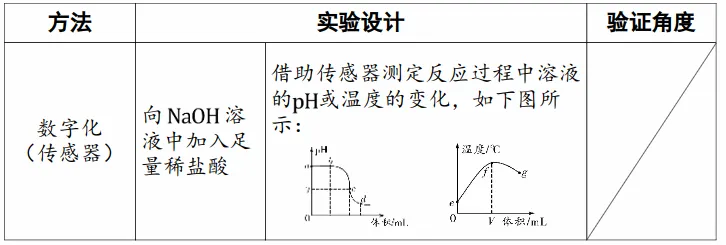
中和反应(以稀盐酸和氢氧化钠的反应为例)
实验1:NaOH溶液中加入足量稀盐酸,检验NaOH的消失
①滴加酸碱指示剂或测定溶液pH:判断溶液的酸碱性变化
②加入可溶性铜盐(或镁盐):观察是否有沉淀
实验2:稀盐酸中加入足量NaOH溶液,检验稀盐酸的消失
①加入活泼金属或碳酸盐:观察是否有沉淀
②加入难溶性碱或金属氧化物:观察固体是否溶解
例:化学实验小组的同学对中和反应进行探究。
【探究活动1】证明酸和碱能否发生反应。
【设计实验】⑴小明同学将稀盐酸和氢氧化钠溶液混合没有明显现象。
由此小明得出结论:稀盐酸和氢氧化钠溶液没有发生反应。经过讨论,同学一致认为小明的结论是错误的,原因是。
⑵小丽同学按图甲所示进行实验,证明了稀盐酸和氢氧化钠溶液之间发生了化学反应,她依据的实验现象是,其中发生反应的化学方程式为________________。
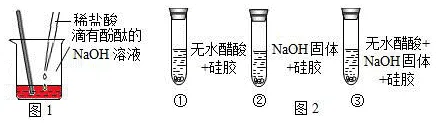
⑶小兵同学利用测定溶液的酸碱度来证明,向试管内pH=12的氢氧化钠溶液中滴加一定量的稀盐酸后,再测定混合液的pH,发现pH=9,于是得出结论:两者间发生了化学变化。你认为,小兵同学的实验(填“正确”或“错误”),理由是。
【探究活动2】能否通过证明有水生成来证明反应的发生?
【设计实验】小亮同学取用变色硅胶,无水醋酸和氢氧化钠固体进行如图乙所示的三个实验。
【查阅资料】①变色硅胶吸水后会由蓝色变为红色;②无水醋酸是一种酸,常温下为无色液体。
⑷实验①②的目的是。
实验中加入试剂后,要迅速塞紧橡胶塞的原因是。
现象:小亮观察到现象,证明了两者发生了反应。
2.温度差法:适用于反应前后温度的变化通过测定溶液温度的变化进行判断。将稀盐酸慢慢滴入盛有氢氧化钠溶液的烧杯中,用温度计测量烧杯中溶液的温度,温度随加入稀盐酸的质量变化曲线。
例:将稀盐酸慢慢滴入盛有氢氧化钠溶液的烧杯中,用温度计测量烧杯中溶液的温度,温度随加入稀盐酸的质量变化曲线如图所示。
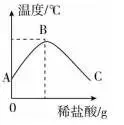
⑴在滴加的过程中,烧杯中溶液的pH逐渐(填”增大“、”减小“或”不变“)。
⑵由图可知,稀盐酸与氢氧化钠溶液发生的反应是(填”放热“或”吸热“)反应。
⑶图中B点时,溶液中的溶质是(填化学式)。
解析:有些反应没有明显的现象,但反应过程中会放出热量,使溶液的温度发生变化,故可以借助温度计或温度传感器测量两种溶液混合后温度的变化情况,从而判断反应的发生情况。
典型考题(转载)
1.如图所示,小组同学研究“CO2与水的反应”。三颈瓶中充满CO2,将注射器中的蒸馏水缓慢注入三颈瓶中,54s至100s,缓慢将注射器拉至原刻度处。实验前测得蒸馏水的pH为7,过程中用传感器采集液体pH和相对压强(将初始压强设置为0)。下列说法不正确的是( )
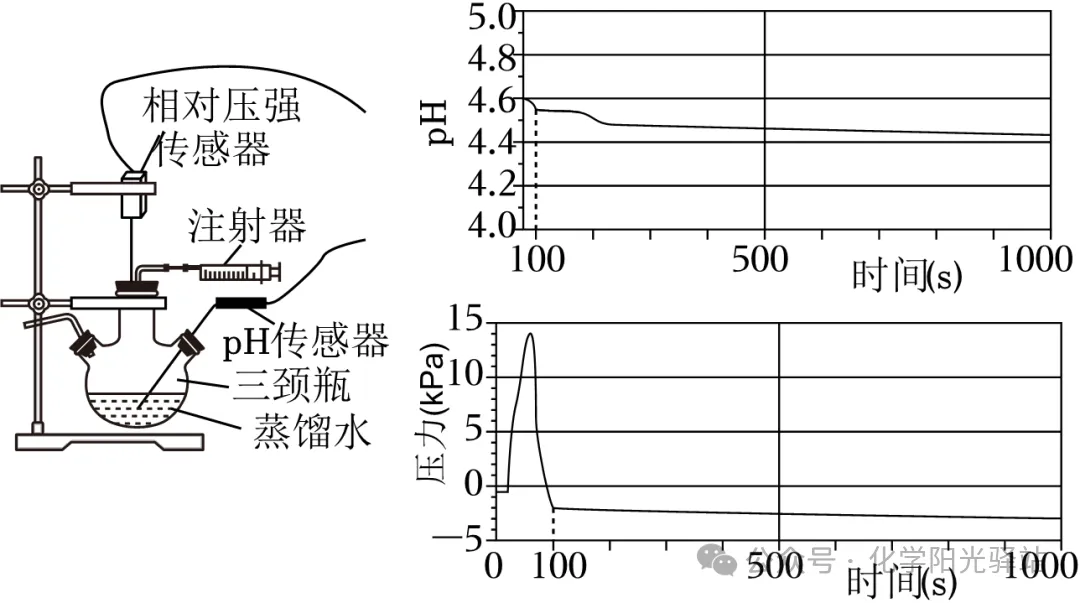
A.实验前需要检查装置气密性
B.pH下降的原因是CO2和水反应生成了碳酸
C.压强下降可以证明CO2与水的反应
D.100s后CO2继续与水反应
【解答】解:A、该反应有气体参加反应还要测定相对压强的变化,实验前需要检查装置气密性,故A说法正确;
B、pH下降的原因是CO2和水反应生成了碳酸,故B说法正确;
C、由于二氧化碳能溶于水,压强下降不可以证明CO2与水的反应,故C说法不正确;
D、由图示可知,100s后pH还在下降酸性增强,说明了CO2继续与水反应,故D说法正确。
故选:C。
2.某小组用图1的装置探究CO2的化学性质。相同条件下,分别将等体积的水、澄清石灰水和氢氧化钠溶液注入集满CO2的锥形瓶中,测得压强随时间的变化如图2。下列说法错误的是( )
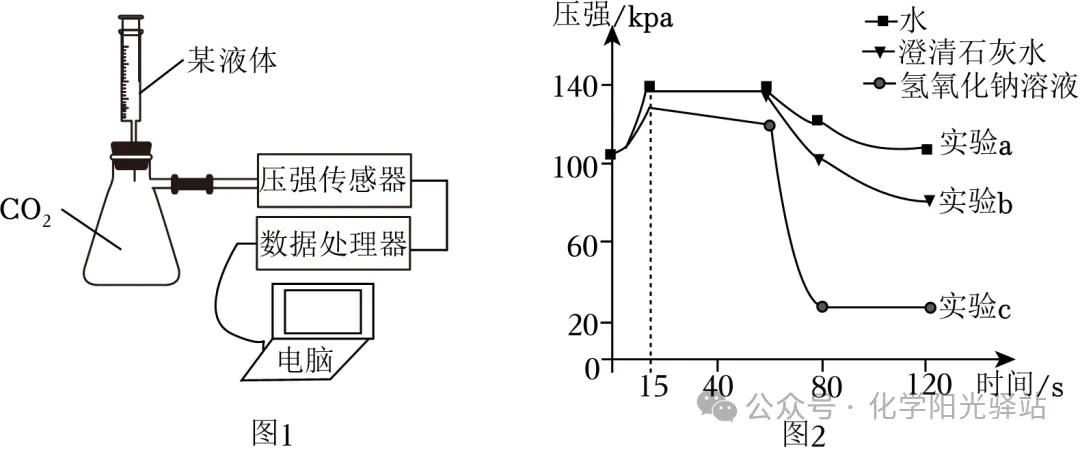
A.0~15s,压强迅速上升是因为向锥形瓶中注入了液体
B.100s时,实验c中锥形瓶内的CO2已经被完全吸收
C.实验a中反应生成了能使紫色石蕊溶液变红的物质
D.对比三组实验,氢氧化钠溶液吸收CO2的效果最好
【解答】解:A、0~15s,压强迅速上升是因为向锥形瓶中注入了液体,气体被压缩从而引起气体压强增大,故A正确;
B、根据题干信息,锥形瓶内集满二氧化碳,如果100s时二氧化碳被完全吸收,此时气体的压强应变为接近0(存在少量水蒸气),但100s时瓶内气体压强仍较大,说明二氧化碳没有被完全吸收,故B错误;
C、实验a中的反应是水和二氧化碳反应生成碳酸,碳酸能使紫色石蕊溶液变红,故C正确;
D、对比三组实验,实验c中压强变化最大,故氢氧化钠溶液吸收二氧化碳的效果最好,故D正确。
故选:B。
3.如图进行实验,关闭K,向盛满CO2的U形管中注入足量NaOH溶液,一段时间后,打开K并滴加足量稀盐酸,实验过程中观察到气球先变瘪后变大。关于该实验的说法不正确的是( )
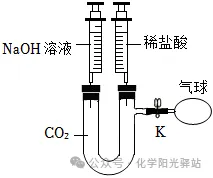
A.气球变瘪可证明二氧化碳能与氢氧化钠反应
B.滴加稀盐酸后,U形管内混合液的pH逐渐减小
C.气球变大是因为有二氧化碳产生
D.注入NaOH溶液后U形管内压强减小
【解答】解:A、二氧化碳能溶于水,则装置中的气体减少,压强减小,则气球变瘪不可证明二氧化碳能与氢氧化钠反应,故A错误;
B、氢氧化钠与二氧化碳反应生成碳酸钠和水,碳酸钠溶液显碱性,而碳酸钠与盐酸反应生成氯化钠、水和二氧化碳,则碱性减弱,pH减小,故B正确;
C、滴加盐酸时,有气体生成,则气球变大,故C正确;
D、氢氧化钠消耗了二氧化碳,气体减小,压强减小,故D正确。
故选:A。
4.电导率是衡量溶液导电能力大小的物理量,在相同条件下,电导率与离子浓度(单位体积内的离子数)成正比,盐酸和氢氧化钠反应电导率曲线如图所示,以下分析不正确的是( )
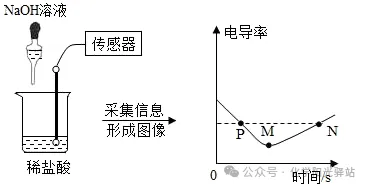
A.电导率减小可能是由于溶液中离子数量逐渐减小
B.M点时NaOH溶液与稀盐酸恰好完全反应
C.N点时溶液中的离子数大于P点
D.该实验证明溶液中始终含有带电的粒子
【解答】解:A、电导率减小,是由于溶液中离子浓度逐渐减小,该选项说法不正确;
B、M点时电导率最低,是因为NaOH溶液与稀盐酸恰好完全反应,离子浓度最小,该选项说法正确;
C、N点时氢氧化钠过量,溶液中的离子数大于P点,该选项说法正确;
D、该实验中电导率始终大于0,证明溶液中始终含有带电的粒子,该选项说法正确。
故选:A。








