山东济宁市2026届高三下学期高考模拟考试
山东济宁市2026届高三下学期高考模拟考试
化学试题
注意事项:
1.答题前,考生务必将自己的姓名、考生号、座号填写在相应位置,认真核对条形码上的姓名、考生号和座号信息,并将条形码粘贴在指定位置。
2.选择题答案必须使用2B铅笔正确填涂;非选择题答案必须使用0.5毫米黑色签字笔书写,绘图时可使用2B铅笔,字体工整、笔迹清晰。
3.请按照题号在各题目的答题区域内作答,超出答题区域书写的答案无效;在草稿纸、试题卷上答题无效。保持答题卡清洁,不折叠、不破损。
可能用到的相对原子质量:H-1C-12N-14O-16Na-23Cl-35.5Mn-55Fe-56
一、选择题:本题共10小题,每小题2分,共20分。每小题只有一个选项符合题目要求。
1. 馆藏文物是历史见证,下列文物主要成分为硅酸盐的是
|
|
A.商朝四羊青铜方尊 | B.战国曾侯乙墓竹简 |
|
|
C.西汉素纱禅衣 | D.唐代三彩腾空马 |
A. AB. BC. CD. D
2. 化学品在食品工业中有重要应用,下列说法错误的是
A. CaSO4可用作豆腐生产的凝固剂B. 硫酸铁可用作铁强化酱油补铁剂
C. 活性炭可用作食品脱色剂D. 谷氨酸钠可用作调味剂
3. 关于实验室安全,下列说法错误的是
A. 钠着火时,可用泡沫灭火器灭火
B. 点燃甲烷前,须检验气体的纯度
C. 酒精灯不慎被碰倒着火,可用湿抹布盖灭
D. 不慎将苯酚沾到皮肤上,应立即用酒精冲洗,再用水冲洗
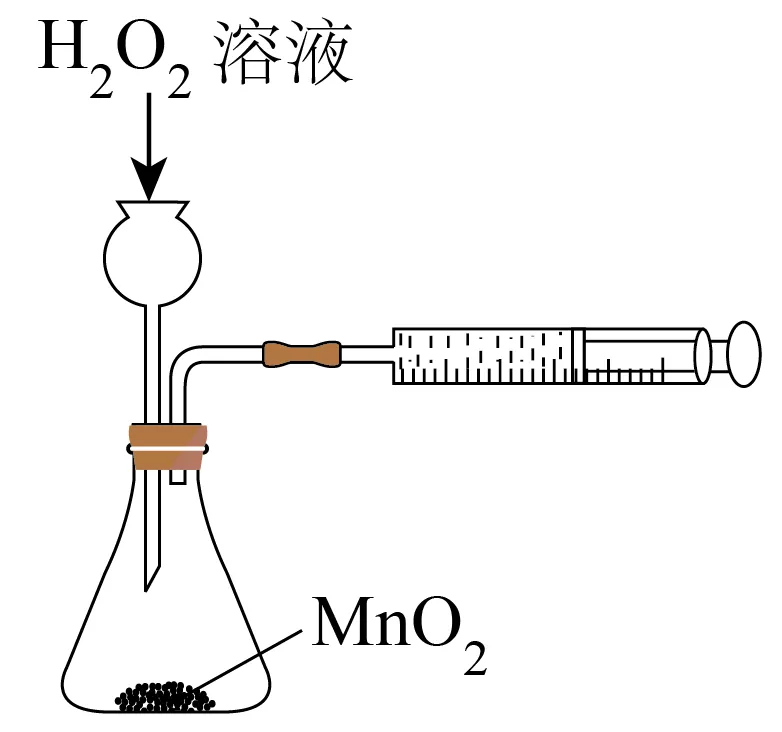
4. 下列图示中,实验操作或方法符合规范 是
是
|
|
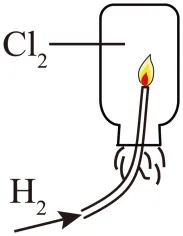
A.测定H2O2溶液分解反应速率 | B.观察H2在Cl2中的燃烧 |
|
|
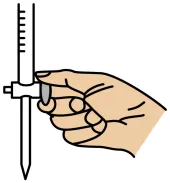
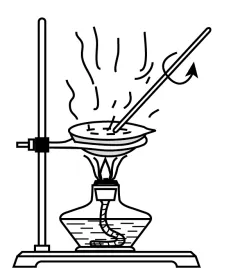
C.调控滴定速度 | D.蒸干Fe2(SO4)3溶液得到Fe2(SO4)3晶体 |
A. AB. BC. CD. D
5. 下列过程中发生的化学反应,离子方程式书写错误的是
A. 向硫酸氢钠溶液中滴加少量碳酸氢钡溶液: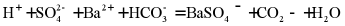
B. TiCl4加入水中: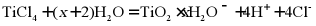
C. 用碳酸钠溶液浸泡锅炉水垢中的硫酸钙: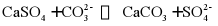
D. Na2CO3溶液中通入少量氯气: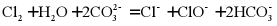
6. 雄黄和雌黄是提取砷的主要矿物原料,二者均为砷的硫化物,其球棍模型如图所示, 表示阿伏加德罗常数的值。下列说法错误的是
表示阿伏加德罗常数的值。下列说法错误的是
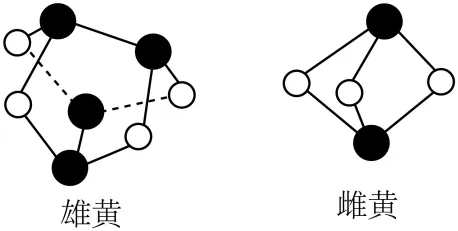
A. 雌黄为只含有极性键的非极性分子B. 两物质中As元素价态相同
C. 两物质中所有原子均为sp3杂化D. 1mol雄黄的孤电子对数为12
7. 下列关于物质性质的解释错误的是
A. 离子液体具有导电性,因为离子液体中有可移动的阴、阳离子
B. O3在水中溶解度小于在CCl4中,因为O3为非极性分子
C. P形成PF5而N形成NF3,因为P的价层电子轨道更多且半径更大
D. 酸性:HClO>HBrO,因为电负性:Cl>Br
8. 石墨炭负载单原子铁催化2CO(g)+2NO(g)=N2(g)+2CO2(g)反应的能量变化如图所示(*表示在催化剂表面吸附),下列关于该反应的说法错误的是
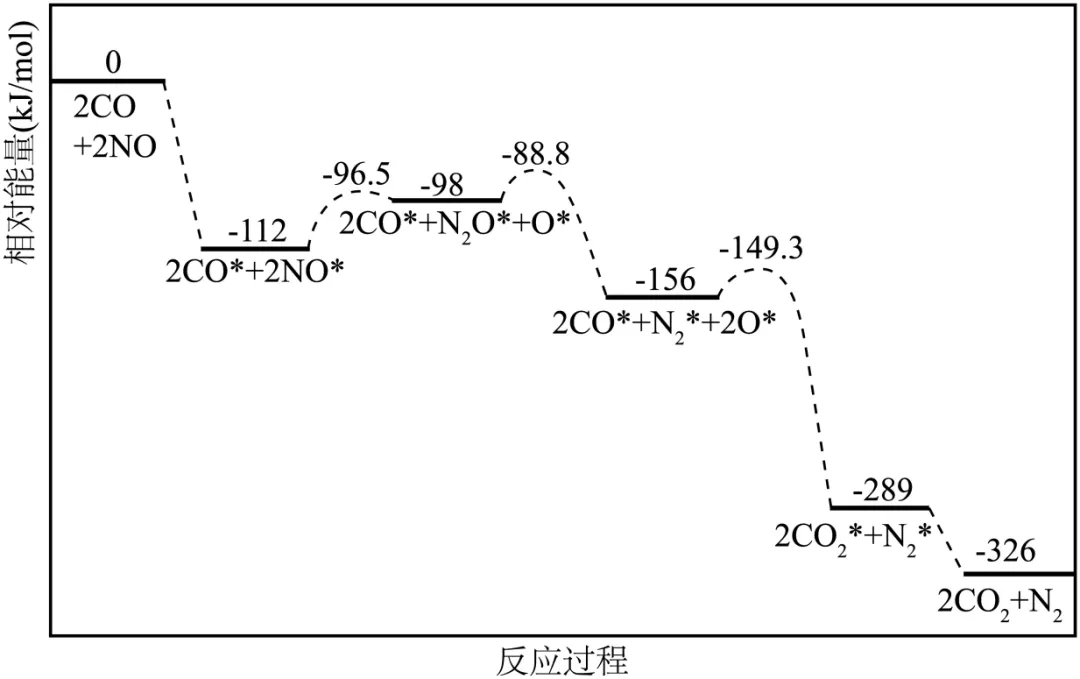
A. 该反应低温下可自发进行
B. 正反应 决速步为2NO*→N2O*+O*
决速步为2NO*→N2O*+O*
C. 升高温度化学反应速率增大程度为v逆 <v< span>正 </v<>
D. 该过程包含三个基元反应
9. 工业上为了提高Au的浸取率常将其放在一定量的Na2S2O3、CuSO4、NH3·H2O的混合溶液中,其反应机理为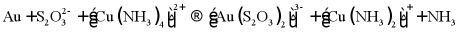 (未配平),反应过程中不断通入O2,可实现[Cu(NH3)4]2+的再利用,已知
(未配平),反应过程中不断通入O2,可实现[Cu(NH3)4]2+的再利用,已知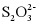 可看作是
可看作是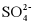 中的一个O被S替代的产物,[Cu(NH3)4]2+中的两个NH3被两个
中的一个O被S替代的产物,[Cu(NH3)4]2+中的两个NH3被两个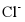 取代后形成两种结构不同的产物,以下说法错误的是
取代后形成两种结构不同的产物,以下说法错误的是
A. 79Au位于元素周期表中的ds区
B. 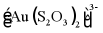 中配位原子为S
中配位原子为S
C. [Cu(NH3)4]2+中Cu2+与N均采用sp3杂化
D. 理论上参加反应的Au与O2的物质的量比为4∶1
10. 镍基催化剂可以催化储氢物质氨硼烷(NH3BH3)的分解反应:
I.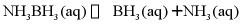
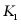
Ⅱ.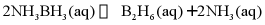
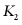
恒温条件下,以氨硼烷的四氢呋喃溶液为原料(含NH3BH3的物质的量为n)进行实验,得到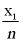 、
、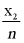 、
、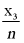 随时间t变化的曲线。其中x1为BH3与NH3的物质的量之和,x2为BH3的物质的量,x3为剩余NH3BH3的物质的量。
随时间t变化的曲线。其中x1为BH3与NH3的物质的量之和,x2为BH3的物质的量,x3为剩余NH3BH3的物质的量。
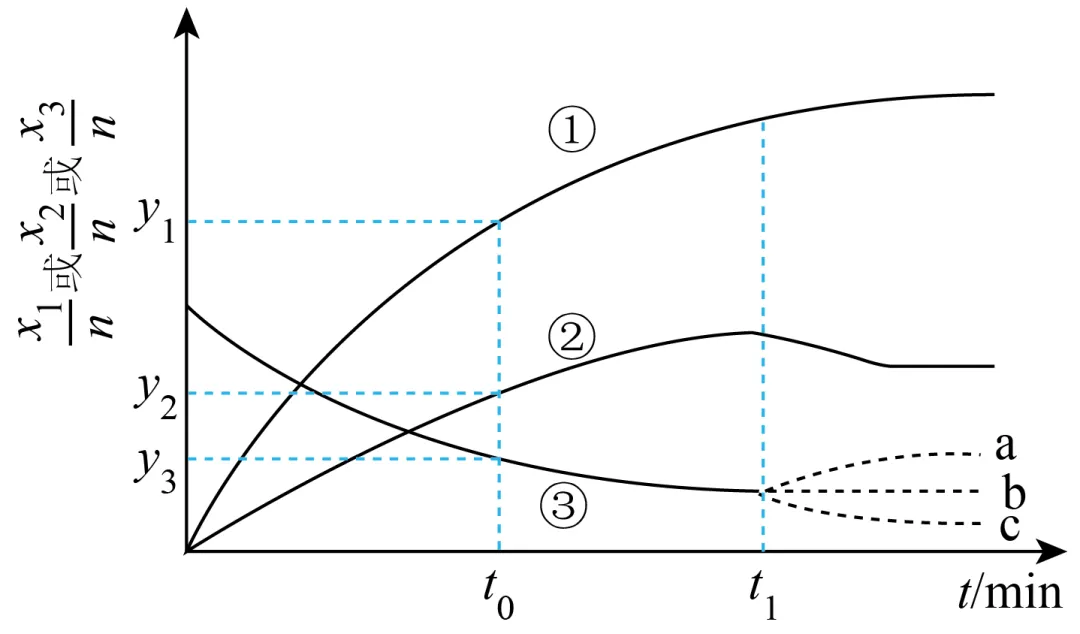
下列说法正确的是
A. 0~t0内,NH3BH3的转化率为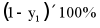
B. t1后曲线③的变化趋势可能为a
C. 
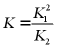
D. 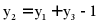
二、选择题:本题共5小题,每小题4分,共20分。每小题有一个或两个选项符合题目要求,全部选对得4分,选对但不全的得2分,有选错的得0分。
11. 下列实验操作和现象及所得结论均正确的有
选项 | 实验操作和现象 | 结论 |
A | 向盛有2 mL鸡蛋清溶液的试管中滴加AgNO3溶液,有沉淀析出,加蒸馏水稀释后,振荡,沉淀不溶解 | 蛋白质活性发生改变 |
B | CH3CH2Br与NaOH的乙醇溶液共热,将产生的气体通入KMnO4溶液中,溶液褪色 | 有CH2=CH2生成 |
C | 向某卤代烃中滴加NaOH水溶液振荡后加热,静置。取上层水溶液于试管中,加入足量HNO3,再滴加AgNO3溶液,产生白色沉淀 | 该卤代烃中的卤素原子为Cl |
D | 向2 mL 10% | M中无醛基 |
A. AB. BC. CD. D
12. X、Y、Z、M、Q为元素周期表中原子序数依次增大的前四周期元素,可形成如图所示配合物,已知基态Q原子的价电子数与最外层电子数之比为5∶1,Z、M处于对角线位置,下列说法错误的是
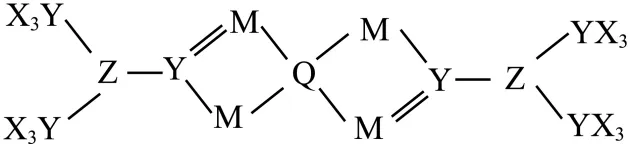
A. 化合物XYZ和YM2均为直线形分子
B. 该配合物中Q元素的化合价为+2
C. M的简单氢化物与少量Z的简单氢化物在水溶液中反应生成(ZH4)2M
D. 该配合物中配体数与配位数之比为1∶2
13. 在双室电解槽中实现两种尼龙单体的高效同步制备,装置原理如图所示。下列说法正确的是
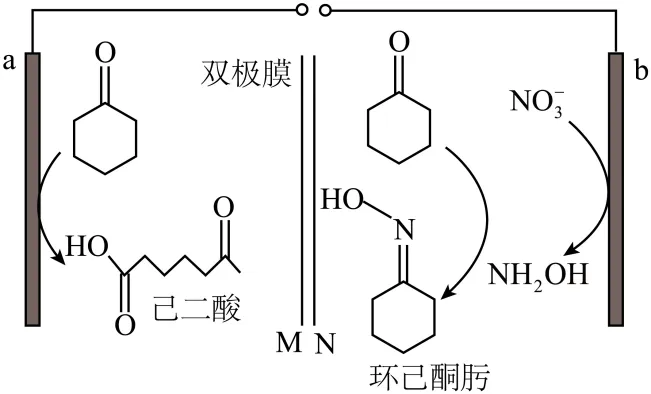
A. b极与电源正极相连
B. M膜为阳离子交换膜
C. 理论上生成1 mol己二酸,可以产生1 mol环己酮肟
D. 电解过程中,阴极室溶液pH增大
14. Carroll重排反应如图所示,下列说法正确的是
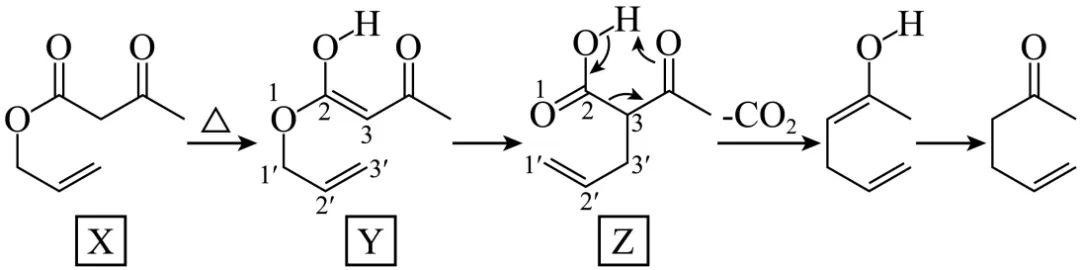
A. X与足量H2充分反应的产物中含有2个手性碳
B. 依据红外光谱可确证Y、Z存在不同的官能团
C. 用14C标记3号碳原子,会生成14CO2
D. 类比上述反应,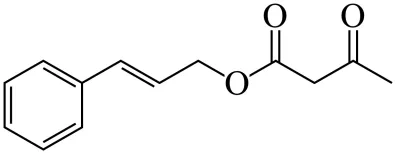 的产物为
的产物为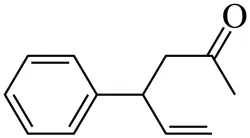
15. 常温下,将Ca2+初始浓度为0.01 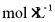 溶液,置于CO2、SO2分压固定的混合体系中,体系中lgM~pH关系如图所示。M为溶液中
溶液,置于CO2、SO2分压固定的混合体系中,体系中lgM~pH关系如图所示。M为溶液中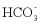 、
、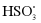 、
、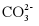 、
、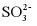 、Ca2+的浓度。(已知:
、Ca2+的浓度。(已知: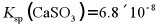 ;
;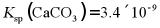 )
)
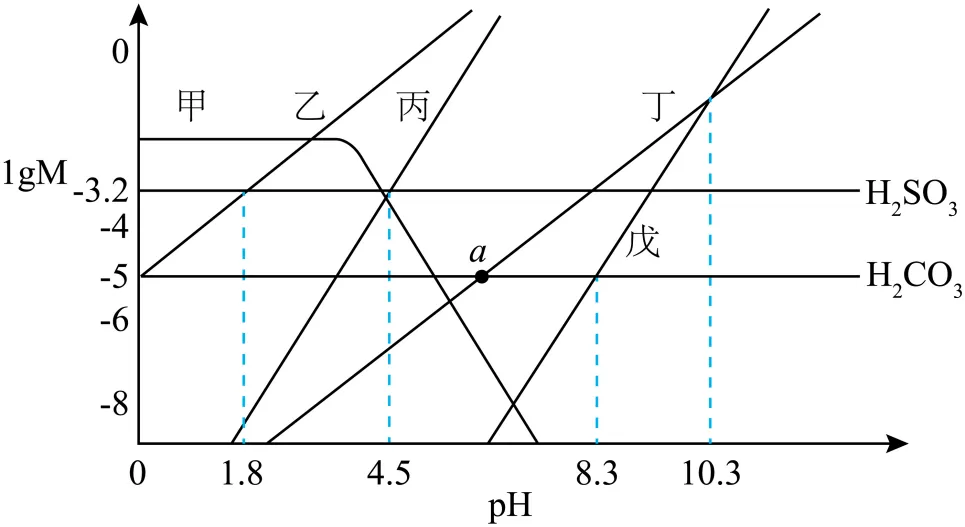
下列说法正确的是
A. 乙线表示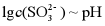
B. 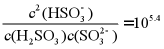
C. pH=4.6时,若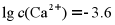 ,无CaSO3沉淀生成
,无CaSO3沉淀生成
D. a点坐标为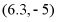
三、非选择题:本题共5小题,共60分。
16. Zn单质及其化合物应用广泛。回答下列问题:
(1)Zn在元素周期表中的位置为___________,同周期元素中,基态原子未成对电子数最多的元素的价层电子轨道表示式___________。
(2)三联吡啶锌叠氮配合物如图所示:
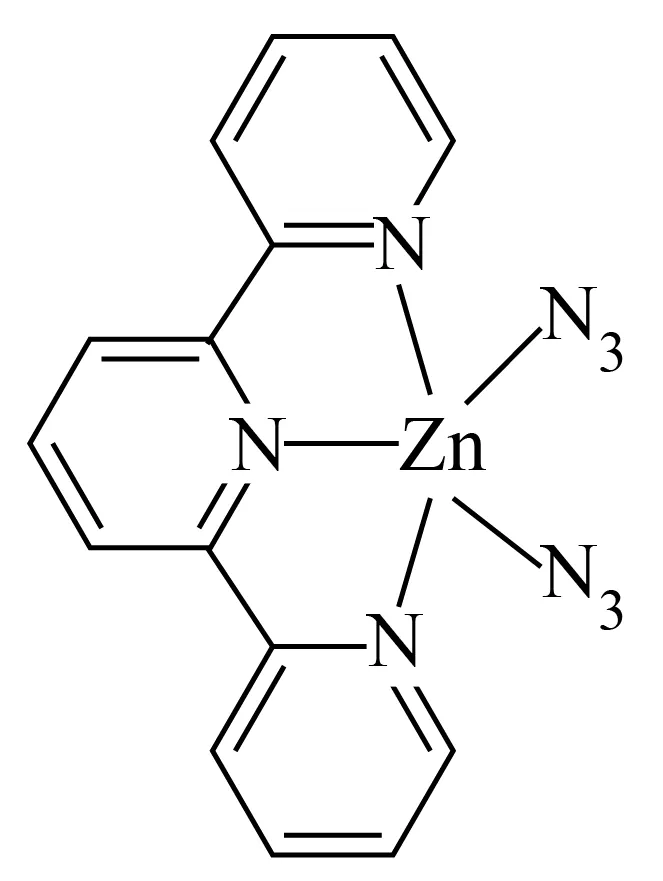
①配合物中主族元素的电负性由大到小的顺序为___________。
②配体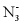 中心原子杂化方式___________,配体三联吡啶易溶于乙醇的原因___________。
中心原子杂化方式___________,配体三联吡啶易溶于乙醇的原因___________。
(3)ZnF2晶胞结构及其在xy面投影如图所示:
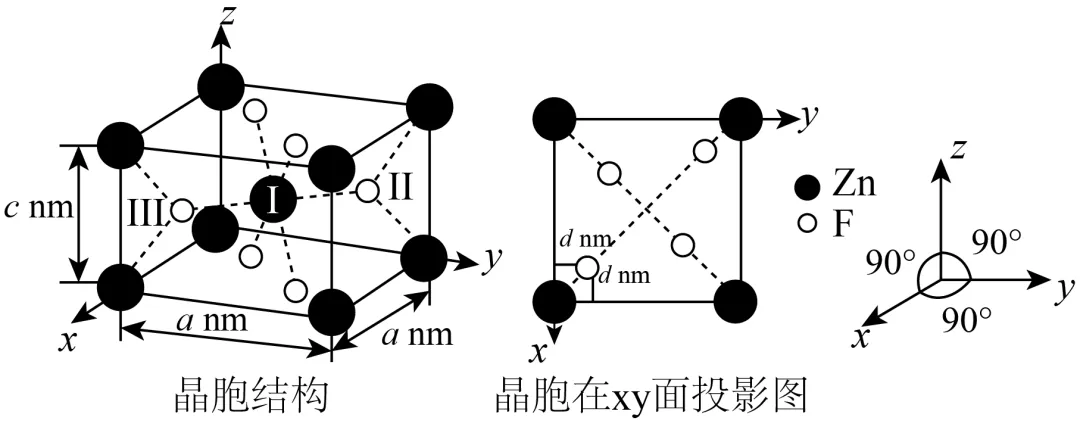
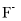 (II)的分数坐标___________,II、III两离子之间的距离为___________nm,Zn2+(I)周围的
(II)的分数坐标___________,II、III两离子之间的距离为___________nm,Zn2+(I)周围的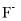 构成的空间结构___________。
构成的空间结构___________。
17. 海洋锰结核(主要成分为MnO2及铜、钴、铁等金属的氧化物)是一种富含多种金属元素的矿物资源,从中制备脱硫剂MnxOy,并回收金属的工艺流程如下:
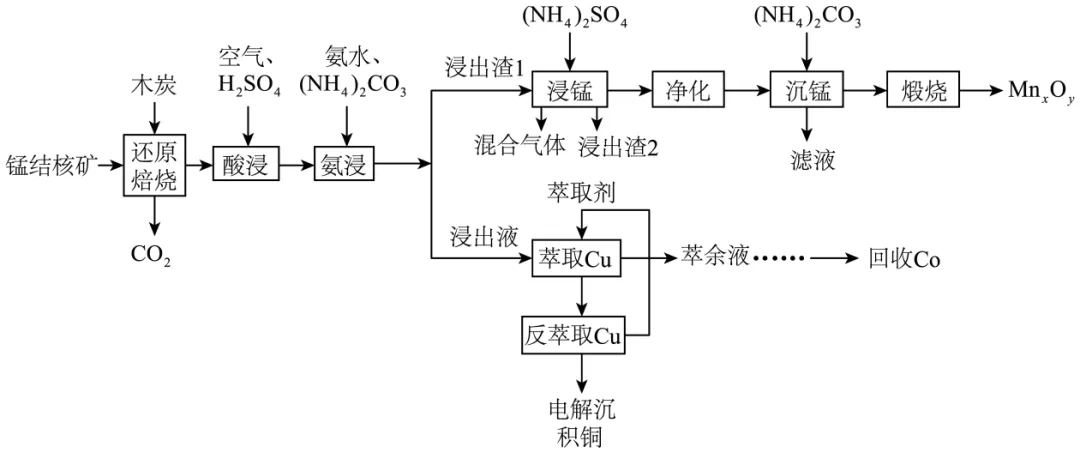
已知:氨浸时,铜、钴以氨络合离子形式进入溶液中,锰以碳酸锰形式进入浸出渣1中。
(1)“还原焙烧”时,加快反应速率的措施___________(任写一种),此过程中MnO2生成MnO的化学方程式___________。
(2)“氨浸”过程中氨水 作用为___________。
作用为___________。
(3)“浸锰”过程产生的混合气体成分为___________(写化学式),浸出渣2的成分为___________(写化学式)。
(4)“沉锰”中可能发生反应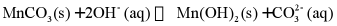 ℃时,该反应的平衡常数的对数值lgK=___________(填数值)。
℃时,该反应的平衡常数的对数值lgK=___________(填数值)。
已知: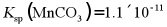 。
。
(5)萃取剂为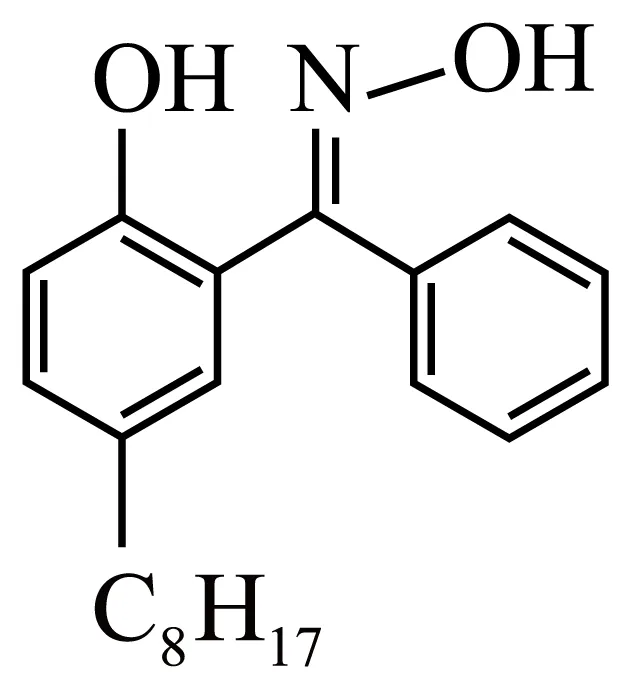 ,“萃取Cu”后铜元素的存在形式为
,“萃取Cu”后铜元素的存在形式为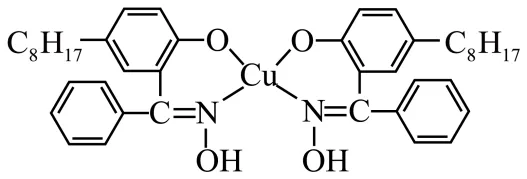 ,写出“萃取Cu”时的离子方程式(
,写出“萃取Cu”时的离子方程式(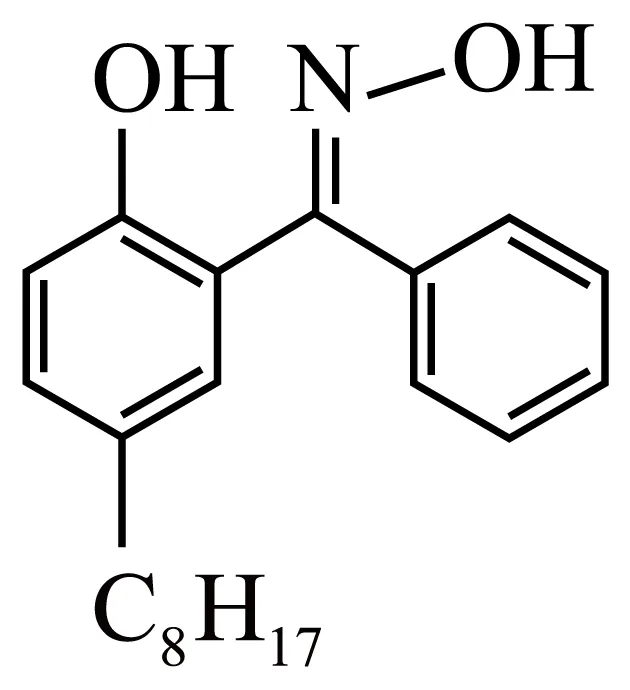 可简写为HR,产物可相应简化书写)___________。
可简写为HR,产物可相应简化书写)___________。
18. 苯亚甲基丙酮是重要的有机化工中间体,一种制备苯亚甲基丙酮的方法为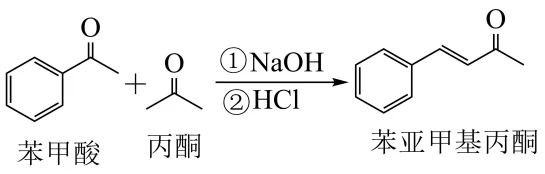 ,可能发生的副反应为:
,可能发生的副反应为: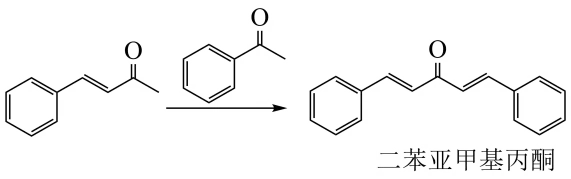 。
。
实验装置如图所示。
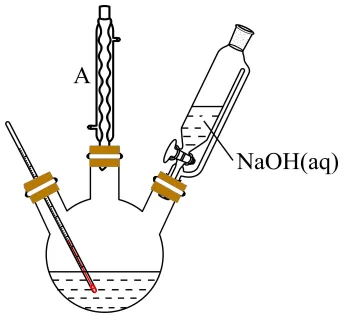
在反应装置中加入一定浓度的苯甲醛和丙酮混合溶液,滴加NaOH溶液,维持一定温度充分反应一段时间后,停止加热,加入盐酸,冷却并不断搅拌析出淡黄色固体。
已知:①苯甲醛易被O2氧化;
②苯亚甲基丙酮为淡黄色固体;
③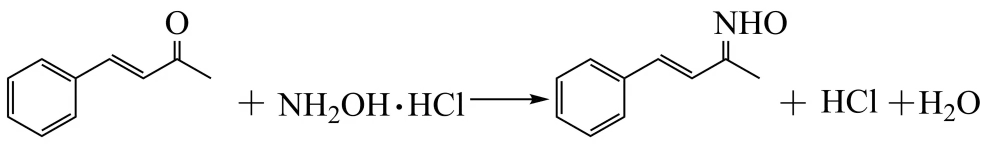 ;盐酸羟胺(NH2OH·HCl)与苯甲酸酸性相近。
;盐酸羟胺(NH2OH·HCl)与苯甲酸酸性相近。
(1)仪器A的名称___________。
(2)实验过程中有少量苯甲醛被氧化成苯甲酸,化学方程式为___________。
(3)投料时需保证丙酮过量的原因是___________。
(4)下图为苯甲醛转化率、苯亚甲基丙酮产率与温度的关系,反应所维持的最佳温度为___________。
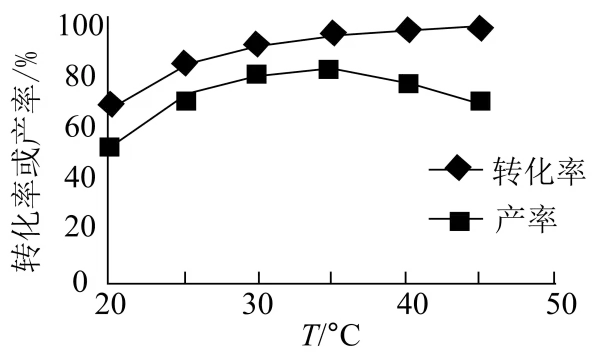
(5)所得产品中混有少量苯甲酸(其余杂质不参与反应),为了测定苯亚甲基丙酮和苯甲酸含量进行如下实验:①将a g样品溶解后加入过量NH2OH·HCl,完全反应后,用c 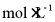 NaOH溶液滴定,第一滴定终点消耗V1 mL NaOH溶液;到达第二滴定终点共消耗V2 mL NaOH溶液;②空白实验:另取等量的NH2OH·HCl于锥形瓶中,用c
NaOH溶液滴定,第一滴定终点消耗V1 mL NaOH溶液;到达第二滴定终点共消耗V2 mL NaOH溶液;②空白实验:另取等量的NH2OH·HCl于锥形瓶中,用c 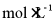 NaOH溶液滴定,消耗V mL NaOH溶液,苯亚甲基丙酮的质量分数为___________;苯甲酸的质量分数为___________[M(苯亚甲基丙酮)=146
NaOH溶液滴定,消耗V mL NaOH溶液,苯亚甲基丙酮的质量分数为___________;苯甲酸的质量分数为___________[M(苯亚甲基丙酮)=146 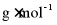 苯甲酸)=122
苯甲酸)=122 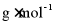 ];空白实验时,滴定前仰视读数,滴定后俯视读数,会使测得苯甲酸含量___________(填“偏高”“偏低”或“无影响”)。
];空白实验时,滴定前仰视读数,滴定后俯视读数,会使测得苯甲酸含量___________(填“偏高”“偏低”或“无影响”)。
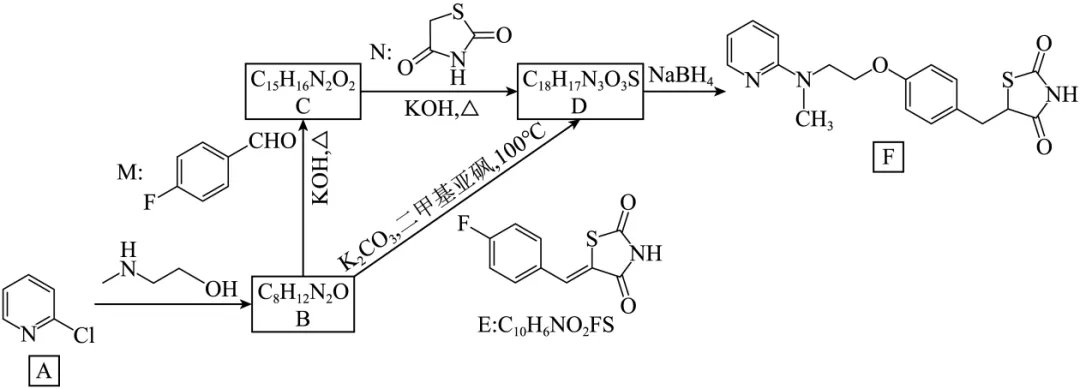
19. 化合物F是一种胰岛素增敏剂,合成路线如下:
已知:①吡啶(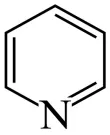 )少与苯环类似,具有芳香性。
)少与苯环类似,具有芳香性。
②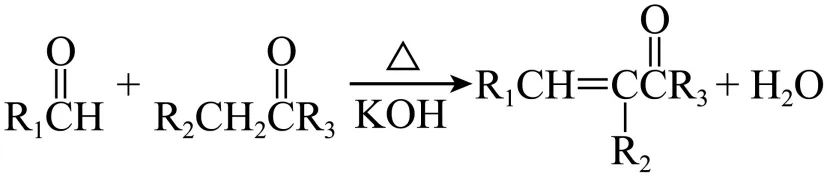 。
。
回答下列问题:
(1)M的化学名称为___________;B结构简式为___________;C中含氧官能团的名称为___________。
(2)C+N→D的反应分两步进行,反应类型分别为___________、___________。
(3)B→D化学方程式为___________。
(4)化合物X为A的同系物,且相对分子质量比A大14,则符合下列条件的X的同分异构体(含X)有___________种。
①含有六元环,且具有芳香性②N原子与Cl原子不直接相连
(5)结合上述信息,写出以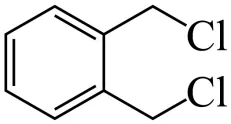 与
与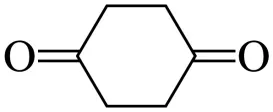 为原料,合成
为原料,合成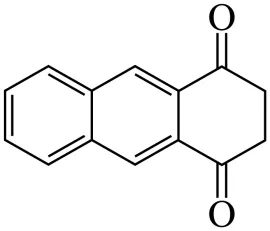 的路线___________(无机试剂任选)。
的路线___________(无机试剂任选)。
20. 1,3-丁二烯(C4H6)是生产丁苯橡胶的基本原料。1-丁烯(C4H8)氧化脱氢制1,3-丁二烯(C4H6)涉及反应如下:
I.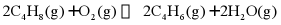
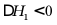
II.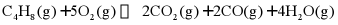
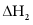
III.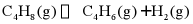
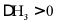
回答下列问题:
(1)在特定温度下,由稳定态单质生成1 mol物质的焓变叫做该物质在此温度下的标准摩尔生成焓。下表为几种物质在298 K时的标准摩尔生成焓
物质 | H2O | CO | CO2 | C4H8 | O2 |
标准摩尔生成焓 |
|
|
|
| 0 |
经计算,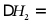 ___________
___________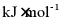 。
。
(2)已知反应空速是指单位时间内通过单位体积催化剂 原料气体流量。一定条件下,不同空速对1-丁烯氧化脱氢反应性能的影响如图所示。
原料气体流量。一定条件下,不同空速对1-丁烯氧化脱氢反应性能的影响如图所示。
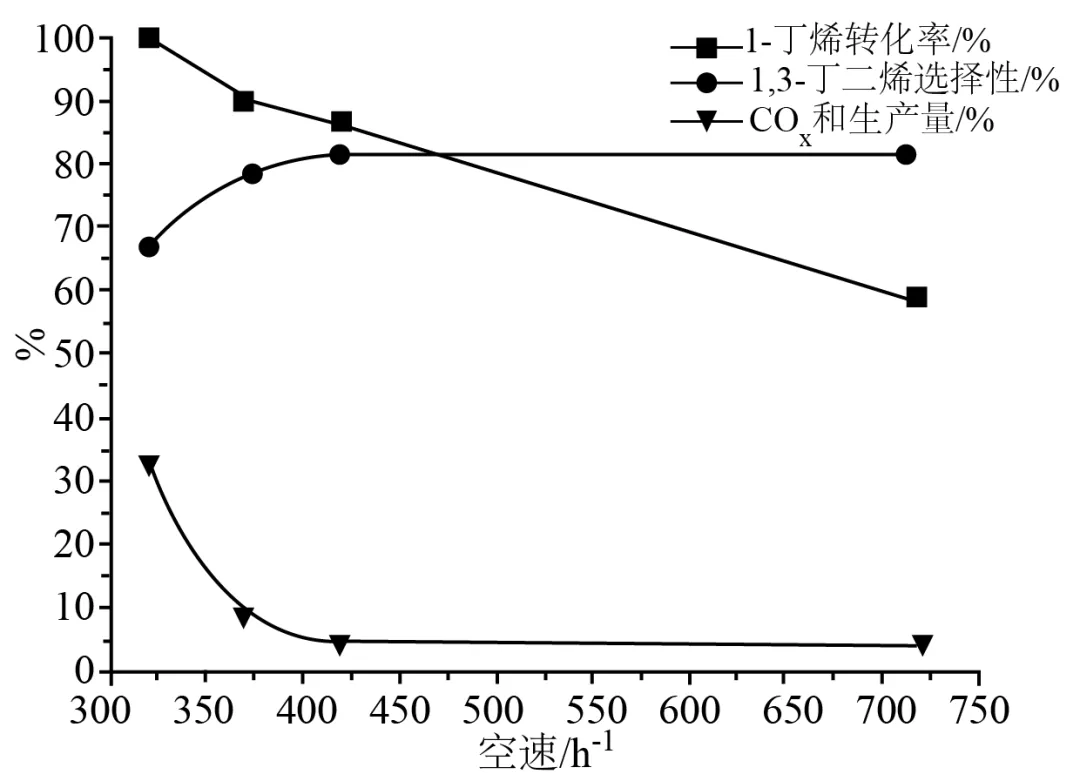
其中较适宜的空速为___________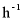 ,空速过小或过大时,1,3-丁二烯产率较低的原因是___________。
,空速过小或过大时,1,3-丁二烯产率较低的原因是___________。
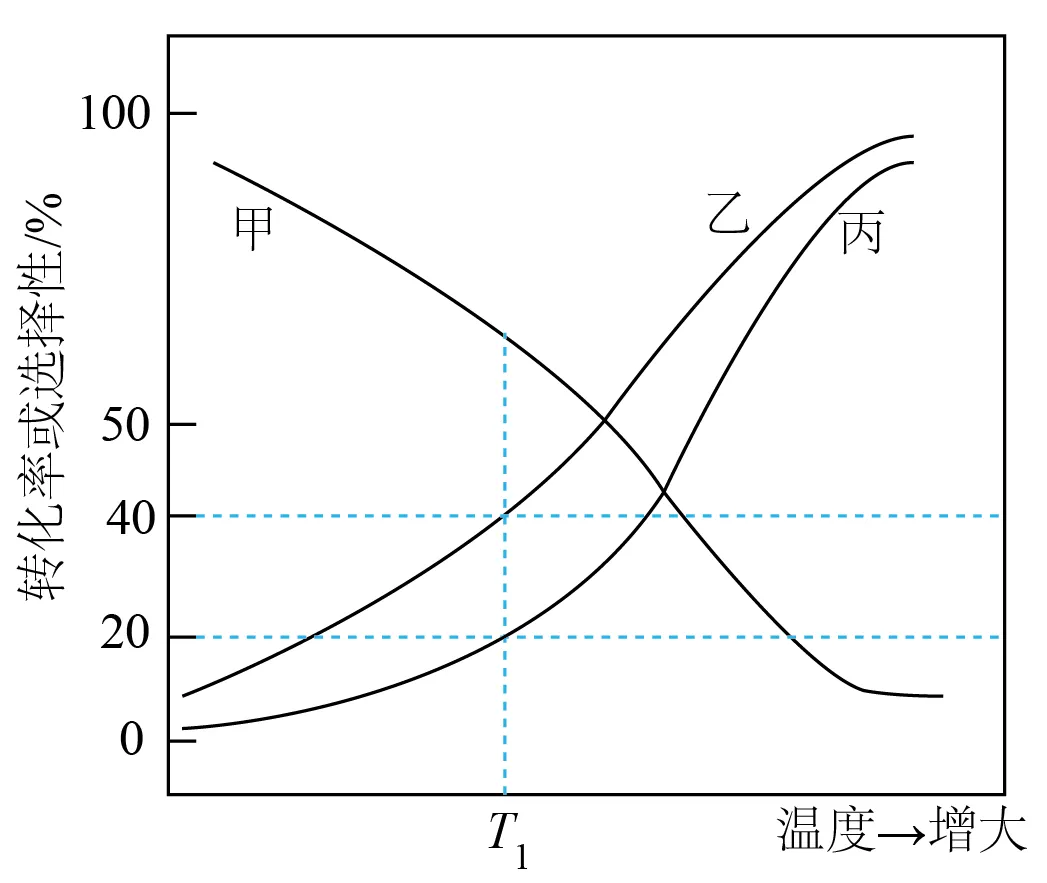
(3)体积为1 L密闭容器中,加入2 mol C4H8、1 mol O2发生反应I、II、III,C4H8的平衡转化率、C4H6和COx的选择性(S)随温度变化如图所示。
已知: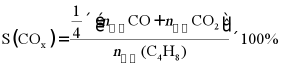
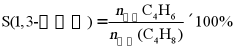
图中表示S(COx)的曲线为___________;T1温度时,n(O2)=a mol,n(H2O)=___________;反应I的Kc=___________(用含a的最简代数式表示)。
解析链接: https://pan.baidu.com/s/172uvcBOVFqKsSY7cuGfGQQ?pwd=j29v 提取码: j29v