把CO₂“抓”起来变燃料?中考化学“碳捕集”考点全突破
[原题材料]
为实现“碳中和”目标,人类不仅需要减少二氧化碳(CO₂)排放,还需主动从大气或工业尾气中捕获并利用它,这项技术被称为“碳捕集、利用与封存”(CCUS)。
捕集是第一步。常用方法是利用碱性溶液(如氢氧化钠溶液)吸收CO₂。这是因为CO₂是一种酸性氧化物,能与碱反应生成盐和水。例如,用澄清石灰水[Ca(OH)₂溶液]检验CO₂,就是此原理的简单应用,反应会生成白色的碳酸钙(CaCO₃)沉淀。
利用是关键。捕获的CO₂并非“废物”,可转化为资源。在催化剂作用下,CO₂能与氢气反应,生成甲醇(CH₃OH)和水,其反应的微观示意图如下图所示。此外,CO₂还可注入温室促进植物光合作用,或用于生产碳酸饮料。
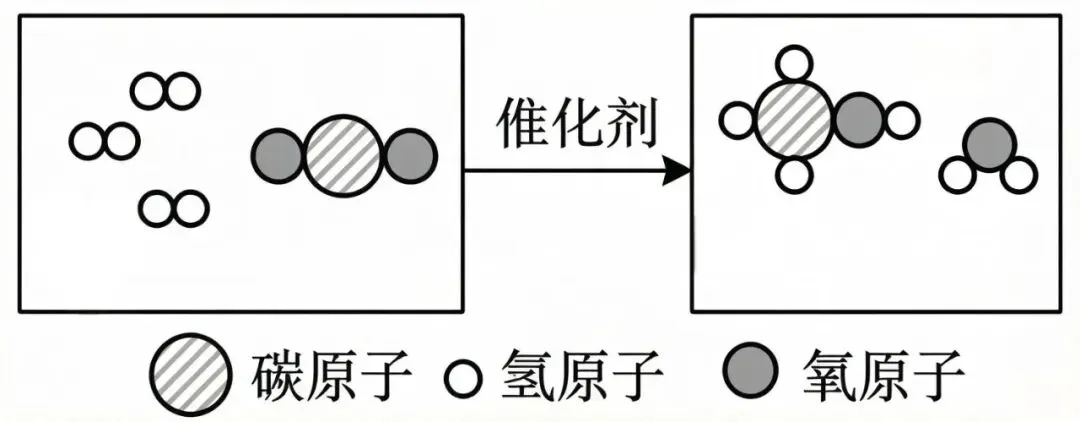
封存是最后手段,将超临界CO₂注入深层地质构造中永久储存。我国在燃煤电厂、水泥厂等排放源附近已开展多项CCUS示范项目。
[阅读与审题指导]
抓关键:圈出“二氧化碳(CO₂)”、“酸性氧化物”、“碱液吸收”、“碳酸钙(CaCO₃)”、“与氢气(H₂)反应”、“催化剂”、“生成甲醇(CH₃OH)”、“碳中和”这几个核心词。它们串联了从捕集原理到资源化利用的完整化学链条。
【考点闯关】
依据上文,回答问题:
1.大气中CO₂含量过高,会导致 ______效应增强,加剧全球气候变化。
2.实现“碳中和”目标中的“碳”,主要是指()。
A. 碳元素B. 二氧化碳
C. 碳单质D. 所有含碳物质
3.文中提及,可用氢氧化钠(NaOH)溶液吸收CO₂,其反应原理与CO₂的检验一样,请写出该反应的化学方程式:______。
4.请写出微观示意图中,二氧化碳与氢气在催化剂作用下反应生成甲醇(CH₃OH)的化学方程式:______。
5.“碳封存”可以减少二氧化碳排放,“碳封存”可将CO₂压缩至地下,转化为液态CO₂储存,其原因是:______(从微观角度解释)。
(✅点击下面空白查看答案)
▼

(✅点击下面空白查看解析)
▼

��今日要点小结:
1.环境问题:过量CO₂导致温室效应,需通过CCUS等技术实现“碳中和”。
2.捕集原理:利用CO₂是酸性氧化物,可与碱反应生成盐和水。
3.利用路径:在催化剂作用下,CO₂可与H₂反应生成甲醇等资源。
4.封存依据:气体分子间存在间隔,可被压缩液化。
【声明与参考】
本文所涉科学原理与技术应用基于公开的科技报道与初中化学知识。题目设计与解析均为原创,旨在结合科技前沿与社会热点,服务于教学与科普。






