2025年江西高考真题:第7题有关c选项,氧化钠和水反应滴入酚酞,先变红后褪色。老师平时教学过程认真酚酞与氧化钠,只变色,不褪色,实质是会褪色,有关褪色的原因,我们再探究
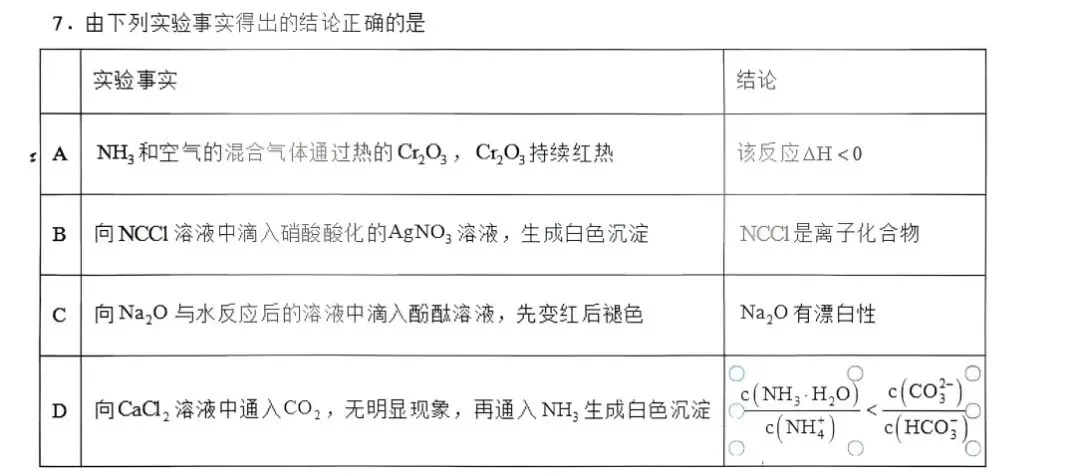
官方解析:

酚酞遇酸碱变化过程中的颜色变化研究
一、引言
酚酞是一种广泛应用的酸碱指示剂,其颜色会随着溶液酸碱度的改变而发生显著变化。这种特性使得酚酞在化学实验,尤其是酸碱滴定实验中发挥着重要作用。准确理解酚酞遇酸碱变化过程中的颜色变化规律,对于正确判断溶液的酸碱性、进行精确的化学分析具有重要意义。
二、酚酞在不同酸碱条件下的颜色变化
2.1 强酸性条件(pH < 0)
在强酸性环境中,酚酞以H3In+的形式存在。从分子结构上看,此时酚酞分子具有特定的化学键连接方式和电子云分布。这种结构使得分子能够吸收特定波长的光,从而使溶液呈现橘红色。具体来说,分子中的某些化学键在强酸性条件下处于稳定的状态,其电子跃迁所吸收的光的波长对应于橘红色光的互补色,因此人眼观察到的溶液颜色为橘红色。
2.2 酸性或近中性条件(0 < pH < 8.2)
当溶液的pH值处于0到8.2之间时,酚酞以H2In的形式存在。在这个pH范围内,酚酞分子的结构相对稳定,分子的电子云分布使得它对可见光的吸收较少。因此,溶液呈现无色。这是由于分子结构决定了它在该pH范围内几乎不吸收可见光,人眼看到的就是无色的溶液。
2.3 碱性条件(8.2 < pH < 12.0)
随着溶液pH值的升高,当处于8.2到12.0之间的碱性环境时,酚酞转化为In2 - 。在这个阶段,分子的结构发生了明显变化,形成了新的化学键和电子云分布。这种新的结构使得分子能够吸收特定波长的光,从而呈现出粉红至紫红色。具体而言,分子中的化学键在水解或其他反应作用下发生了改变,导致电子跃迁所吸收的光的波长对应于粉红至紫红色光的互补色,因此溶液呈现出相应的颜色。
2.4 强碱性条件(pH > 12.0)
当溶液的pH值大于12.0时,处于强碱性环境,酚酞以InOH3 - 的形式存在。在这种强碱性条件下,分子的结构再次发生变化,使得它对可见光的吸收减少,溶液又恢复到无色状态。这是因为分子结构的变化导致其光学性质发生了改变,不再吸收特定波长的光而呈现出无色。
三、颜色变化机理分析
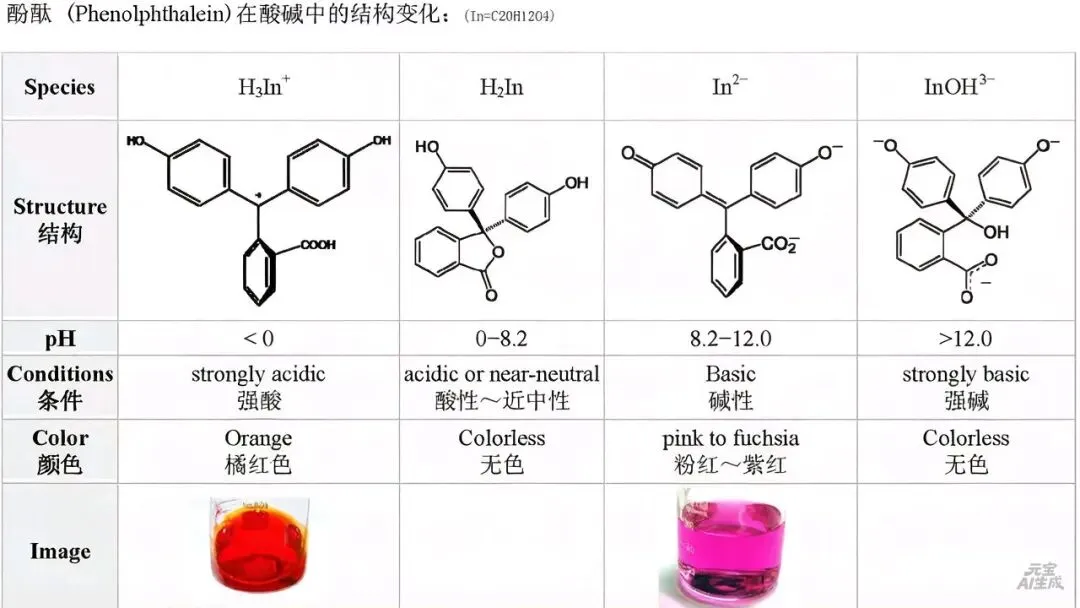
酚酞的颜色变化本质上是由于其分子结构在不同酸碱条件下的改变酚酞共轭体系对光吸不同所引起的。在酸性条件下,酚酞分子的质子化程度较高,分子结构相对稳定,对光的吸收特性使得它呈现无色或橘红色。随着溶液pH的升高,酚酞分子逐渐失去质子,结构发生变化,形成了具有不同电子云分布的物种。在碱性条件下,这些新的物种能够吸收特定波长的光,从而呈现出粉红至紫红色。当溶液的碱性过强时,分子结构再次发生变化,导致其对光的吸收减少,又恢复到无色。
这种结构变化与分子内的化学键断裂和形成、电子云的重新分布等过程密切相关。例如,在碱性条件下,酚酞分子中的某些化学键可能会发生水解或其他反应,导致分子结构的改变。同时,电子云的重新分布会影响分子对光的吸收和反射,从而使我们观察到颜色的变化。
四、结论
综上所述,酚酞在遇酸碱变化过程中,其颜色会随着溶液pH值的变化而发生显著改变。从强酸性的橘红色到酸性或近中性的无色,再到碱性的粉红至紫红色,最后到强碱性的无色,这种颜色变化是由酚酞分子结构在不同酸碱条件下的改变所引起的。深入理解这一颜色变化规律,有助于我们在化学实验中准确使用酚酞作为酸碱指示剂,进行精确的酸碱滴定和其他化学分析。同时,这也为进一步研究有机化合物的光学性质和反应机理提供了重要的参考。
未来的研究可以进一步探索酚酞在不同溶剂、温度等条件下的颜色变化规律,以及其与其他物质相互作用时的颜色变化情况,以更全面地了解酚酞的性质和应用。






