(点击查看详情)
中考生物知识点汇总
【中考复习】生物专题知识点①:构成生物体的细胞、组织、器官和系统
【中考复习】生物专题知识点③:种群、群落、和生态系统及生物圈
中考化学考点汇总
备考指南

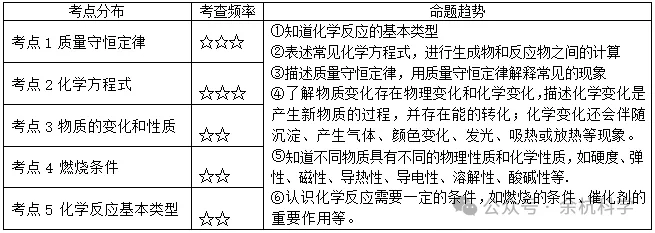
知识导图

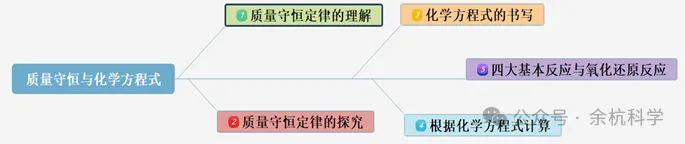
考点梳理

考点一 质量守恒定律

(1)质量守恒定律的概念:在化学反应中,参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和。
把握质量守恒定律应注意几点:
A、一切化学变化都遵循质量守恒定律
B、只有化学变化才遵守质量守恒定律,物理变化不用质量守恒定律解释!
C、质量守恒定律研究的仅是指“质量”,不能任意扩展到其它物理量;
D、守恒的是“总质量”,即“参加反应的各反应物的总质量”和“生成物的总质量”。如沉淀、气体等都应考虑进去。
E、“参加”,意味着没有参加反应(剩余)的物质的质量不能算在内。
(2)化学反应的过程就是组成反应物分子的原子重新组合成生成物分子的过程。
(3)化学反应前后原子的种类和数目不变,所以化学反应前后物质的质量总和必然相等。而物质的分子数和物态可能改变。
考点二 化学方程式

(一)化学方程式的概念
用化学式表示化学反应的方程式叫做化学方程式。
(二)化学方程式的读法
如C+O2=点燃=CO2,可读作“碳和氧气在点燃的条件下,反应生成二氧化碳”。
(三)化学方程式的意义
(1)表明了反应物反应物、生成物和反应条件;
(2)表示各物质间原子与分子的个数比;
(3)表示反应物、生成物各物质间的质量比。
(四)书写化学方程式的原则
(1)以客观事实为依据;
(2)遵守质量守恒定律,即在化学方程式左、右两边各原子的种类和数目必须相等。
(五)书写化学方程式的步骤
(1)根据反应事实,在式子的左边写反应物的化学式,在式子的右边写生成物的化学式,中间连一条短线。如果反应物或生成物不止一种,就分别用“+”连接。
(2)配平化学方程式。在化学式前配上合适的化学计量数,使式子两边每种元素的原子总数相等。一般可用最小公倍数来确定化学计量数。配平后把短线改为等号。
(3)注明反应条件和生成物的状态。把条件写在等号的上方或下方。如果反应物中没有气体,而生成物中有气体产生,则在气体的化学式旁边用“ ↑ ”号表示;如果是溶液中发生的反应,反应物中无固体,而生成物中有固体,则在固体的化学式旁边用“ ↓”号表示。
如:2H2O=通电=O2↑+2H2↑、
CO2+Ca(OH)2=CaCO3↓+H2O。
【注意点】
1.书写化学方程式的韵语:左写反应物,右写生成物;写准化学式,计量数要配平;中间连等号,条件要注明;生成气体和沉淀,要用箭头来标明。
2.在化学方程式中,“+”不能读作“加”,应读作“和”或“与”;“”不能读作“等于”,应读作“生成”。
3.判断化学方程式书写是否正确,从以下几个方面入手:
(1)是否符合客观事实,即反应能否发生,化学式是否正确;
(2)是否配平;
(3)反应条件是否正确;
(4)“↑”或“↓”是否标注正确。
4.配平化学方程式的方法除最小公倍数法外,还有奇数配偶法、观察法等。
(五)依据化学方程式进行计算
(1)由于化学方程式能表示反应前后各物质的质量关系,因此可以利用化学方程式计算化学反应中各成分的质量。
(2)根据化学方程式计算的一般步骤:设未知量→写出化学方程式→写出相关物质的相对分子质量和已知量→列出比例式、求解→对问题做出简明回答。

考点三 物质的变化和性质

1、物理变化和化学变化
(1)概念:有些变化不会产生新的物质,属于物理变化;
有些变化会产生新的物质,属于化学变化。
(2)实质(微观角度分析):物理变化过程中,分子种类不变;化学变化是构成物质分子的原子重新进行组合,形成了新的分子,分子种类改变。
2、物理变化和化学变化的区别及联系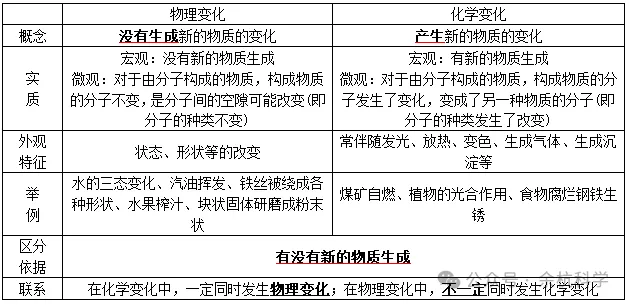
3、物理性质和化学性质
(1)概念:不需要发生化学变化就能表现出来的性质属于物质的物理性质;在化学变化中才能表现出来的性质属于物质的化学性质。
(2)常见性质分类:颜色、气味、状态、密度、熔点、沸点、溶解性、导电性、导热性、吸附性、磁性等属于物质的物理性质;可燃性、氧化性、还原性、酸碱性、活泼性、稳定性等属于物质的化学性质。
4、物质变化和物质性质之间的区别与联系
(1)区别:变化强调的是物质的某种运动过程,是正在进行着的或已经发生了的过程,重在“变”,因此变化往往用动词表示;性质是物质本身所具有的特征,不论变化是否正在进行,都是客观存在的事实,因此性质往往用“能”“不能”“可以”“不可以”“会”“容易”“难”等文字描述。
(2)联系:物质的性质是物质发生变化的内因,而物质的变化则是物质性质的具体体现。
考点四 燃烧条件

(一)燃烧
(1)燃烧的概念:通常情况下,可燃物与氧气发生的一种发光、放热的剧烈的氧化反应叫作燃烧。
(2)燃烧的必要条件(燃烧三要素,缺一不可):可燃物、有助燃剂(氧气)、温度达到着火点。
(3)影响燃烧的因素
1)可燃物不同,性质不同,燃烧现象不同。
2)氧气浓度越大,燃烧越剧烈。
3)可燃物与氧气的接触面积越大,燃烧越剧烈。
(4)可燃物的着火点:物质燃烧所需达到的最低温度叫着火点
不同物质的着火点是不同的。
已知白磷的着火点是40℃,红磷的着火点是240℃。
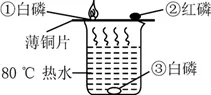
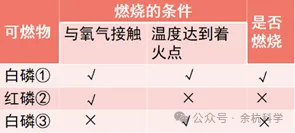
(5)自燃与爆炸
1)自燃:由于缓慢氧化产生的热量被积累后,温度升高达到该可燃物的着火点时,在氧气充足的情况下,不经点火就自发燃烧起来的现象
2)爆炸:如果燃烧以极快的速率在有限的空间里发生,瞬间内累积大量的热,使气体体积急剧地膨胀,就会引起爆炸。
(二)灭火的措施
破坏燃烧的三个条件之一,就可以达到灭火的目的。
(1)清除可燃物或使可燃物与火源隔离。
(2)隔绝空气(或氧气)。
(3)使可燃物的温度降到着火点以下。

(三)促进燃烧
(1)增大氧气的浓度(氧气的浓度越大燃烧越剧烈)
(2)增大可燃物和氧气的接触面积(接触面积越大燃烧越剧烈)
(四)拓展
(1)水灭火有一定范围。不能用水的如汽油、煤油、图书、精密仪器、钾钙钠等金属、高压电器。
(2)油库着火不能用水灭火,因为油的密度比水小。不太严重可用干粉灭火器或沙子来灭火。
(3)当电器或电线燃烧着火时,应先切断电源,再用干粉灭火器或沙子来灭火,不能用水。
考点五 化学反应基本类型

(一)化合反应和分解反应
(1)化合反应:把由两种或两种以上的物质生成一种物质的反应叫做化合反应。如
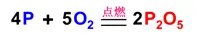
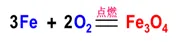
(2)分解反应:由一种物质生成两种或两种以上的物质的反应叫做分解反应。如
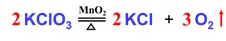
(二)复分解反应
1、概念:两种化合物互相交换成分生成两种新化合物的反应(通式表示为AB+CD→AD+CB )。
2、特点:复分解反应交换成分,但反应前后各元素的化合价不变。
3、复分解反应发生的条件
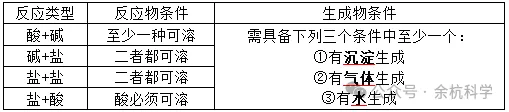
4、复分解反应实质:发生复分解反应的两种物质在水溶液中相互交换离子,结合成难电离的物质-沉淀、气体和水。