(点击查看详情)
中考生物知识点汇总
【中考复习】生物专题知识点①:构成生物体的细胞、组织、器官和系统
【中考复习】生物专题知识点③:种群、群落、和生态系统及生物圈
中考化学考点汇总
备考指南

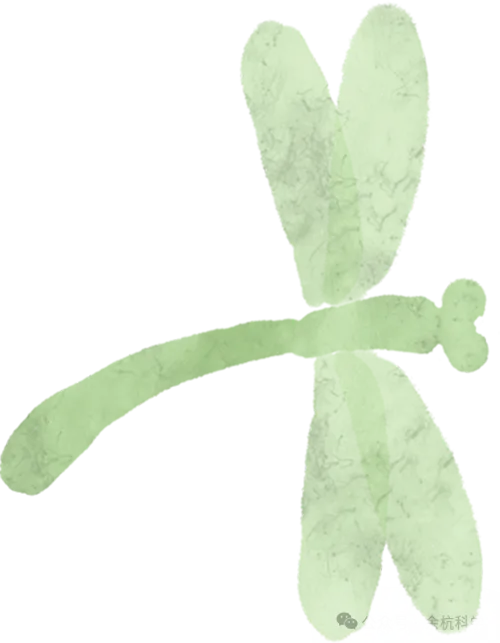
知识导图

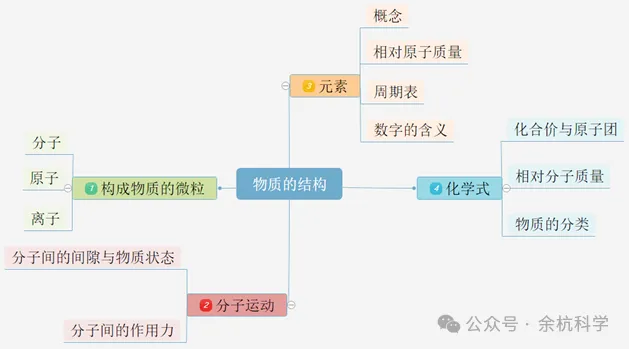
考点梳理

考点一 分子、原子、离子

一、 分子之间存在空隙
(一)实验一:水和酒精混合
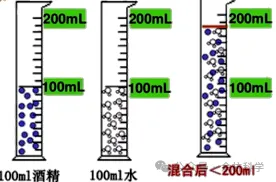
①实验现象:水和酒精混合后的总体积小于水和酒精的体积之和。
②解释:水分子之间和酒精分子之间存在着空隙,当水和酒精混合时,水分子和酒精分子彼此进人对方分子的空隙中,所以水和酒精混合后的总体积会减小。
(二)实验二:芝麻和黄豆混合
①实验现象:芝麻和黄豆混合后的总体积小于混合前的体积之和。
②解释:黄豆与黄豆之间存在空隙,一部分芝麻钻到了黄豆之间的空隙中。
结论:不论固体、液体还是气体,构成物质的分子(或微粒)之间都有一定的空隙,不同物质分子(或微粒)间的空隙大小不同,固体的最小,液体的次之,气体的最大。
二、分子处于不停的运动之中
(一)扩散现象
(1)现象探究:一瓶是(无色)空气,一瓶是二氧化氨(红棕色),用玻璃板隔开。
抽去玻璃板,使两个瓶口相互贴紧,将会看到没有颜色的那瓶气体变红了,两瓶气体的颜色最后变得均匀。这就是气体的扩散现象。将红墨水注人水中,一段时间后,水会变红,这是液体的扩散现象。扩散现象还能在固体中发生,如把磨得很光滑的铅片和金片紧压在起,5年后,将它们切开,发现它们互相渗入约1毫米深。
(2)概念:不同物质的分子彼此进人对方分子空隙中的现象叫做扩散。
(3)扩散现象表明:
①构成物质的分子都在不停地做无规则运动。
②构成物质的分子间存在空隙。(二)扩散快慢与温度的关系
温度越高扩散越快,说明分子的运动越剧烈。因为分子的运动与温度有关,所以分子永不停息的无规则运动也叫做热运动。
三、分子之间的引力和斥力
(一)构成物质的分子间存在相互作用的引力和斥力
(1)构成物质的分子之间(物体内部)存在引力。
分子间的相互引力像一只只无形的手,将分子与分子聚集在一起,构成各种固体和液体。不但物体内部的分子之间存在着引力,两个物体接触面上的分子之间(不同物体之间)同样存在着相互作用的引力。
(2)构成物质的分子之间存在斥力。
构成物质的分子之间存在空隙,很难将其压缩是因为分子之间存在着相互作用的斥力。(二)物质三态的分子结构及宏观特征对比
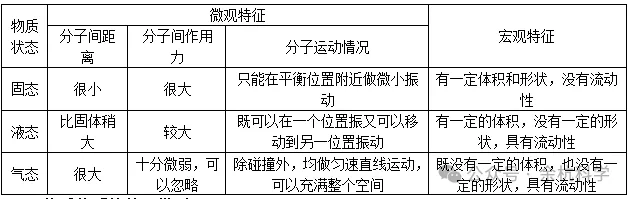
二、构成物质的粒子模型
(1)现在已知的原子有几百种。不同种类和不同数量的原子就能构成不同的分子。构成分子的原子可以是同种原子,也可以是不同种原子
(2)分子在化学变化中是可分的,而原子是不可分的。在电解水时,水分子变成了氢分子和氧分子,它们不再保持水的化学性质。可见,在由分子构成的物质中,分子是保持物质化学性质的最小粒子
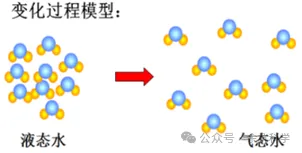
(3)粒子模型可以示意物质变化
①水的汽化是物理变化:水分子之间的距离变大,分子种类不变。
②水的电解是化学变化:分子种类改变,原子的种类和数目不变。
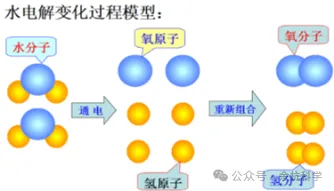
(4)物质通常是由分子构成的,但也有些物质是直接由原子构成的,如:金属铝由铝原子构成,石墨由碳原子构成。
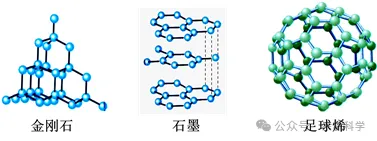
(5)电解水过程的模型相关的信息
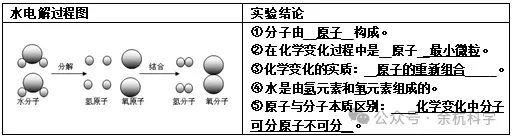
三、粒子的大小与质量
(1)分子和原子的质量和体积都很小。原子半径一般在 10-10米数量级,如碳原子的半径为0.6×10-10米。一个碳原子的质量约为1.993×10-26千克。不同种类的分子和原子,质量是不同的。
(2)原子不一定比分子小。分子与构成该分子的原子相比,分子比原子大,如:氧分子一定比氧原子大;但不同种类的分子与原子相比,则分子有可能比原子小,如:氧分子就比汞原子小。
(3)分子与原子的比较

四、原子结构模型的建立
(一)原子结构模型的建立过程
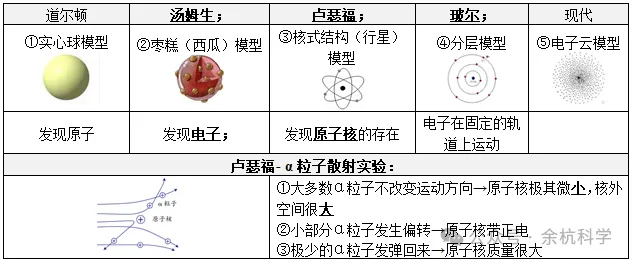
(二)原子的结构
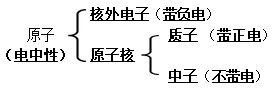
(1)原子由原子核和核外电子构成。原子核带正电荷,居于原子中心;核外电子带负电荷,在核外空间做高速运动。
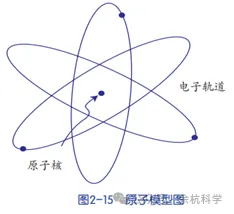
(2)原子核相对原子来说,体积很小,但质量却很大,它几乎集中了原子的全部质量。由于原子核和核外电子所带的电量大小相等,电性相反,所以整个原子呈电中性。
(3)氦原子的原子核带两个单位正电荷,核外有两个带负电的电子围绕原子核做高速运动,如图所示。
五、揭开原子核的秘密
(1)用高能量的粒子撞击、打碎核的方法是研究微观粒子结构的一种方法。
(2)原子核是由两种更小的粒子——质子和中子构成的。如一种氧原子的原子核就是由8个质子和8个中子紧密相连构成的
(3)一个质子带一个单位的正电荷,中子不带电,一个电子带一个单位的负电荷。如氧原子核内有8个质子,则氧原子核带 8 个单位正电荷(即+8)。科学上把原子核所带的电荷数称为核电荷数,氧原子的核电荷数为 8 。
(4)由于原子呈电中性,根据原子中各微粒的电性及电荷量可知:原子中,核电荷数=质子数=核外电子数。
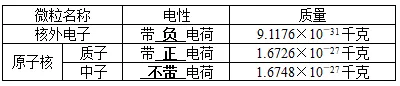
(6)质子和中子都是由更微小的基本粒子——夸克构成的。
六、带电的原子——离子
(一)氯化钠的生成
A、取一瓶氯气,观察它的颜色为黄绿色。
B、用镊子在放有煤油的试剂瓶中夹取一块钠,用刀切割成一小块,观察到钠是一种质软、带银白色光泽的金属固体。
C、点燃钠,将燃烧匙伸入氯气瓶中,反应结束后观察瓶内的物质为白色固体。
D、实验现象:剧烈燃烧,产生光亮的黄色火焰,产生白烟,生成白色固体物质。
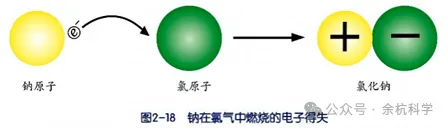
金属钠在氯气中燃烧时,钠原子失去 1个电子后形成带正电荷的钠离子(阳离子),氯原子得到1个电子后形成带负电荷的氯离子(阴离子)。带有相反电荷的钠离子和氯离子之间相互吸引,构成了电中性的氯化钠。如下图所示
★微观解释:
(1)钠原子失去一个电子成为一个带正电的微粒叫钠离子Na+。
(2)氯原子得到一个电子成为一个带负电的微粒叫氯离子 Cl—。
(二)离子
离子是带电的原子或___原子团___,带正电的叫阳离子,带负电的叫阴离子。离子也是构成物质的基本粒子,如硫酸铜就是由铜离子和硫酸根离子构成的。
阳离子:带正电的原子或原子团。例:钠离子Na+、铵根离子NH4+
阴离子:带负电的原子或原子团。例:氯离子Cl-、硫酸根离子SO42-
(三)原子、分子和离子的区别和联系
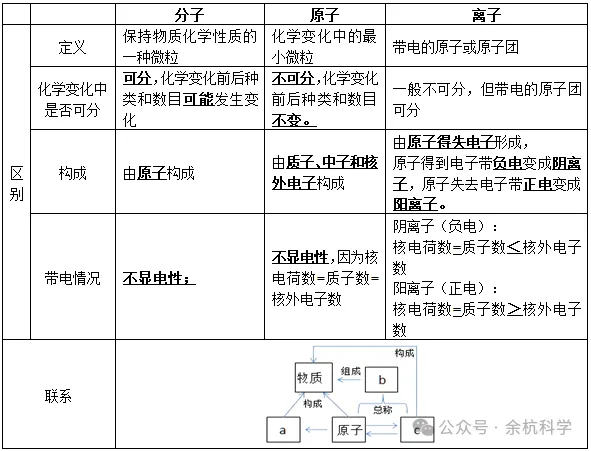
(四)注意
阳离子的核内质子数>核外电子数;阴离子的核内质子数<核外电子数。
七、同位素——原子的“孪生兄弟”
(1)科学上把具有相同核电荷数(即质子数)的一类原子总称为元素。如:氧元素就是所有核电荷数为 8 的原子的总称。
(2)原子核内的质子数相同、中子数不相同的同类原子互为同位素原子。元素是互为同位素的原子的总称。大多数元素都有同位素,如汞元素有7种稳定的同位素。
(3)同位素原子的两种表示方法
①常用原子符号(X)表示,其中X表示原子种类,Z表示质子数,A表示质子数与中子数之和。如氢有氕(H)、氘(H)、氚(H)三种同位素原子。
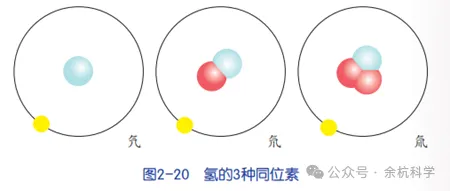
②也可以用“原子名称(或符号)-质子数与中子数之和”来表示。如氧的三种同位素原子分别为氧-16(O-16)、氧-17(O-17)、氧-18(O-18)。
(4)同位素的应用
1)质谱分析中,用稳定同位素原子作为示踪原子;
2)核潜艇利用铀的同位素裂变释放的能量作为动力;
3)利用放射性同位素对一些脏器进行扫描,诊断肿瘤等疾病;
4)根据放射性同位素的半衰期,进行古董鉴定。
根据元素的定义可知,不同元素之间最本质的区别是核电荷数(即质子数)不同。
八、相对原子质量
(1)原子的质量极小,计算起来极不方便。为此,国际上规定采用相对原子质量来表示原子的质量关系。
(2)相对原子质量的概念:把一个碳-12 原子的质量分为 12 等份,则1份质量为
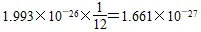
千克。其他原子的质量与1.661×10-27千克质量相比后得出一定的比值,这个比值就是该原子的相对原子质量。
(3)相对原子质量的计算式:
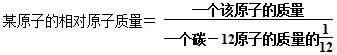
(4)原子的质量与相对原子质量的区别和联系如下表所示:
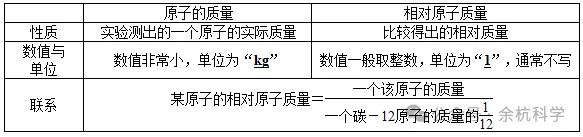
九、相对分子质量
(1)一个分子中各原子的相对原子质量总和就是该分子的相对分子质量。
(2)求物质的相对分子质量,首先要写出正确的化学式,再利用相对原子质量表,查出各元素的相对原子质量,最后根据分子中各元素的相对原子质量总和求出相对分子质量。
(3)相对分子质量计算的注意事项
①元素符号与其右下角数字之间在计算相对分子质量时需用“×”,元素符号之间在计算相对分子质量时需用“+”。如CO2的相对分子质量= 12+16×2 =44。
②原子团括号外右下角的数字表示原子团的个数,应先将原子团内各原子的相对原子质量之和计算出来,再乘以其个数。如Al2(SO4)3的相对分子质量= 27×2+(32+16×4)×3 =342。
③结晶水合物中的“·”表示结合的含义,在计算相对分子质量时应将“·”前后两部分的相对分子质量相加而不是相乘。如CuSO4·5H2O的相对分子质量= 64+32+16×4+5×(1×2+16) =250。
④相对分子质量与相对原子质量一样,也是一个比值,其单位也是“ 1 ”,通常不写。
(4)相对分子质量是一个定值,只要知道物质的化学式,就可以计算出它的相对分子质量。
十、元素质量分数和质量比的确定
(一)计算组成物质的各元素的质量比
(1)计算依据:化合物中各元素的质量比等于各元素相对原子质量乘以其原子个数的乘积的比值。
(2)计算注意事项
①元素只讲种类,不讲个数,因此在计算格式的书写上有严格的规定,如计算硝酸铵(NH4NO3)中各元素的质量比,不能写成2N∶4H∶3O,也不能写成N2∶H4∶O3,应该写成m(N)∶m(H)∶m(O)=(14×2)∶(1×4)∶(16×3)= 7∶1∶12 。
②检查各原子的原子总数,如硝酸铵(NH4NO3)中氮元素的原子总数是 2 而不是1,不要遗漏。
③不要把原子个数比当作是元素的质量比。原子个数比是元素符号右下角的数字之比,如H2O中,氢元素与氧元素的原子个数比为 2∶1 ,而氢元素与氧元素的质量比为(1×2)∶(16×1)= 1∶8 。
(二)计算物质中某元素的质量分数或质量
(1)化合物中某元素的质量分数=

(2)化合物中某元素的质量=化合物的质量×化合物中该元素的质量分数。
(三)不纯物质中,计算某一元素的质量。
元素的质量=不纯物质量x该物质的质量分数x纯物质中该元素的质量分数
例:现有含氧化铁80%的铁矿石500吨,问最多可冶炼出铁多少吨?
解:氧化铁的质量 =500吨×80% =400吨
铁元素的质量 =400吨×70%=280吨
考点二 元素

一、元素的种类
(1)目前人类已知的元素有 110 多种,其中有些是人造元素。世界上大部分物质只是由几十种常见元素组成的,其中仅碳、氢、氧三种元素就能组成许许多多种物质。
(2)人们通常把元素分为金属元素和非金属元素(包括稀有气体元素,如氩元素)。在110多种元素中,金属元素占大多数
(3)物质的分类
A.物质的分类:

B.纯净物的分类:
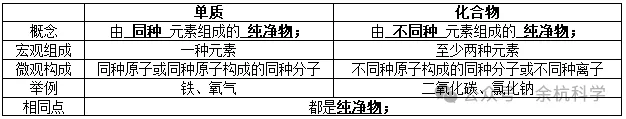
C.氧化物:由两种元素组成的,其中一种是氧元素的化合物。
D.由一种元素组成的物质不一定是单质,可能是混合物。例:氧气和臭氧的混合物,都由氧元素构成。
二、元素的分布
(1)地壳主要由氧、硅、铝、铁、钙、钠、钾、镁、氢等元素组成,其中含量最高的是氧,其次是硅。金属元素中含量最高的是铝,其次是铁。
(2)人体中的元素及作用
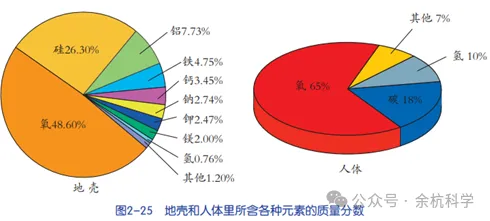
①人体内大约含有30多种元素,其中 11 种为大量元素,约占99.95%,其余为微量元素。它们中有些是必需元素,每一种必需元素在体内都有一个适量范围,过多或过少都不利于人体健康。另外,人体内也含有一些有害元素,如镉、汞、铅等。
②人体含量最高的元素是氧元素,含量最高的金属元素是钙元素。
③钙元素能促进儿童骨骼生长;铁元素能预防贫血;碘元素能预防甲状腺肿大;氟元素能预防龋齿;锌元素能增进食欲,促进儿童的生长发育;硒元素能预防癌症。
(3)海水中,除了水由氢、氧两种元素组成以外,含量较高的是氯元素、钠元素和镁元素,还有一些贵重金属,如金等
(4)有机化合物中大都含有碳、氢、氧三种元素。
(5)人造元素是通过核反应制得的,其中有些人造元素和天然元素具有放射性。放射性元素对人体有害,但利用放射性可以检查和治疗一些疾病、灭菌和消毒。
(6)元素与原子的区别和联系
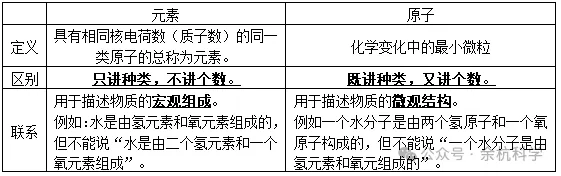
举例:水的结构和组成正确说法
A、水是由大量的水分子构成的。
B、一个水分子是由两个氢原子和一个氧原子构成的。
C、水是由氢元素和氧元素组成的。
三、元素符号
(1)元素符号的写法
A、通常用该元素拉丁文的第一个字母的大写来表示,如H、O、N等。
B、当两种元素的第一个字母相同时,可写上该元素名称的第二个字母(小写)以示区别,如Na、Mg、Cu等。
(2)元素符号的意义
①表示一种元素【宏观】。如H可表示氢元素;
②若物质是由原子直接构成的,还表示一种物质,如Cu可表示铜这种物质。
③表示这种元素的1个原子【微观】,如H还可表示一个氢原子。
④如果在元素符号前面加上数字,则表示某元素的若干个原子。如3H表示 3个氢原子。
元素符号本身既有宏观含义——表示某种元素,又有微观含义——表示该元素的1个原子。但当元素符号前面有数字时,则只有微观含义,只能表示几个某原子,不再具有宏观含义。故“2N”只能表示“两个氮原子”。
(3)元素符号周围数字的意义
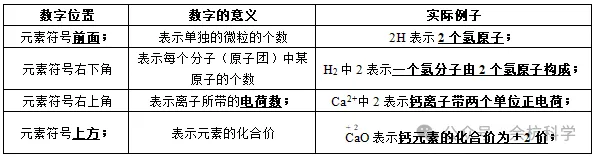
四、元素周期表
(1)根据元素的原子结构和性质,科学家把人们已知的110多种元素按原子序数科学有序地排列起来,得到的表叫做元素周期表。
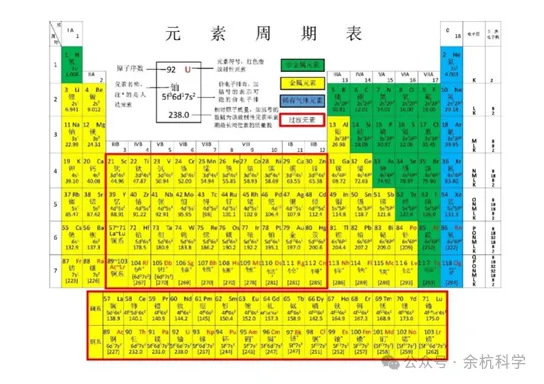
(2)元素周期表的每一个横行叫做一个周期,表中共有7个横行,表示有 7 个周期。每个周期由金属元素开头(第一周期除外),过渡到非金属元素,最后以稀有气体元素结尾。同一周期从左到右,元素原子的核电荷数逐渐增加。同一周期电子层数相同。
(3)元素周期表的每一个纵列叫做一个族,元素周期表中共有18个纵列, 16 个族(其中第8、9、10三个纵列共同组成一个族)。同族元素的化学性质相似。同族最外层电子数相同。
(4)在元素周期表中,每一种元素都占有一格位置,每一格包括元素的原子序数、元素符号、元素名称、相对原子质量(将在本章第7节学习)等内容(如下图所示)。
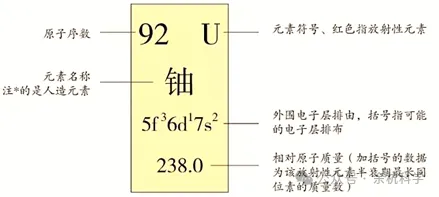
注意:在元素周期表中同位素占同一个位置。
(5)元素周期表的应用:元素周期表是学习和研究科学的重要工具。我们可以从元素周期表中获得有关元素的许多信息,如元素单质的物理状态;元素是人工合成的还是自然存在的;元素是金属、非金属还是稀有气体等。