(点击查看详情)
【中考复习】生物专题知识点①:构成生物体的细胞、组织、器官和系统
【中考复习】生物专题知识点③:种群、群落、和生态系统及生物圈

备考指南
考点分布 | ||

知识导图
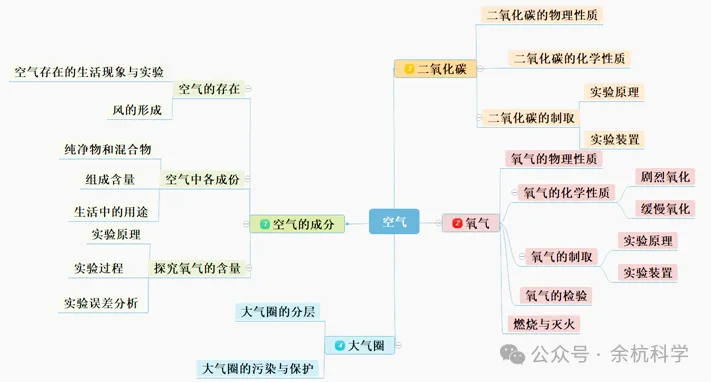

考点梳理
考点一 空气、空气污染

一、空气的成分
气体 | 含量 | 性质 | 用途 |
氧气(O2); | 21%; | 性质较活泼的气体 | 1.供给呼吸;2.帮助燃烧; 3.燃料在氧气中燃烧后产生的高温火焰可用来切割或焊接金属 |
氮气(N2); | 78%; | 无色、无味、性质较不活泼的气体。 | 1.充入灯泡中,延长灯泡的使用寿命; 2.充入食品装包袋防腐,保鲜。 3.制造化肥、炸药的重要原料。 4.用作致冷剂,医疗上常用液氮冷冻麻醉或冷藏人体细胞组织 |
稀有气体 | 0.93% | 化学性质不活泼,又称惰性气体。 | 1.霓虹灯内充气,稀有气体通电后能发出不同颜色的光 2.激光技术,制造低温环境(氦气)用于医疗麻醉(氙气)等 |
二氧化碳 | 0.04% |
|
二、空气中氧气含量的测定
(1)装置图:
(2)实验步骤:
1)按图把装置连接,先在广口瓶内加入少量水,再把剩余的容积用记号划成5等份。
2)点燃燃烧匙内的红磷,立即塞紧瓶塞,观察现象。
3)火焰熄灭后,振荡广口瓶,打开导管上的夹子,观察现象。
(3)实验现象:
A、红磷燃烧,放出热量,有大量白烟产生。
B、待集气瓶冷却后,打开止水夹,水经导管进入集气瓶,约占集气瓶内空气总体积的1/5。
C、水经导管倒流进入集气瓶,消耗的气体跟剩下的气体的体积比为1 : 4
(4)实验结论:空气中氧气的体积约占空气总体积的1/5。
(5)化学方程式:4P + 5O2=点燃=2P2O5;
(6)注意事项:
a.装置的气密性要好,(否则测量结果偏小);
b.所用的红磷必须过量,过少则氧气没有全部消耗完,会导致测量结果偏小;
c.要等集气瓶(装置)冷却后才能打开弹簧夹,(否则测量结果偏小);
d.在实验前,导管应预先注满水,(否则测量结果偏小)
e.要先夹住橡皮管,然后再点红磷(否则测量结果偏大);
f.点燃红磷伸入瓶中要立即塞紧瓶塞(否则测量结果偏大)。
(7)此实验说明剩余气体有哪些性质:
①不燃烧也不支持燃烧 。②不溶于水。
(8)其他实验方法:
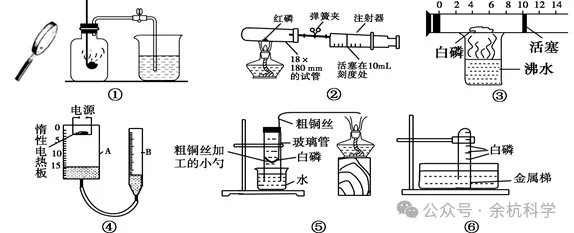
注意:不能用木炭、硫或铁丝来代替红磷!
理由:木炭和硫燃烧会生成气体,铁丝在空气中燃烧。
三、温室效应与臭氧层破坏等环境问题
(1)大气中的二氧化碳具有与温室玻璃相似的作用,对地球起着保温作用,大气中二氧化碳的含量增加 ,进而导致气温 上升 ,引起“温室效应”。
(2)“温室效应”加剧的原因:大量使用化石燃料 ;森林面积因乱砍滥伐 而急剧减少等。
(3)能造成“温室效应”的气体除二氧化碳外,还包括水蒸气、臭氧、氧化亚氮、甲烷、氯氟烃、全氟碳化物及六氟化硫等,统称为温室气体。其中二氧化碳所占比例最大,约为55%。
(4)酸雨
①酸雨:pH低于5.6的酸性降水,称为酸雨。
②酸雨的形成:
降水过程中吸收并溶解空气中的二氧化硫、氮氧化物等污染物,形成硫酸(H2SO4)和硝酸(HNO3 )有害物质。
③酸雨的危害:
酸雨不仅危害健康,而且使水域和土壤酸化,损害农作物和林木生长,危害渔业,腐蚀建筑物、工业设备和文化古迹。
(5)臭氧空洞
①臭氧O3:臭氧是一种蓝色的、带有腥臭气味的气体。
②臭氧层则能阻挡和削弱过强的紫外线,对生物起到保护的作用。
③破坏臭氧层的主要物质为氯氟烃,“氟利昂”就是其中一种氯氟烃。
考点二 氧化与燃烧

一、氧化反应
(一)定义
物质跟氧发生的反应叫作氧化反应。
在氧化反应中,氧气提供氧,氧气具有氧化性。
(二)类型
①缓慢氧化:变化缓慢、短期内不易觉察只放出少量热、不发光。
例:动植物呼吸、食物腐败塑料和橡胶制品的老化、金属生锈、酒的酿造…
②剧烈氧化:变化剧烈、容易觉察。既发热、又发光。
例:燃烧、爆炸……
二、燃烧
(1)燃烧的概念:通常情况下,可燃物与氧气发生的一种发光、放热的剧烈的氧化反应叫作燃烧。
(2)燃烧的必要条件(燃烧三要素,缺一不可):可燃物、有助燃剂(氧气)、温度达到着火点。
(3)影响燃烧的因素
1)可燃物不同,性质不同,燃烧现象不同。
2)氧气浓度越大,燃烧越剧烈。
3)可燃物与氧气的接触面积越大,燃烧越剧烈。
(4)可燃物的着火点:物质燃烧所需达到的最低温度叫着火点
不同物质的着火点是不同的。
已知白磷的着火点是40℃,红磷的着火点是240℃。

(5)自燃与爆炸
1)自燃:由于缓慢氧化产生的热量被积累后,温度升高达到该可燃物的着火点时,在氧气充足的情况下,不经点火就自发燃烧起来的现象
2)爆炸:如果燃烧以极快的速率在有限的空间里发生,瞬间内累积大量的热,使气体体积急剧地膨胀,就会引起爆炸。
考点三 氧气与二氧化碳的性质

一、氧气的性质
化学式 | O2 |
物质分类 | 非金属单质 |
结构 | 由氧分子构成,每个氧分子由两个氧原子构成的。 |
物理性质 | 1、氧气是一种无色无味的气体。 2、溶解性:不易溶解于水。 3、密度:比空气密度大。 4、低温下液化成淡蓝色的液体或凝固成雪花状的蓝色固体。 |
化学性质 | 1、供给呼吸 2、支持燃烧(助燃剂) |
1、一些物质在氧气中燃烧
物质(颜色、状态) | 反应现象 | 注意事项及化学方程式 |
硫粉(淡黄色) | a.在空气中:发出微弱的淡蓝色火焰,生成一种有刺激性气味的气体 b.在氧气中:发出明亮的蓝紫色火焰,生成一种带有刺激性气味的气体 | 要在瓶底装少量水(目的:吸收二氧化硫, 防止污染空气) S+O2=点燃=SO2 |
铁丝(银白色金属) | a.在空气中:不燃烧 b.在氧气中:剧烈燃烧,火星四射,放出热量,生成一种黑色固体。 | 瓶底装有少量水或铺上一层细沙(目的:防止溅落的融化物使瓶底炸裂) 3Fe+2O2=点燃=Fe3O4 |
红磷( 暗红色固体) | a.在空气中:发出黄色火焰 b.在氧气中:剧烈燃烧,发出白光,放出热量,产生大量的白烟。 | 反应生成的是固体小颗粒,现象应描述为白烟,而不是白雾(指小液滴)。 4P+5O2=点燃=2P2O5 |
木炭 (灰黑色固体) | a.在空气:不燃烧,发出红光 b. 在氧气中:剧烈燃烧,发出白光,放出热量,生成一种能使澄清石灰水变浑浊的气体。 | C+O2=点燃=CO2 |
二、二氧化碳的性质
(1)物理性质:无色无味的气体,密度比空气大,能溶于水,加压降温可变成无色液体,甚至变成雪状固体(干冰),干冰易吸热升华;
(2)化学性质:
①通常不燃烧,也不支持燃烧
②不能供给呼吸;
③与水反应:H2O+CO2===H2CO3(不稳定)
④与石灰水反应:Ca(OH)2+CO2===CaCO3↓+H2O
(3)二氧化碳的用途
①二氧化碳用于灭火:二氧化碳既不能燃烧也不支持燃烧,密度比空气大。
简易酸碱灭火器工作原理:
Na2CO3+2HCl=2NaCl+CO2↑+H2O
Na2CO3+H2SO4=Na2SO4+CO2↑+H2O
②二氧化碳作气肥,用于光合作用:植物的光合作用需要大量的二氧化碳,因此可把二氧化碳作为气体肥料,提高光合作用的强度和效率。
③二氧化碳也是一种工业和食品原料:可用于制纯碱(Na2CO3)、尿素和汽水。
④制冷剂:干冰(固体二氧化碳)可用于人工降雨。
考点四 实验室制取二氧化碳和氧气的方式

一、实验室里制取氧气的方法
分解双氧水H2O2和加热分解高锰酸钾KMnO4或氯酸钾KClO3,化学方程式为:
(1)2H2O2=MnO2= 2H2O + O2 ↑
(2)2KMnO4=△=K2MnO4 + MnO2 + O2↑
(3)2KClO3=MnO2=2KCl + 3O2↑。
固体加热型 | 固液(液液)不加热型 | |||
发生装置 | 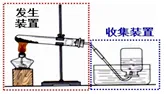 | 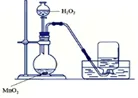 | ||
实验步骤 | 查→装→定→加→收→验 | 查→装→定→点→收→离→熄; | ||
①查:检查装置的气密性注意安装顺序:先从下到上,后从左到右。 ②装:装入药品 ③定:固定试管 ④点:点燃酒精灯 ⑤收:用排水法收集 ⑥离:将导管移离水面 ⑦熄:熄灭酒精灯。 【谐音记忆: “茶-庄-定-点-收-利-息”】 | ||||
排水法 (不易溶于水) | 向上排空气法 (密度比空气大) | 向下排空气法 (密度比空气小) | ||
收集装置 | 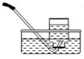 |  | 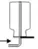 | |
优点 | 较纯净; | 较干燥; | ||
缺点 | 含较多的水蒸气; | 不够纯净; | ||
验满方法 | 1.将带火星的木条放在集气瓶口,木条复燃(排气法) 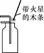 2.集气瓶口出现大气泡(排水法) 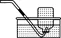 | |||
检验方法 | 将带火星的木条放在集气瓶中,木条复燃
| |||
注意 | 长颈漏斗末端要伸到液面以下(分液漏斗则不必) | ①试管口略向下倾斜;②试管夹夹在离试管口1/3处;③实验完毕,先移出导气管,再熄灭酒精灯;④用KMnO4制O2时,试管口放一团棉花; | ||
注意:
(1)在过氧化氢和氯酸钾制取氧气的反应中,用二氧化锰作为催化剂,它的作用是改变反应速度,本身的质量和化学性质在反应前后都不变。
a)催化剂不一定加快反应速率,也有减慢反应速率。
b)催化剂的物理性质在反应前后可以改变。但化学性质和质量不变
c)催化剂在反应中可以参与反应而发生变化,但反应结束时又能转化回原来的物质。
d)催化剂只影响反应速率,不影响最终产量。
e)催化剂在反应中起催化作用。同一反应可采用多种催化剂。
(2)为什么在试管口要放一团棉花?防止高锰酸钾粉末进入导管。
(3)为什么试管口要略向下倾斜?防止试管口的冷凝水倒流入试管底而使试管破裂。
(4)为什么要来回移动酒精灯使试管受热均匀?防止试管受热不均而破裂。
(5)为什么刚出现气泡时不能立即收集?为了排尽试管内的空气,防止收集的氧气不纯。
(6)什么时候才可以开始收集气体?气泡连续、均匀地放出。
(7)集满氧气后,为什么要先从水槽中移出导管,再熄灭酒精灯?防止水槽中的水倒吸入试管而使试管破裂。
(8)为什么导管不能伸入试管太长?有利于试管内空气排出。
(9)为什么加热前,试管外壁要保持干燥。加热时,用酒精灯的外焰加热,灯芯不能 碰到试管。结束时,热的试管不能立即用冷水冲洗? 防止试管破裂。
(二)装置的改进与评价:
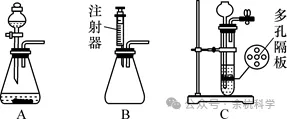
(1)将固液常温型装置中的长颈漏斗换成分液漏斗或注射器(如图A、图B所示),改进后装置的优点是通过控制液体的滴加速度,从而控制反应速;
(2)C装置的优点是能随时控制反应的发生和停止。
总结:相比于高锰酸钾或氯酸钾,实验室用过氧化氢溶液和二氧化锰制取氧气的优点是可随时添加液体、反应不需要加热、操作简便等。
(三)检查装置气密性的常见方法
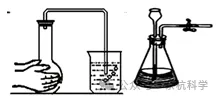
A. 手捂(加热)法:将导管的出口浸入水中,手握试管等容器,如果有气泡从导管口逸出,放手后导管末端形成稳定的水柱,表明装置气密性良好。
B. 液差(注水)法:从漏斗注入一定量的水,使漏斗下端浸没,塞紧橡皮塞,夹紧弹簧夹后,继续加水,使漏斗管内的液面高于瓶内液面,停止加水观察。液面差不变,表明装置气密性良好。
(四)固体加热型实验装置易错处(图为错误示范):
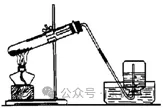
1)试管口应略向下;
2)导管应稍露出橡皮塞;
3)酒精灯应用外焰加热;
4)铁夹应夹在离试管口1/3处
5)火焰应加热在试管底部;
6)高锰酸钾制取氧气试管口应塞棉花;
7)排水收集时导管不能太长
(五)工业上用分离空气制取氧气
空气冷冻分离法:是物理变化,只是利用各种成分的沸点不同,把氧气从液态空气中分离出来,属于物理变化。

(六)典型气体
气体 | 收集方法 | 验满方法 | 检验方法 |
氧气 | 排水法、 向上排空气法 | 将带火星的木条放在瓶口 | 将带火星的木条伸入集气瓶,木条复燃,说明是氧气 |
二氧化碳 | 向上排空气法 | 将燃烧的木条放在瓶口 | 将气体通入澄清石灰水,石灰水变浑浊,说明是二氧化碳 |
二、二氧化碳的实验室制备
(1)药品:大理石(或石灰石)CaCO3与稀盐酸。
一般不用其他药品代替的理由:不能用H2SO4代替盐酸,是因为H2SO4与CaCO3反应生成微溶的CaSO4会覆盖在大理石的表面,阻止反应的继续进行
(2) 原理:CaCO3+2HCl===CaCl2+H2O+CO2↑。
(3)制取装置如图所示:
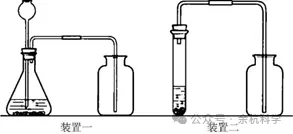
(4)收集:CO2密度比空气大、能溶于水且与水反应生成碳酸,一般只用向上排空气法收集CO2气体。
(5)操作步骤:
①. 检查装置的气密性;
②. 锥形瓶中加入大理石;
③. 连接好装置,导管口接近瓶底处;
④. 长颈漏斗中加入稀盐酸;
⑤. 用向上排空气法收集气体;
⑥. 用燃着的木条放在集气瓶口验满。
⑦. 收满盖好毛玻璃片,将集气瓶口向上放置。
(6)CO2气体的验证:将生成的无色、无味的气体通入澄清的石灰水中,若澄清的石灰水变浑浊,则该气体为CO2。反应的化学方程式为:
CO2+Ca(OH)2===CaCO3↓+H2O.
(二)二氧化碳的工业制法
(1)原料:石灰石(主要成分CaCO3);
(2)原理:CaCO3 =高温= CaO+CO2↑;
(3)设备:石灰窑
(三)实验室制取气体和收集气体的装置
发生装置 | 收集装置 | |||
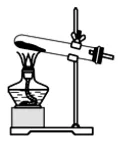 | 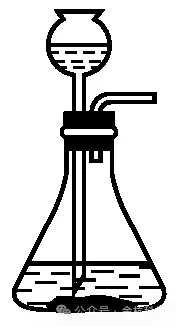 | 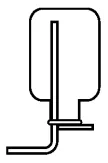 | 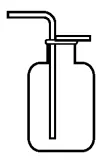 | 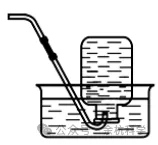 |
固体与固体反应,需加热 | 固体与液体反应,不用加热 | 密度比空气小,且不与空气中的物质反应 | 密度比空气大,且不与空气中的物质反应 | 难溶于水,不与水反应 |