初中化学中考专题——粗盐的提纯
四季读书网
15
初中化学中考专题——粗盐的提纯
我们天天都吃的食盐,首先经过盐场晒盐,只是把水分蒸发掉了,得到的是粗盐,里面还混有泥土和其他的杂质,在实验室中怎样除去杂质呢?粗盐成分:不溶性泥沙、可溶性杂质(CaCl2、MgCl2及SO42-)(1)原理:利用物质溶解性的差异,将液体与不溶于液体的固体分离的方法。(2)主要仪器:漏斗、烧杯、玻璃棒、铁架台(带铁圈)、滤纸。 (4)注意: "一贴、两低、三靠"例题1、某学生发现滴瓶中的溶液有悬浮物,拟用右图所示操作进行过滤,操作上错误的地方有
(4)注意: "一贴、两低、三靠"例题1、某学生发现滴瓶中的溶液有悬浮物,拟用右图所示操作进行过滤,操作上错误的地方有 (4)注意:a蒸发过程中要不断搅拌。b 在加热至有大量固体析出时,要用余温加热;c热的蒸发皿不能直接放在实验台上,以免烫坏实验台或遇实验台上冷水引起蒸发皿炸裂,取用它用坩埚钳。例题1、实验室进行NaCl溶液蒸发时,一般有以下操作过程:①放置酒精灯 ②固定铁圈位置 ③放置蒸发皿 ④加热搅拌 ⑤停止加热,余热蒸干。其中正确的操作顺序是( )练习2、提纯含有少量泥沙的粗盐,下列操作顺序正确的是( )原理:利用溶剂对被提纯物质及杂质的溶解度不同,使被提纯物质从过饱和溶液中析出。而让杂质全部或大部分仍留在溶液中,从而达到提纯的目的。①蒸发结晶:通过蒸发或汽化,减少一部分溶剂达到饱和而析出晶体。②冷却结晶:通过降低温度,使溶液冷却达到饱和而析出晶体。重结晶指的是重复冷却结晶(用于溶解度随温度下降而明显减小的物质)。B.加热蒸发硝酸钾溶液,开始时就会有大量硝酸钾晶体析出D.将析出硝酸钾晶体后的溶液再冷却,仍然有硝酸钾晶体析出(五)除去可溶性杂质CaCl2、MgCl2及SO42-取少量食盐,配制成溶液,先滴入几滴稀盐酸,然后向试管中滴入几滴BaCl2溶液,观察现象。实验现象:滴入盐酸后,无新现象产生,再加BaCl2溶液,则有白色沉淀生成。
(4)注意:a蒸发过程中要不断搅拌。b 在加热至有大量固体析出时,要用余温加热;c热的蒸发皿不能直接放在实验台上,以免烫坏实验台或遇实验台上冷水引起蒸发皿炸裂,取用它用坩埚钳。例题1、实验室进行NaCl溶液蒸发时,一般有以下操作过程:①放置酒精灯 ②固定铁圈位置 ③放置蒸发皿 ④加热搅拌 ⑤停止加热,余热蒸干。其中正确的操作顺序是( )练习2、提纯含有少量泥沙的粗盐,下列操作顺序正确的是( )原理:利用溶剂对被提纯物质及杂质的溶解度不同,使被提纯物质从过饱和溶液中析出。而让杂质全部或大部分仍留在溶液中,从而达到提纯的目的。①蒸发结晶:通过蒸发或汽化,减少一部分溶剂达到饱和而析出晶体。②冷却结晶:通过降低温度,使溶液冷却达到饱和而析出晶体。重结晶指的是重复冷却结晶(用于溶解度随温度下降而明显减小的物质)。B.加热蒸发硝酸钾溶液,开始时就会有大量硝酸钾晶体析出D.将析出硝酸钾晶体后的溶液再冷却,仍然有硝酸钾晶体析出(五)除去可溶性杂质CaCl2、MgCl2及SO42-取少量食盐,配制成溶液,先滴入几滴稀盐酸,然后向试管中滴入几滴BaCl2溶液,观察现象。实验现象:滴入盐酸后,无新现象产生,再加BaCl2溶液,则有白色沉淀生成。 | | |
| | Na2SO4+BaCl2=BaSO4↓+2NaCl |
| | MgCl2+2NaOH=Mg(OH)2↓+2NaCl |
| | Na2CO3+CaCl2=CaCO3↓+2NaCl |
| Na2CO3+BaCl2=BaCO3↓+2NaCl |
| Na2CO3+2HCl=CO2↑+H2O+2NaCl |
(1)BaCl2——Na2CO3——NaOH——HCl(2)BaCl2——NaOH——Na2CO3——HCl(3)NaOH——BaCl2——Na2CO3——HCl例题1、根据从草木灰中提取钾盐(碳酸钾、氯化钾、硫酸钾)的实验,填写下列空白:(2)用托盘天平(指针向上的)称量样品时,若指针偏向右边,则表示A 左盘重,样品轻 B左盘轻,砝码重 C 右盘重,砝码轻 D右盘轻,样品重(3)在进行第③步操作时,有可能要重复进行,这是由于(4)在进行第③步操作时,要用玻璃棒不断小心地搅动液体,目的是防止。例题2、在粗盐提纯的实验中,蒸发时正确的操作是( )练习1、下列是有关实验操作的步骤和做法,不正确的是( )B.实验室制取氧气完毕后,应先取出集气瓶,再取出导管,最后停止加热C.不慎将浓硫酸洒在桌上,应先用烧碱溶液中和,再用湿布抹净D.用试管夹夹持试管时,把试管夹从试管底部往上套,夹在试管中上部练习2、在粗盐的提纯实验中,用到玻璃棒的实验步骤有、、。
版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌抄袭侵权/违法违规的内容, 请发送邮件至23467321@qq.com举报,一经查实,本站将立刻删除;如已特别标注为本站原创文章的,转载时请以链接形式注明文章出处,谢谢!



 (4)注意: "一贴、两低、三靠"
(4)注意: "一贴、两低、三靠"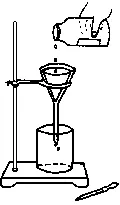
 (4)注意:a蒸发过程中要不断搅拌。b 在加热至有大量固体析出时,要用余温加热;c热的蒸发皿不能直接放在实验台上,以免烫坏实验台或遇实验台上冷水引起蒸发皿炸裂,取用它用坩埚钳。
(4)注意:a蒸发过程中要不断搅拌。b 在加热至有大量固体析出时,要用余温加热;c热的蒸发皿不能直接放在实验台上,以免烫坏实验台或遇实验台上冷水引起蒸发皿炸裂,取用它用坩埚钳。





