中考化学 | 《酸碱盐》必考知识点汇总梳理,高分必备
四季读书网
45


关注:香涛书院
一对一个性化、定制化补习的最佳选择
常见的酸有①盐酸(HCl)②硫酸(H₂SO4) ③硝酸(HNO₃)④醋酸(CH₃COOH)
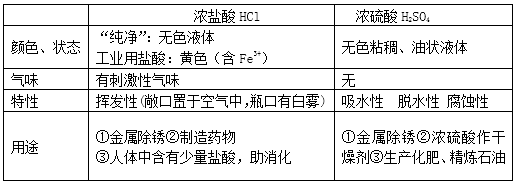
1.浓盐酸、浓硫酸的特性、用途
②活泼金属+酸→盐+氢气(注:此处酸不包括浓硫酸和硝酸)Zn+H₂SO4=ZnSO4+H₂↑ Zn+2HCl=ZnCl2+H₂↑ Fe+H₂SO4=FeSO4+H₂↑ Fe+2HCl=FeCl2+H₂↑ 2Al+3H₂SO4=Al₂(SO4)₃+3H₂↑Fe₂O₃+3H₂SO4=Fe2(SO4)₃+3H₂O3HCl + Al(OH)₃ = AlCl₃ + 3H₂O
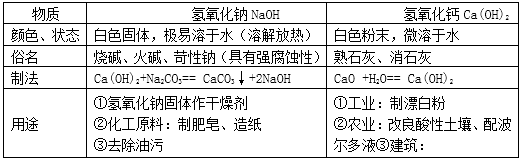
碱由离子构成,碱在水溶液中能解离出金属离子和氢氧根离子(OH-)。常见的碱有氢氧化钠(NaOH) 、氢氧化钙 Ca(OH)₂、氨水(NH₃·H₂O)等。紫色石蕊试液遇碱溶液变蓝,无色酚酞试液遇碱溶液变红。2NaOH+CuSO4=Na₂SO4+Cu(OH)₂↓盐由离子构成,组成里含有金属离子(或NH4+)和酸根离子的一类化合物。CaCO₃+2HCl=CaCl₂+H₂O+CO₂↑ Na₂CO₃+2HCl=2NaCl+H₂O+CO₂↑Ca(OH)₂+Na₂CO₃=CaCO₃↓+2NaOH(明星反应)3NaOH+FeCl₃=3NaCl+Fe(OH)₃↓CaCl₂+Na₂CO₃=CaCO₃↓+2NaCl 
复分解反应:由两种化合物(通常为酸碱盐)相互交换成分,生成另外两种化合物的反应。发生的条件:生成物中如果有↑、↓或有H₂O(稳定、难溶、难电离物质)硫酸盐不溶钡和铅;氯化物不溶银亚汞,碳酸盐只溶钾钠铵。取少量样品于试管中,滴加AgNO3溶液和稀HNO3有不溶于稀硝酸的白色沉淀生成,样品含有Cl-取少量样品于试管中,滴加Ba(NO3)2溶液和稀HNO₃有不溶于稀硝酸的白色沉淀生成,样品含有SO42- Ba(NO₃)₂+H₂SO4=BaSO4↓+2HNO₃取少量样品于试管中,滴加稀HCl,将生成的气体通入澄清石灰水有无色气体生成,该气体使澄清石灰水变浑浊,样品含有CO₃2-,取少量待检物于洁净的试管中,滴入适量NaOH溶液并加热,有使湿的红色石蕊试纸变成蓝色的气体产生。分别取少量待检液体于两支洁净的试管中,各滴入几滴BaCl₂溶液,有白色沉淀产生的原溶液是稀硫酸,无现象产生的原溶液是稀盐酸。
黑色的固体——C、CuO、Fe₃O4、FeO、MnO₂白色的固体——KClO₃、P₂O5、P(白磷)、CuSO4(无水硫酸铜)、KCl、NaCl等*白色沉淀(碱)——Mg(OH)₂、Al(OH)₃蓝色溶液——CuSO4、Cu(NO₃)₂等含Cu2+溶液浅绿色溶液——FeSO4、FeCl₂等含Fe2+溶液棕黄色溶液——FeCl₃、Fe₂(SO4)₃等含Fe3+溶液--END--
(免责声明:本文素材来源网络,由香涛书院整理,侵删。)


香涛书院特色:
1、专注初中一对一个性化、定制化辅导,与学校课程配合,展现合力的教学理念。
2、独特的5W1H教学法,独创课程体系,自主研发的紧扣考点的配套教案.
3、充分挖掘学生的学习能力,进行靶向定位的强化训练,专业授课,全程进行监督指导.
4、个性化特色教育,真正的因材施教,以学定教的课外辅导.
5、兼有线上一对一辅导课程,保证学习质量,跨越空间限制,让孩子全面提升有保障。
提分热线:
15847462008(同微信)李老师
往期精彩推荐:
免费课程 | 香涛书院分享国家中小学智慧教育平台同步视频课程
免费课程 | 香涛书院分享国家教育资源公共服务平台基础教育精品课
免费课程 | 香涛书院分享CETV同上一堂课同步、复习视频课程
中考化学 | 重点题型之物质的转化与推断解题思路及突破口
中考化学 | 2024广东省江门市中考一模试题
中考化学 | 2024湖南省初中学业水平模拟联考试题含答案
中考化学 | 2024九年级下阶段性教学质量调研试题含答案
中考化学 | 2024年3月中考化学一模测试题
中考化学 | 2023年广东省广州市中考化学真题含答案
版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌抄袭侵权/违法违规的内容, 请发送邮件至23467321@qq.com举报,一经查实,本站将立刻删除;如已特别标注为本站原创文章的,转载时请以链接形式注明文章出处,谢谢!