考试时间:60分钟满分:80分)
说明:1.本试题分为第Ⅰ卷和第Ⅱ卷两部分,共26题。第I卷为选择题,共20小题,25分:第Ⅱ卷为非选择题和附加题,共6小题,55分。2.所有题目均在答题卡上作答,在试题上作答无效。3.可能用到的相对原子质量:H-1C-12N-14O-16Na-23S-32C1-35.5Ca-40Cu-64
第Ⅱ卷 简答题(共55分)
三、非选择题(本大题共5小题,满分45分)
21. 工业烟气中常含有NOx(NO、NO2)。用NaClO溶液将NOx氧化为NO3-,实现烟气中NOx的脱除。
(1)NOx在大气中会形成酸雨。形成酸雨的过程中,NOx表现_____性。(选填“氧化”或“还原”)
(2)向NaClO溶液中加入硫酸,研究初始pH对NOx脱除率的影响,结果如下:
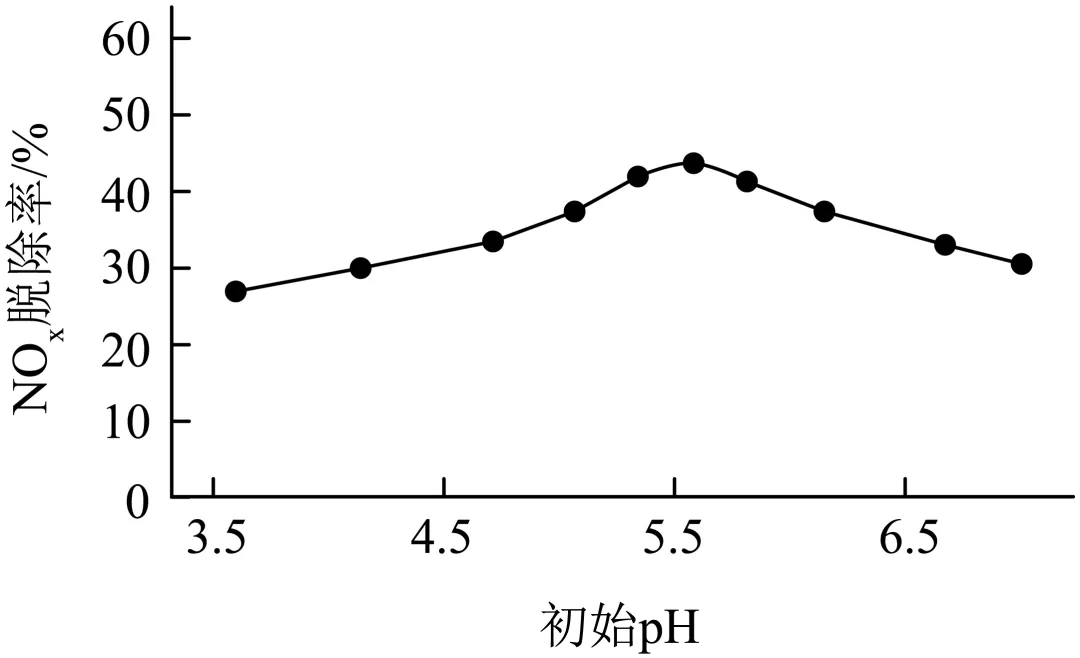
已知:NOx脱除率=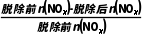 ×100%
×100%
①不用盐酸调节NaClO溶液初始pH的原因是___________。
②将pH=3.5时NaClO溶液脱除NO的离子方程式补充完整:_____NO+_____+_____=_____NO3-+_____ Cl-+_____。
③pH<5.5时,分析NOx脱除率随溶液初始pH升高而增大的可能原因:____________。
22. 三草酸合铁(Ⅲ)酸钾晶体K3[Fe(C2O4)3]·3H2O可用于摄影和印刷,在110 ℃可完全失去结晶水,继续升高温度可发生分解反应。某化学研究小组对K3[Fe(C2O4)3]·3H2O受热分解生成的气体产物进行探究。
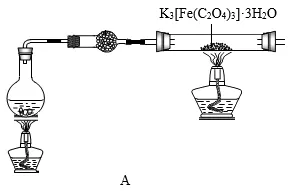
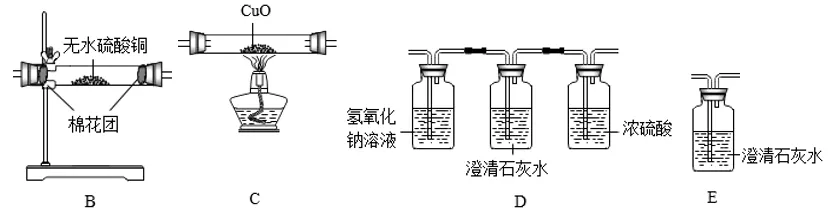
(1)实验所需的装置如上图所示,A装置烧瓶中盛有饱和NH4Cl和饱和NaNO2的混合溶液,加热可生成N2。 干燥管中盛放的试剂可以是________。
A. 无水硫酸铜B. 熟石灰C. 碱石灰D. 无水CaCl2
(2)各装置的连接顺序为:A—_______________(部分装置可重复使用) 。
(3)检查装置气密性后,先通一段时间N2,其目的是_____________。结束实验时先熄灭C处酒精灯并继续通入N2至常温,其目的是________________。
(4)D装置中澄清石灰水的作用是____________________。
(5)有同学认为该装置在实验安全方面不够严谨,并提出应该在装置末端加一个点燃的酒精灯,其目的是__________。
23. 碳酸亚铁(FeCO3)可作补血剂,某硫酸厂生产的炉渣中除了有Fe2O3、FeO,还有一定量的SiO2,兴趣小组利用炉渣尝试制备FeCO3,其流程如图所示:
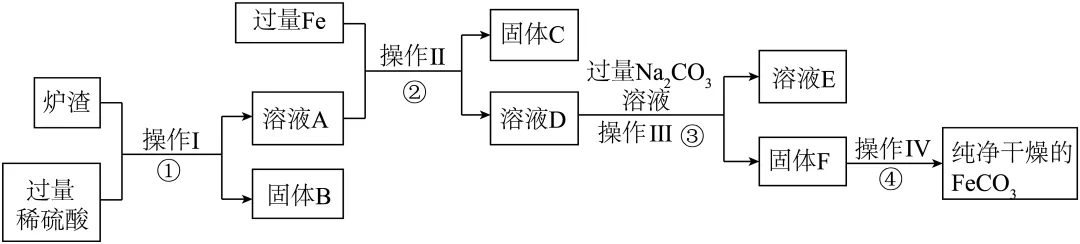
已知:SiO2不溶于水,也不与稀硫酸反应;碳酸亚铁隔绝空气加热至282℃开始分解为CO2和FeO。
(1)固体B的名称是___________,步骤①中Fe2O3发生反应的化学方程式___________。
(2)反应②的化学方程式Fe+Fe2(SO4)3=___________;操作II的名称是___________,该操作所用到的玻璃仪器有___________。
(3)步骤③反应发生的化学方程式___________。溶液E中溶质的化学式___________。
(4)操作IV包括洗涤、烘干等,其中烘干的温度不能超过282℃的原因___________。
24. 次氯酸钠(NaClO)是常用的含氯消毒剂之一,是“84消毒液”的有效成分。
【查阅资料】①有效氯含量可用来衡量含氯消毒剂的消毒灭菌能力。②次氯酸钠不稳定,易分解,会导致有效氯含量降低。
Ⅰ.探究次氯酸钠溶液稳定性的影响因素
[进行实验]
序号 | 实验操作 | 实验结果 |
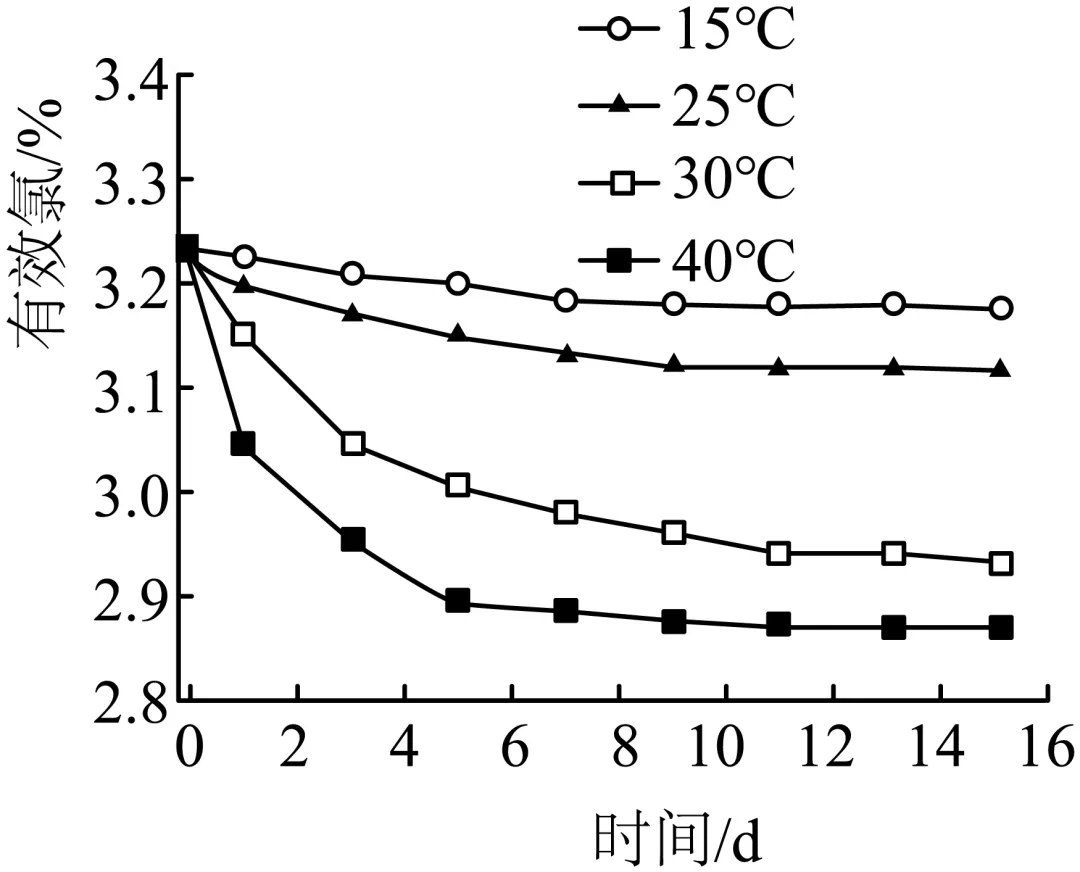
1-1 | 取相同体积、相同pH的次氯酸钠溶液,分别在温度为15℃、25℃、30℃、40℃条件下,放置15天,检测有效氯含量。 |
|
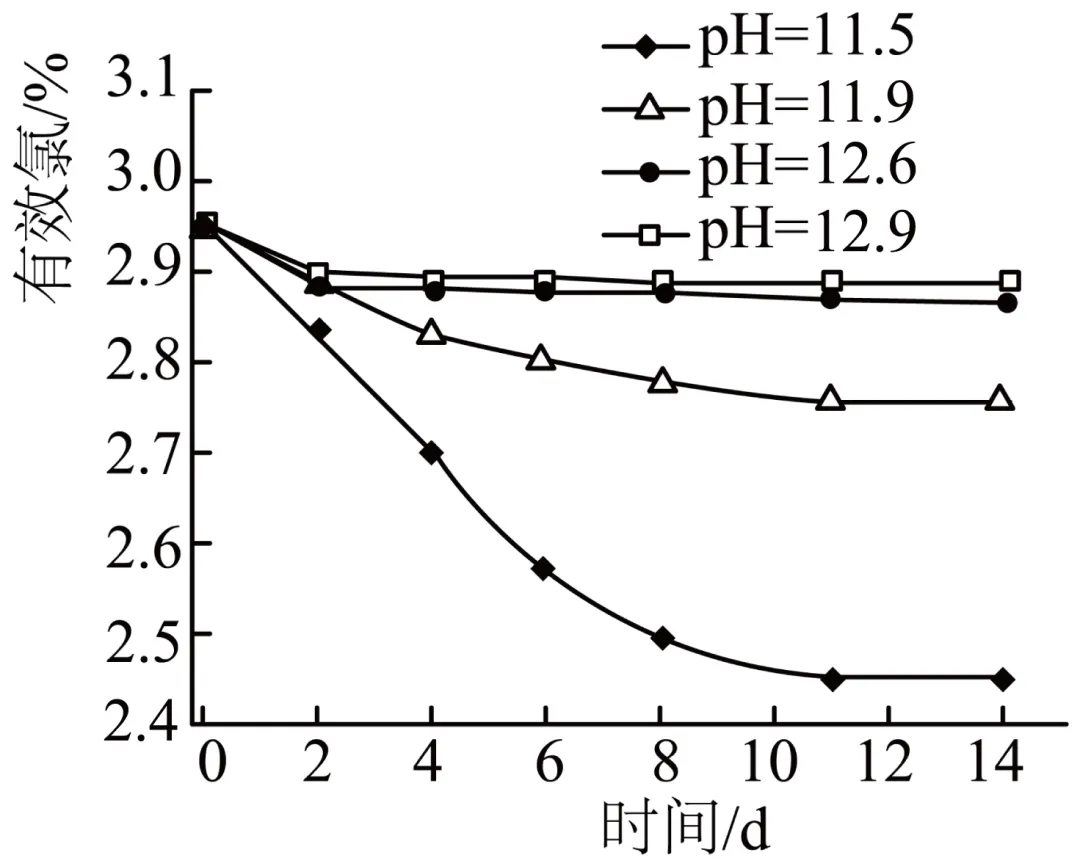
1-2 | 25℃时,取相同体积,pH分别为11.5、11.9、12.6、12.9的次氯酸钠溶液,放置14天,检测有效氯含量。 |
|
【解释与结论】
(1)用Cl2和NaOH溶液制备次氯酸钠,补全其反应的化学方程式:Cl2+2NaOH=NaClO+NaCl+________。
(2)实验1-2的目的是_______________。
Ⅱ.探究次氯酸钠溶液的灭菌效果
【进行实验】取某污水处理厂含粪大肠菌群的水样,按照①~⑤条件,用新制的次氯酸钠溶液进行实验,记录如下:
序号 | ① | ② | ③ | ④ | ⑤ | |
实验条件 | pH | 7.25 | 7.25 | 7.25 | 7.25 | 7.25 |
温度/℃ | 16.8 | 16.8 | 16.8 | 16.8 | 168 | |
接触时间/min | 5 | 5 | 5 | 12 | 30 | |
有效氯含量/(mg/L) | 2 | 5 | 8 | 2 | 2 | |
粪大肠菌群灭菌率/% | 90 | 99.87 | 99.94 | 94.99 | 99.37 |
【解释与结论】
(3)探究“接触时间是否影响灭菌效果”的实验是__________(填序号)。
(4)由实验Ⅱ可知,次氯酸钠中有效氯含量与灭菌效果的关系是__________。
[反思与评价]
(5)使用Cl2和NaQH溶液制备次氯酸钠时,需控制较低的反应温度。推测其原因是_____。
(6)在冬季水温较低时,欲提高次氯酸钠溶液的灭菌率,你的建议是__________。
25. S4N4是重要的硫氮二元化合物,室温下为橙黄色固体,178~187℃熔化并分解。实验室利用NH3和SCl2制备S4N4的装置如图所示(加热及夹持装置略)。已知SCl2易水解,熔点为-78℃,沸点为60℃。
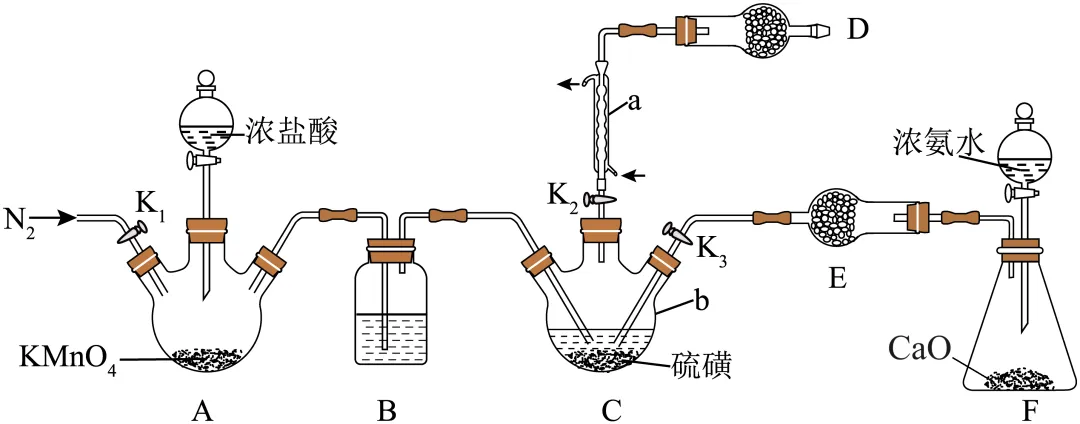
回答下列问题:
Ⅰ.制备SCl2
(1)操作步骤的先后顺序为__________。
①组装仪器并检验装置气密性,加入药品②加热装置C使其中的硫磺熔化
③通入N2,通冷凝水,一段时间后,关闭K1④打开K1、K2,关闭K3
⑤充分反应后停止滴加浓盐酸⑥向装置A中滴加浓盐酸,加热装置C至135℃左右
(2)仪器b的名称为______,装置B中盛放的试剂为__________(填试剂名称)。
(3)为使装置C受热均匀,可采取的加热方式为______,。装置D的作用为__________。
Ⅱ.制备S4N4
打开止水夹K3,向装置F中滴入浓氨水,待装置C中充分反应后停止滴加浓氨水,冷却后停止通冷凝水。
(4)生成S4N4的同时还生成一种常见固体单质和一种盐,反应的化学方程式为__________。
完整内容,请对应文本电子版。