注意事项:
1.本试卷分试题卷和答题卡两部分,试题卷共4页,满分50分,考试时间50分钟。
2.试题卷上不要答题,请用0.5毫米黑色签字水笔直接把答案写在答题卡上。答在试题卷上的答案无效。
3.答题前,考生务必将本人姓名、准考证号填写在答题卡第一面的指定位置上。
相对原子质量:H:1 C:12 N:14 O:16 Mg:24 Al:27 Cl:35.5 Fe:56 Cu:64 Zn:65
一、选择题(本题包括14个小题,每小题1分,共14分。每小题只有一个选项符合题意)
1.成语是中华文化的瑰宝。下列成语包含的物质变化中,一定发生化学变化的是
A.磨杵成针B.木已成舟C.火树银花D.滴水成冰
2.我国以玉米淀粉制备的“生物基尼龙”面料已广泛应用于日常生活,淀粉属于
A.糖类B.蛋白质C.油脂D.维生素
3.在“探究蜡烛及其燃烧”的实验中,与该实验无关的安全图标是
A.洗手B.用电C.明火D.护目镜
4.下列传统国画颜料的主要成分属于单质的是
A.朱砂(HgS)B.铅丹(Pb3O4)C.炭黑(C) D.石绿[Cu2(OH)2CO3]
5.“刀片电池”在新能源汽车领域备受瞩目,其核心成分是磷酸铁锂(LiFePO4)。已知LiFePO4中锂元素为+1价,铁元素为+2价,则其中磷元素的化合价是
A.+5B.+3C.0D.-3
某兴趣小组开展“探究土壤酸碱性对植物生长影响”跨学科实践活动,请回答6~7题。
6.下列实验操作不正确的是
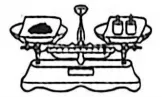
A.称量土壤样品B.溶解土壤样品C.过滤得到浸出液D.测定浸出液酸碱度
7.实验测得某土壤为弱碱性,该土壤最适宜种植的作物是(括号内为农作物适宜生长的pH范围)
A.棉花(7.0~8.0)B.茶树(5.0~5.5)
C.玉米(6.0~7.0)D.马铃薯(4.8~5.5)
8.工业上常用焦炭还原石英砂(主要成分SiO2)来制取粗硅,其反应原理为SiO2+2C 高温 Si+2CO↑,该反应属于
A.化合反应B.分解反应C.置换反应D.复分解反应
9.下列物质与氧气的构成粒子类型相同的是
A.铁B.C60C.金刚石D.硫酸铜
10.2025年诺贝尔化学奖授予发现金属有机框架(MOF)的科学家,这种新型多孔材料在储氢、捕获CO2、催化剂等领域展现巨大价值,下列有关说法不正确的是
A.该材料的应用有助于推动氢能产业发展
B.利用该材料的多孔结构,可实现混合气体的高效分离
C.该材料作为催化剂,可提高化学反应的产物产量
D.这项发现对实现碳中和具有重要意义
11.不同温度时KCl的溶解度如表所示。下列分析正确的是
温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
溶解度/ g | 27.6 | 31.0 | 34.0 | 37.0 | 40.0 | 42.6 | 45.5 |
A.20℃时,KCl的溶解度为34.0
B.30℃时,50 g水中加入20 g KCl,所得溶液质量为70 g
C.40℃时,KCl饱和溶液的溶质质量分数为40%
D.将100 g KCl溶液由60℃冷却到50℃,可能有晶体析出
12.开展跨学科实践活动中,下列做法所对应的解释正确的是
A.调查家用燃料的变迁与合理使用——将煤球变为蜂窝状,可减少CO产生
B.用轻质黏土制作水分子的模型——水是由氢原子和氧原子构成的
C.垃圾的分类与回收利用——废电池、废水银温度计属于可回收垃圾
D.微型空气质量“检测站”组装与使用——测量空气中的CO2等污染物浓度
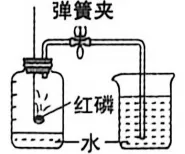
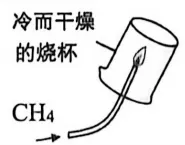
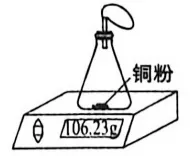
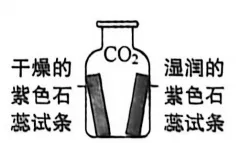
13.下列实验不能达到实验目的的是
选项 | A | B | C | D |
实验 |
|
|
|
|
实验 目的 | 探究空气中氧气的含量 | 证明CH4中含有碳元素 | 验证质量守恒定律 | 探究二氧化碳与水反应 |
14.某同学将新制的镀锌铁钉加入足量的稀硫酸中,充分反应后生成氢气0.2 g。则参加反应铁钉的质量可能是
A.4.8 gB.5.6 gC.6.0 gD.6.5 g
二、填空题(本题包括6个小题,每空1分,共16分)
15.膨化食品包装袋内常充入空气中含量最多的气体(填化学式)作防腐剂;塑料包装袋属于(填“天然”或“合成”)材料。
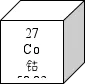
16.航天科技中,钴合金可用于制造火箭发动机部件。如图是钴元素在元素周期表中的信息,从元素分类角度,钴属于元素;据图还能获得的信息有(写出一条即可)。
17.以二氧化碳为原料生产尿素[化学式为CO(NH2)2]有助于实现碳捕集和利用,该反应微观过程如图所示。
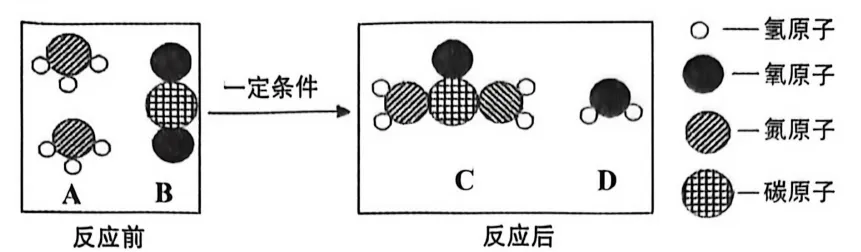
(1)尿素属于(填“氮肥”或“复合肥”)。
(2)该过程涉及的物质中,属于氧化物的有(填化学式)。
(3)参加反应的A、B的质量比为。
18.化学兴趣小组开展如图所示“酸的化学性质”主题探究活动,依据实验A可知稀盐酸能用于;若想证明实验B发生了化学反应,可先向氢氧化钠溶液中滴加试剂以便观察现象;写出实验C发生反应的化学方程式。
19.工业上利用CO还原Fe2O3炼铁,反应的化学方程式为;将3.2 gFe2O3和CuO的混合物与足量CO充分反应后,固体质量减少了0.8 g,则产生的二氧化碳质量是 g。
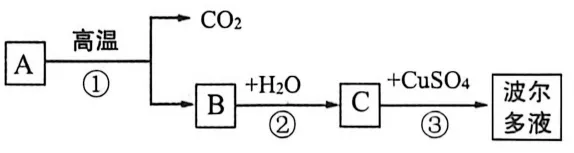 20.波尔多液的生产流程如下图所示。(“→”表示反应可一步实现,部分物质、反应条件已略去)
20.波尔多液的生产流程如下图所示。(“→”表示反应可一步实现,部分物质、反应条件已略去)
(1)物质A的化学式为______。
(2)反应②的化学方程式为______。
(3)波尔多液常用作________;反应③过程中需要搅拌,其目的是_______。
三、简答题(本题包括4个小题,共10分)
21.(2分)端午时节,粽叶飘香。吃粽子是我国端午节的习俗之一。
(1)请从分子的角度解释“粽叶飘香”所描述的现象。
 (2)粽子长途运输中常用干冰冷藏保鲜,请分析其中的原理。
(2)粽子长途运输中常用干冰冷藏保鲜,请分析其中的原理。
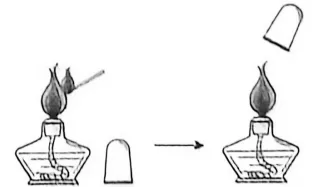
22.(2分)正确使用酒精灯的方法如图所示。
(1)用火柴点燃酒精灯,说明可燃物燃烧需满足什么条件?
(2)加热完毕,要用灯帽盖灭酒精灯,其灭火原理是什么?
23.(3分)在铝基电路板表面镀铜可提升导电性,某工厂利用Al和CuSO4溶液的反应实现该工艺。
(1)将铝片浸入硫酸铜溶液中,初期未观察到明显现象,请从铝的性质角度分析原因。
(2)对铝片表面打磨后,成功在其表面镀上一层红色物质,写出该反应的化学方程式。
(3)该镀铜过程中溶液的质量会如何变化?
24.(3分)兴趣小组利用空塑料瓶及常用仪器进行气体制取探究实验,选用装置如图所示。
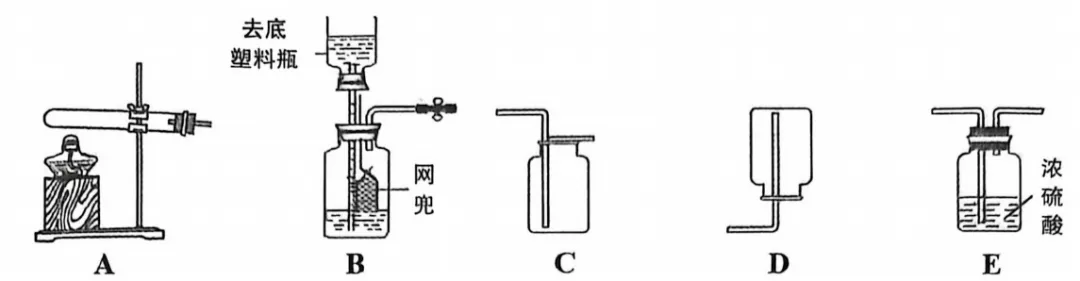
(1)写出实验室用装置A制取O2的化学方程式。
(2)该小组欲利用装置B制取干燥的CO2,所需装置从左到右的正确连接顺序为B→_____(填字母),该发生装置除了能实现废物利用外,还有什么优点?
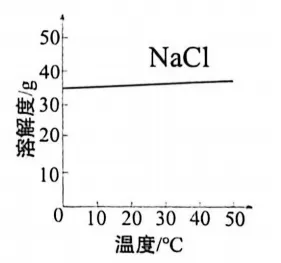
25.海洋是巨大的资源宝库,海水制盐、制氢提镁等都是对海洋资源的充分利用。(1)配制模拟海水
借助AI查询得到常温下海水中部分溶质的质量分数如下表:
溶质种类 | NaCl | MgCl2 | CaCl2 |
溶质质量分数% | 3.5 | 0.5 | 0.1 |
配制200 g模拟海水,需要氯化钠 g。配制过程中若其他操作正确,量取水时俯视读数,会使溶液溶质质量分数(填字母)。
 a.偏大 b.偏小 c.不变
a.偏大 b.偏小 c.不变
(2)海水制盐
同学们通过以下操作模拟海水制盐:取样→浓缩→结晶→提纯。
①浓缩制得粗盐过程中为什么要采用蒸发而不是降低溶液温度的方法?
②结晶后的溶液中是否含有CaCl2,可加入(写化学式)溶液来进行检验。
③提纯氯化钠时可采用什么物理方法来去除粗盐晶体中的可溶性杂质?
(3)海水制氢提镁
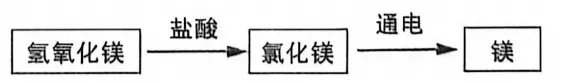 我国科研团队依靠新技术电解海水,以实现氢气和氢氧化镁量产,大幅降低氢气生产成本。
我国科研团队依靠新技术电解海水,以实现氢气和氢氧化镁量产,大幅降低氢气生产成本。
①写出电解水制取氢气的化学方程式。
②新工艺电解海水时使用特制“不粘锅”电极,电解时产生的副产物氢氧化镁不会沉积在电极上从而使电解持续进行。将氢氧化镁从海水中分离后表面仍含有少量氯化钠,可用反复冲洗除去。将氢氧化镁加入稀盐酸中可制取氯化镁,其反应的化学方程式为。
③电解熔融氯化镁可以制取金属镁,反应的化学方程式为MgCl2通电Mg+Cl2↑,若通过该反应制取4.8 t的镁,理论上需要MgCl2的质量是多少?