关注公众号,再添加微信“Cxfz1972”获取更多化学资源
文章末尾有更多资源链接
丹东市2026年中考适应性测试
化学试卷
(本试卷共14小题满分50分化学和物理考试时长共150分钟)
考生注意:所有试题必须在答题卡指定区域内作答,在本试卷上作答无效
可能用到的相对原子质量:C-12H-10-16Na-23
第 一 部 分选择题(共10分)
本部分包括10小题,在每小题给出的四个选项中,只有一项符合题目要求。
1.下列做法符合绿色化学理念的是
A. 减少使用一次性塑料制品
B. 废旧电池深埋地下
C. 大力推广使用火力发电
D. 工业烟尘高空排放
2. 空气是一种宝贵的自然资源。人体吸入空气主要是利用其中的
A.O₂B.N₂
C.CO₂D.H₂O
3.用质量分数为6%的NaCl 溶液(p=1.04g/mL)配制50g 质量分数为3%的NaCl 溶液。下列 仪器中需要用到的是
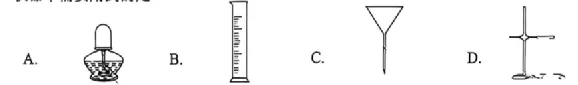
4.2026年丹东投入重大项目推进清洁能源使用。下列属于新能源的是
A. 煤B. 石油
C. 风能D. 天然气
5. 将一定量的氧气置于密闭容器中加压降温,可以得到淡蓝色液体。下列说法正确的是
A. 氧分子的体积减小
B. 氧分子数目减少
C. 氧分子之间间隔变小
D. 氧分子质量减轻
6.绿色植物通过光合作用将空气中的CO₂和H₂O 转化为葡萄糖(C₆H₁₂O₆),同时生成O₂。 下列有关说法正确的是
A. 洁净的空气是纯净物
B. C₆H₁₂O6属于氧化物
C. 光合作用将化学能转化为光能
D.CO₂ 可作大棚蔬菜的气体肥料
7.农产品种植需要化肥,下列属于氮肥的是
A.K₂SO₄B.Ca3(PO4)2
C.NH₄ClD.KCl
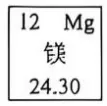
8.如图是镁元素在元素周期表中的信息,下列有关说法错误的是
A镁元素属于金属元素
B. 镁原子的符号为Mg
C. 镁原子的相对原子质量为24.30g
D. 镁原子核内有12个质子
9.某反应的微观过程如图。下列说法正确的是

10. 下列关于溶液的说法不正确的是
A. 溶液是一种均一、稳定的混合物
B. 可以用溶解度判断某种物质在某种溶剂中的溶解能力
C. 不饱和溶液变成饱和溶液后,溶质质量分数一定变大
D. 两种溶质质量分数不同的食盐水会有不同的性质,从而有不同的应用
关注公众号,再添加微信“Cxfz1972”获取更多化学资源
文章末尾有更多资源链接
第 二 部 分非 选 择 题(共40分)
本部分共包括4小题
11. (8分)实验是学习化学的重要途径。如图是实验室制取气体及性质实验的装置。
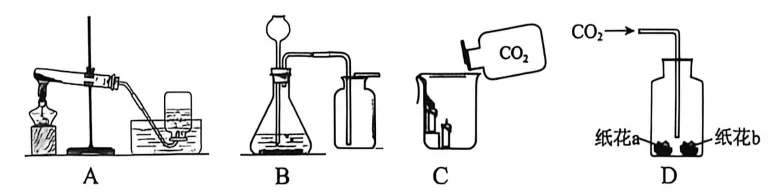
(1)实验室用加热高锰酸钾的方法制取并收集氧气,选用装置(填字母)。实验室用大理石和稀盐酸制取二氧化碳,其反应的化学方程式为。
(2)同学们利用收集的氧气进行了木炭燃烧实验,夹取一块木炭,在酒精灯上加热至发红,再将其插入集满O2的集气瓶中,观察到木炭燃烧、发出白光、放出热量。由此实验可得出促进燃烧的方法为。
(3)图C 实验中将二氧化碳沿器壁缓慢地倒入烧杯中,观察到现象是。
(4)图D 实验中,纸花a 用紫色石蕊溶液浸泡后干燥,纸花b 用紫色石蕊溶液润湿, 通入二氧化碳气体后,纸花(填字母)变红。
(5)小亮借助数字化技术对CO₂的性质进行了定量探究(图1),收集数据如图2、3所示。由图2中信息可知,二氧化碳能溶于水;由信息可知,二氧化 碳在水中的溶解有一定限度;图3中pH 曲线逐渐下降,原因是。
12. (10分)阅读下列短文并回答相关问题。
材料1:泡菜在中华饮食文化中占有重要地位,将新鲜蔬菜泡在食盐水里,放在陶土泡菜坛中密封腌制,经发酵制成。蔬菜中含有的硝酸盐对人体无直接危害,但腌制泡菜过程中会生成少量亚硝酸钠(NaNO₂),关于亚硝酸钠查阅资料可知:
①亚硝酸钠是白色至淡黄色的粉末,易溶于水,外观与氯化钠相似。
②亚硝酸钠的水溶液呈碱性,人若误食会引起中毒。
③亚硝酸盐广泛用于肉类食品添加剂,但其使用有严格限制。 如图是泡菜腌制过程中亚硝酸钠含量的变化规律。
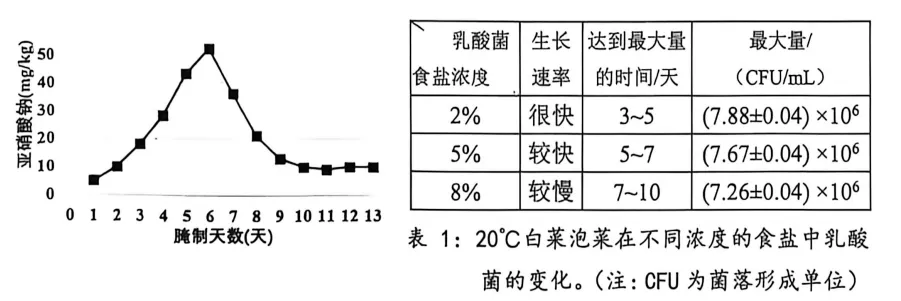
材料2:腌制过程中,蔬菜表面的天然乳酸菌在无氧环境下大量繁殖,将蔬菜中的糖 类物质分解为乳酸(C₃H₆O₃)。现代医学表明,乳酸和乳酸菌对人体健康有益,具有抑 制肠道中的腐败菌生长、降低胆固醇等保健作用。
(1)MaNO₂中氮元素的化合价为; 亚硝酸钠的物理性质有 (写一点)。
(2)泡菜中主要富含的营养物质是(填字母)。
A.维生素B. 蛋白质
(3)泡菜腌制过程中亚硝酸钠含量的变化规律是。
(4)腌制泡菜的坛口偶尔可见白色晶体,是因为。
(5)乳酸中碳、氢、氧三种元素的质量比为(最简整数比):。
(6)根据表1 可知,随食盐浓度升高,乳酸菌生长速率逐渐(填“加快”或“减慢”),最大量逐渐(填“增大”或“减小”),因此(填“高 盐”或“低盐”)环境对乳酸菌的生长有一定的抑制作用。
(7)下列说法错误的是。
A.腌制泡菜时为了防腐,加入食盐越多越好
B.亚硝酸盐严禁作为任何食品的添加剂使用
C.泡菜制作后5~6天亚硝酸钠含量较高,不是最佳食用时间
D.20℃ 时,食盐浓度为2%的泡菜中乳酸菌最大量一定为7.92×10⁶CFU/mL
13. (10分)金属冶炼技术的古今传承——中国古代已掌握了一定的金属冶炼技术,现代冶炼技术在古法基础上不断革新。请结合所学知识回答下列问题:
1、古文记载的冶炼技术
(1)战国《韩非子·内储说上》提到,早期采金技术均是“沙里淘金”。黄金能以单 质形式存在于自然界的原因是。
(2)东汉《周易参同契》记载:“胡粉[主要含PbCO₃·Pb(OH)₂], 投火中,色坏还为铅 (Pb)”。该过程主要原理之一:

,下列分析正确的是。
A. 胡粉属于混合物
B. 冶炼过程中胡粉受热分解可能生成水
C. 上述反应均属于分解反应
(3) 明代《天工开物》记载:“火法炼锌”过程为“炉甘石(主要含ZnCO₃)装载入泥 罐内……然后逐层用煤炭饼垫盛,其底铺薪,发火煅红,冷定毁罐取出,即倭铅也”。
①炉甘石炼锌的第一步是在高温下分解,生成两种氧化物,写出该反应的化学方程式: 。
②“其底铺薪”指利用燃烧的“薪”将煤炭饼引燃,从燃烧条件分析“薪”的作用是。
③火法炼锌时在鼓风炉中控制温度在1100℃至1300℃进行,使生成的锌汽化蒸馏出来,蒸馏过程属于(填“物理”或“化学”)变化。
④“冷定”才能“毁罐取出”,从化学变化角度分析,其原因是。
⑤文中“倭铅”的主要成分是(填字母)。
A.PbB.ZnC. Pb 和 Zn 混合物
Ⅱ、现代金属冶炼
现代湿法冶铜的技术在古法“曾青得铁则化为铜”基础上优化,工艺流程如图所示。
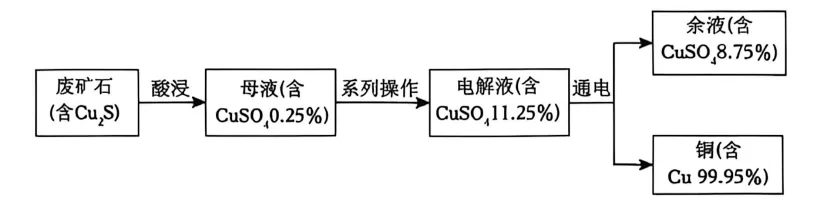
(4)结合工艺目的分析流程中“系列操作”的作用是。
(5)上述流程中,可回收再利用的物质是。
(6)工艺后期通过通电获得99.95%的高纯度铜,相较于古法炼铜,现代湿法冶铜的 优势是(答出一点即可)
14. (12分)某果蔬洗盐部分标签如下,小组同学对该果蔬洗盐的成分及含量进行探究。

【查阅资料】
I. 该果蔬洗盐中pH 调节剂的成分可能是碳酸钠( Na₂CO₃) 、碳酸氢钠( NaHCO₃) 、酒石酸或柠檬酸中的一种或两种。
Ⅱ.大多数农药是酸性的,碱性溶液可使其毒性降低。
Ⅲ.碳酸氢钠在50℃以上逐渐分解产生二氧化碳、碳酸钠和水;碳酸钠受热不分解。
IV.碳酸钠溶液与氯化钙溶液反应会产生白色沉淀。而浓度大于0.83%的碳酸氢钠溶液中 加入0.1%的氯化钙溶液,也会产生白色沉淀;浓度小于0.83%的碳酸氢钠溶液中加入 0.1%的氯化钙溶液则无现象。室温下,碳酸氢钠饱和溶液的浓度为8.8%。
(1)碳酸氢钠俗称, 它和碳酸钠都属于盐,判断依据是。
任务一:验证标签配料表中pH 调节剂的成分
【实验验证】
(2)取样溶于水,测得pH=10, 该果蔬洗盐溶液呈碱性,能 (填“中和”或“氧化”)酸性农药,使农药毒性降低。由此可排除pH 调节剂中含有酒石酸、柠檬酸 的原因是。
(3)再取样加热,将产生的气体(填操作),发现(填现象),说明pH调节剂的成分中含NaHCO₃,写出产生上述现象的化学方程式。
(4)另取样溶于水并用玻璃棒搅拌形成饱和溶液,加入0.1%的氯化钙溶液,产生了白色沉淀,说明pH调节剂的成分中含有Na₂CO₃。实验中玻璃棒搅拌的作用是。
【交流反思】
(5)小组同学认为(4)中实验结论不严谨,理由是 。因此小组同学改进了实验,最终验证pH 调节剂成分中含有Na₂CO₃ 和NaHCO₃。
任务二:测定一定量该果蔬洗盐中碳酸氢钠的质量
【实验测定】称取20g 该果蔬洗盐,加热至质量不再减少,冷却后称量固体质量为17.8g (实验数据均准确)
【实验结论】小组同学据此得出生成了2.2gCO₂ , 从而计算出该果蔬洗盐样品中NaHCO₃ 的质量为8.4g。
【交流反思】
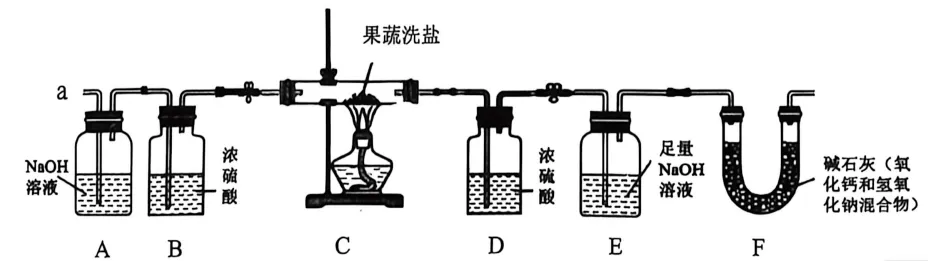
(6)经检测20g该样品中NaHCO₃的实际质量远小于8.4g,请分析NaHCO₃质量计算错误的原因:。同学们讨论后设计了如图装置(图中试剂均足量),通过 测定装置(填字母)的质量变化,也可计算出该果蔬洗盐中NaHCO₃的质量。正确的操作顺序是(填序号,选出必要的步骤,可重复选择)。
①从a口通入一段时间空气②称量D 装置质量
③称量E 装置质量④称量F 装置质量
⑤加热C装置⑥充分反应后停止加热
关注公众号,再添加微信“Cxfz1972”获取更多化学资源
文章末尾有更多资源链接

供稿:出峡飞舟
审核:昌图县杨智超初中化学名师种子工作室
版权:资料来源于网络,如商用转载,请先关注公众号,再添加公众号管理员“Cxfz1972”微信号!
如若您喜欢该篇文章敬请转发、分享!








