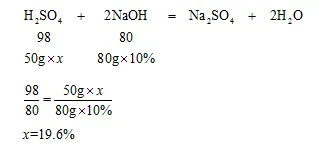一、单项选择题(本大题共20小题,每小题2分,共40分。在每小题列出的四个备选项中,只有一项符合题目要求,错选、多选或未选均不得分。)
1.下列我国古代的发明或技术中,主要原理涉及化学变化的是
A.烧制陶瓷 B.水车灌溉 C.雕版印刷 D.剪纸窗花
2.广西中科阿尔法、飓芯科技等AI企业正深耕芯片核心领域。人工智能芯片的主要成分是硅,硅元素在元素周期表中的信息及硅原子的结构示意图如图所示。下列说法正确的是
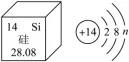
A.硅的相对原子质量为B.硅元素的质子数为14
C.硅元素位于元素周期表中第二周期
D.图中n的值为2
3.广西“三月三”的霓虹灯绚丽多彩,正是因为灯管中填充了
A.氮气 B.氧气 C.稀有气体 D.二氧化碳
4.2026年中国六五环境日的主题为“全面绿色转型,共建美丽中国”。下列做法中不利于环境保护的是
A.垃圾分类投放 B.开展植树造林
C.燃放烟花爆竹 D.自备布袋购物
5.化学在人类面对重大挑战中发挥着不可替代的作用。下列不属于化学研究范畴的是
A.开发智能机器人使生活更便利
B.应用新技术进行污水处理实现水资源良性循环
C.研发新型催化剂将煤转化为乙醇
D.研制复合材料制造风电叶片
6.下列关于水和溶液的说法不正确的是
A.明矾可加速天然水中悬浮杂质的沉降
B.过滤不能除去天然水中溶解的矿物质
C.溶液是一种或几种物质分散到另一种物质里形成的混合物
D.配制溶液用量筒量取水时俯视读数,会导致溶质质量分数偏大
7.化学与人类生活和社会发展关系密切。下列说法正确的是
A.化学与生活:工人用铝合金制成门窗——铝在常温下与氧气不反应
B.化学与安全:皮肤沾上浓硫酸——先大量冲水再涂上硼酸溶液
C.化学与健康:低血糖病人常备糖块——糖块补充人体必需的蛋白质
D.化学与能源:开发新的燃料电池——该电池将燃料的化学能转化为电能
8.广西北海某体育用品公司量产的碳纤维反曲弓弓片,采用碳纤维与树脂复合工艺制成,具有重量轻、强度高、箭速快的特点。从材料类别角度分析,该碳纤维成品属于
A.金属材料 B.复合材料 C.合成材料 D.天然材料
9.化学是一门以实验为基础的学科。下列实验操作正确的是

10.下列关于化学与人类生产、生活及身体健康的知识整理或认识,不正确的是
A.人体缺少维生素C会引起坏血病,骨质疏松患者可食用钙片补钙
B.用米粉、碎蒿末、食用油和腊猪肉等食材制作的蒿子粑粑,能够为人体提供均衡的营养。
C.淀粉属于糖类,可以提供人体需要的能量
D.为了使馒头颜色变白好看,可用二氧化硫熏蒸
11.绿色低碳转型是“十五五”规划的重要任务,旨在推动经济发展与生态保护协同共进。下列做法符合这一任务的是
A.推动废旧塑料循环利用 B.提高化石能源消费占比
C.大力提高钢铁企业产能 D.露天大量焚烧生活垃圾
12.化学小组在“垃圾的分类与回收利用”跨学科实践活动中对部分垃圾进行分类处理,其中生锈的铁制品应投放到下列哪种标识的垃圾箱?

13.利用图1所示装置探究溶液与溶液混合后发生的变化。常温下,向NaHCO3溶液中匀速滴加CaCl2溶液,传感器测得溶液的pH随时间变化如图2所示。一段时间后,三颈烧瓶和试管中均有白色沉淀生成。已知溶液呈中性。下列说法不正确的是
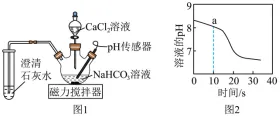
A.NaHCO3溶液显碱性
B.取a点的溶液,向其中加入稀盐酸,观察到产生气泡
C.30s时溶液显酸性的原因是CaCl2过量
D.该实验说明碳酸氢钠和氯化钙反应生成的产物有碳酸钙和二氧化碳
14.电解饱和食盐水制取NaOH的反应方程式为:
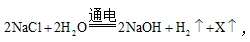 下列描述正确的是
下列描述正确的是
A.H2表示:氢气由2个氢原子构成
B.氯化钠由氯化钠分子构成
C.NaOH中氢元素的化合价为-1价
D.X是一种气体单质
15.燃烧是人类最早利用的化学反应之一,正确处理燃烧与灭火的关系,能让我们的生活更加幸福。下列做法不正确的是
A.炒菜时油锅着火可以放入青菜灭火,也可以用锅盖盖灭
B.厨房有燃气泄漏时,为避免火灾,要赶紧打开排风扇降低燃气的浓度
C.图书馆发生火灾时,要使用二氧化碳灭火器灭火
D.实验室偶发酒精在实验台燃烧事故时,要迅速使用湿抹布盖灭
16.我国科学家研发的“液态太阳燃料合成”项目工艺流程如图所示。下列说法不正确的是
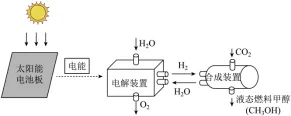
A.在合成装置中发生的是置换反应
B.电解水所用的电能是由太阳能转化而来
C.流程中H2O可以循环使用
D.该工艺为“碳中和”目标的实现提供了新路径
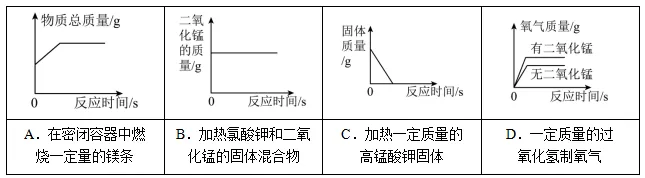
17.学会识图有助于培养科学思维。下列图像与反应过程的变化趋势对应正确的是
18.物质类别和元素价态是学习元素及其化合物性质的重要认识视角。如图展示了含硫、氮物质的类别与化合价的对应关系,
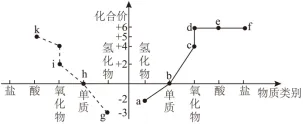
下列说法错误的是
A.e的浓溶液常用作气体干燥剂,但不能干燥g
B.c与a的水溶液反应生成b,体现出a的还原性
C.d可以与碱溶液发生复分解反应
D.j的水溶液能使紫色石蕊溶液变红,j也是导致酸雨的污染物之一
19.实验是化学研究的灵魂,以下实验无法达到预期目的
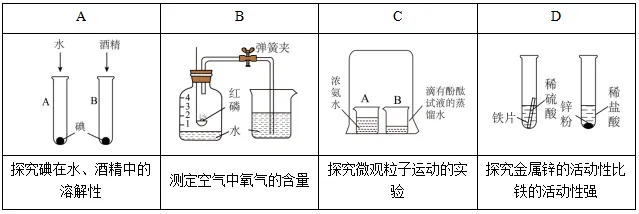
20.海洋中蕴藏着丰富的食品、矿产、能源、药物及水产资源等。如下图所示,下列有关说法不正确的是
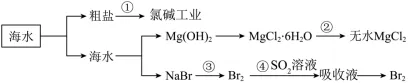

二、填空与简答题(本大题共6小题,每个方程式2分,其余每空1分,共38分。)
21.(6分)用化学用语填空。
(1)3个硫原子________;(2)镁元素_______;(3)氧离子________;
(4)2个过氧化氢分子________;(5)氢氧化铝________;
(6)标出二氧化碳中碳元素化合价________。
22.(6分)请用下列物质对应的序号填空。
①钛合金②食盐③明矾④盐酸⑤酒精⑥氖气
(1)用作调味品的是___________;(2)用于制造人造骨的是___________;
(3)可用于制造电光源的是___________;(4)胃液中可帮助消化的是___________;
(5)用作液体燃料的是___________;(6)可用作净水的混凝剂的是___________。
23.(6分)为培养学生创新思维和实践能力,某化学实验小组积极开展一系列微项目实践活动。
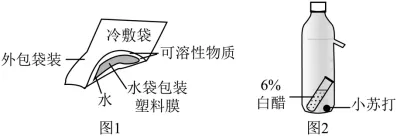
(1)自制简易净水器:利用(填名称)作絮凝剂,该物质溶于水后生成胶状物吸附杂质使其沉降;利用吸附水中色素和异味。
(2)自制加热包:原理为氧化钙与水反应放热,化学方程式为。
(3)自制冷敷袋(如图1):可溶性物质溶于水时会吸热,这种物质是(填“氯化钠”或“硝酸铵”)。
(4)自制简易灭火器(如图2):白醋与小苏打反应生成二氧化碳灭火,利用二氧化碳的性质是。
24.(6分)《2050年世界与中国能源展望》指出,全球能源结构正朝着多元化、清洁化和低碳化的方向转变。如图为不同年份的世界能源占比结构图。
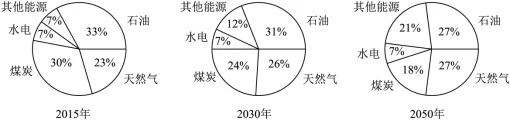
可燃冰外观与冰相似,其主要成分为甲烷水合物(由甲烷分子与水分子构成),还含有少量二氧化碳等气体,被广泛认为是极具潜力的替代能源。不过,天然气水合物的开采对温度和压强条件的控制要求极高,若控制不当导致泄漏,可能会加剧温室效应。请回答下列问题。
(1)比较2015年、2030年和2050年的能源结构。化石能源中占比日益减少的是_____、_____;它们均属于_____(填“可再生”或“不可再生”)能源。
(2)天然气是一种相对清洁的能源,其主要成分燃烧的化学方程式为_____。
(3)如果在开采天然气水合物的过程中发生泄漏,会导致______的加剧。
25.(7分)燃料的使用推动了人类社会的发展。
(1)燃料变迁过程:木柴(12KJ热值)→煤34KJ热值)→天然气(55KJ热值)。
①木柴的热值比煤 (填“高”或“低”)。
②为使煤充分燃烧,可采取的一种方法是。
③用电火花引燃气态燃料,为燃料燃烧提供的条件是。
④从达成“碳中和”的目标分析,用天然气()替代煤(C)作燃料的理由是。
(2)氢气是未来理想的能源。
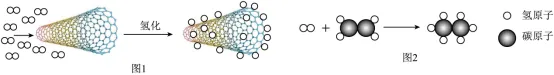
①2024年6月,我国首次实现利用海上风电电解海水制氢。电解的水,理论上能得到氢气的质量为。
②用单壁碳纳米管可储存氢气如图1,该过程中不变的微观粒子是。另一种储氢方式如图2,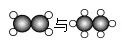 的质量比是(填最简整数比)。
的质量比是(填最简整数比)。
26.(7分)氯化钠是日常生活中不可或缺的必需品,同时也是重要的化工原料。
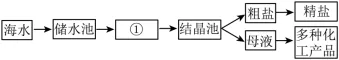
(1)下图是利用海水提取粗盐的过程:上图中①是______池(填“蒸发”或“冷却”)。
(2)粗盐进行精制,流程如下图所示。粗盐除含NaCl外,还含有少量MgCl2、CaCl2、Na2SO4以及泥沙等杂质。某同学将该粗盐样品进行提纯。
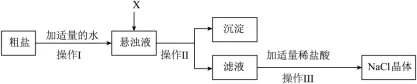
提供的试剂:A.BaCl2溶液;B.Na2CO3溶液;C.K2CO3溶液;D.NaOH溶液。
① 欲除去悬浊液中的MgCl2,CaCl2,Na2SO4,从提供的试剂中选出X所代表的试剂,按滴加顺序依次为:过量的_______(填序号)。
② 操作Ⅱ的名称是_____,此操作使用玻璃棒的作用是________,通过此操作得到的滤液中除了有NaCl外,还含有的溶质有______(填化学式)。
③ 加适量盐酸过程中,发生反应的化学方程式为____________(非中和反应)。
三、实验探究题(本大题共2小题,每个方程式2分,其余每空1分,共16分。)
27.化学是一门以实验为基础的科学。请根据下列实验装置图,回答相关问题:
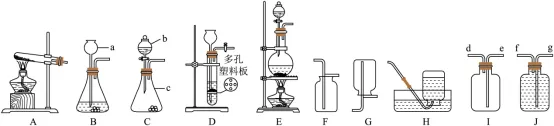
(1)实验室用双氧水制取氧气时,反应的化学方程式为_________;若使用J装置收集氧气,氧气应从_________端通入(填“f”或“g”)。
(2)实验室若用I装置收集二氧化碳,验满方法是:________。
(3)实验室通过加热氯化铵固体与熟石灰固体的混合物来制取氨气。已知氨气极易溶于水,且密度比空气小,若使用A~H装置进行制取,可选择的制取装置为:________(填字母序号,下同)。
(4)常温下,电石与水反应生成氢氧化钙和乙炔气体,该反应的化学方程式为____________;已知乙炔难溶于水且密度比空气略小,若使用A~H装置制取并收集较纯净的乙炔气体,且需控制反应速率,可选择的制取装置为:_________。
28.中华优秀传统文化中蕴含着丰富的化学知识,我国早期文献《礼记·内则》有载:“冠带垢,和灰清漱;衣裳垢,和灰清浣”。古人洗衣所用的“灰”主要是草木灰,其主要成分是碳酸钾(K2CO3)。某化学兴趣小组结合这一史料,对碳酸钾展开了探究。
【查阅资料】
① 氢氧化钾与氢氧化钠同属一类物质,它们溶于水时均会伴随能量变化。
② 常温下,碳酸钾难溶于无水乙醇,而氢氧化钾易溶于无水乙醇。
③ 碱石灰是氢氧化钠与氧化钙的固体混合物,可吸收二氧化碳和水蒸气。
【任务一】实验室制备K2CO3
取适量氢氧化钾固体于试管中,加水溶解后向溶液中通入二氧化碳气体。
(1)实验过程中,小组同学触摸试管外壁,感觉试管外壁发烫,由此认为CO₂与KOH发生了反应,但小明同学指出该方案不够严谨,理由是________。
(2)碳酸钾溶液呈碱性,能去除油污,是因为其溶液中含有较多的________(填离子符号)。
【任务二】证明K2CO3的生成
(3)取任务一中反应后的少量溶液于试管中,加入足量CaCl2溶液,若观察到,即可证明该反应已发生。
(4)小组同学认为,还可利用KOH和K2CO3在无水乙醇中的溶解度差异来证明该反应已发生。请设计实验方案:________。
【任务三】测定草木灰中K2CO3的质量分数
课外小组同学利用下图所示装置,通过测定D装置的质量变化,计算草木灰中K2CO3的质量分数。
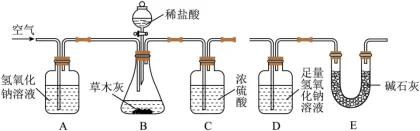
请回答下面问题:
(5)装置E的作用是________。
(6)反应前后均需通入空气,反应结束后再次通入空气的目的是________。
(7)若草木灰的质量为a克,反应后D装置质量增重b克,则该草木灰中K2CO3的质量分数为________(用含a、b的计算式表示)。
四、计算题(本大题共1小题,共16分。)
29.在“从废旧铅酸蓄电池中回收硫酸”的研学项目中,需测定电池废液中硫酸的质量分数。实验时,向盛有50 g废液的锥形瓶中加入质量分数为10%的氢氧化钠溶液并充分搅拌,同时利用温度传感器等电子设备采集信息并绘制成图像。请根据下图回答问题。(杂质可溶但不参与反应)
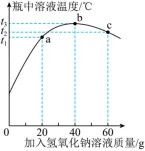
(1)由图可知,t2℃时所加入的氢氧化钠溶液___________(填“不足”“恰好反应”或“过量”)。
(2)计算废液中硫酸的质量分数(请写出计算过程)。
参考答案
1.A2.B3.D4.C5.A6.C7.D8.B9.C10.D
11.A12.B13.C14.D15.B16.A17.B18.C19.D20.D
21.(1)3S(2)Mg(3)O2-(4)2H2O2(5)Al(OH)3(6)
22.(1)②(2)①(3)⑥(4)④(5)⑤(6)③
23.(1)明矾 活性炭(2)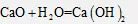
(3)硝酸铵(4)不燃烧也不支持燃烧,密度比空气大
24.(1) 煤炭 石油 不可再生(2) (3)温室效应
25.(1) 低 将煤制成蜂窝煤(合理即可) 使温度达到燃料的着火点
要得到同样的热量,需要消耗的煤更多,产生的二氧化碳更多
26.(1)蒸发(2) DAB或ADB 过滤 引流 NaOH和Na2CO3 Na2CO3+2HCl═2NaCl+H2O+CO2↑
27.(1) 2H2O2= 2H2O+O2↑ f
(2)将燃着的木条放到d端管口,若木条熄灭,则说明已收集满
(3)AG
(4) CaC2+2H2O=Ca(OH)2+C2H2↑ CH
28.

29.(1)过量
(2)解:设废液中硫酸的质量分数为x。