水和溶液
水和溶液
会有乱码,电子版下载方式在文章最后面!!!

知识点一爱护水资源
一、人类拥有水资源
1.地球表面71%被水覆盖,各种形态的水总储量为1.39×1018m3,但供人类利用的淡水小于1% 。
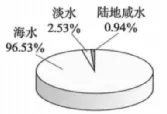
全球海水、陆地水储量比国家节水标志
2.海洋是地球上最大的储水库,海水中含有80多种元素。海水中含量最多的物质是H2O,最多的金属元素是Na,最多的元素是O。
3.我国水资源的状况是分布不均,人均量少。
二、爱护水资源
1.爱护水资源的途径:节约用水,防止水体污染
(1)节约用水
节约用水即提高水的利用效益。
生活中提倡一水多用,使用节水型器具;农业中改大水漫灌为喷灌、滴灌;工业中应用新技术新工艺循环使用。
2.防止污染
①水污染:指大量污染物质排入水体,超过水体的自净能力使水质恶化,水体及其周围的生态平衡遭到破坏,对人类健康、生活和生产活动等造成损失和威胁。
②水污染物:工业“三废”(废渣、废水、废气);农药、化肥的不合理施用;生活垃圾、生活污水的任意排放。
③防止水体污染:工业上:应用新技术、新工艺减少污染物的产生,对污染的水体处理达标后排放;
农业上:合理施用农药、化肥,提倡使用农家肥;
生活上:生活污水要集中处理达标排放,不使用含磷洗涤剂等。加强水质监测。
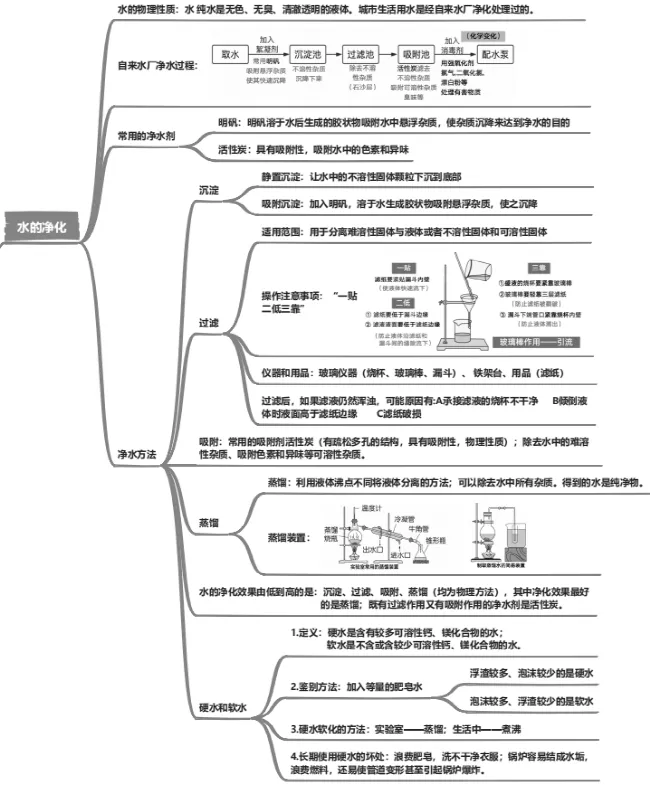
知识点二水的净化
一、水的净化
1.水 纯水是无色、无臭、清澈透明的液体。城市生活用水是经自来水厂净化处理过的。
2.自来水厂净水过程
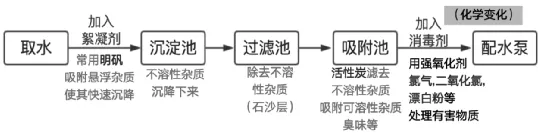
明矾的作用:明矾溶于水后生成的胶状物吸附水中悬浮杂质,使杂质沉降来达到净水的目的。
3.净化水的常用方法
沉淀、过滤和吸附、蒸馏是工业中常用的方法,也是在化学实验中分离混合物的常用方法。
(1)沉淀:①静置沉淀,让水中的不溶性固体颗粒下沉到底部;
②吸附沉淀,加入明矾,溶于水生成胶状物吸附悬浮杂质,使之沉降。
(2)过滤:①适用范围:用于分离难溶性固体与液体或者不溶性固体和可溶性固体
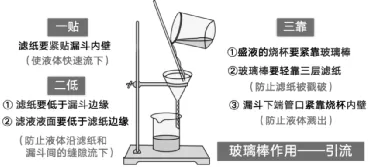
②操作注意事项:“一贴二低三靠”
③仪器和用品:玻璃仪器(烧杯、玻璃棒、漏斗)、 铁架台、用品(滤纸)
④过滤后,如果滤液仍然浑浊,可能原因有:
A承接滤液的烧杯不干净B倾倒液体时液面高于滤纸边缘 C滤纸破损
⑤过滤后仍然浑浊的处理方法,清洗仪器,更换滤纸,重新过滤。
(3)吸附:常用的吸附剂活性炭(有疏松多孔的结构,具有吸附性,物理性质);
除去水中的难溶性杂质、吸附色素和异味等可溶性杂质。
(市场上出售的净水器,有些就是利用活性炭来吸附、过滤水中的杂质的)
(4)蒸馏:利用液体沸点不同将液体分离的方法;可以除去水中所有杂质。得到的水是纯净物。
沸石(碎瓷片)的作用:防止液体暴沸。
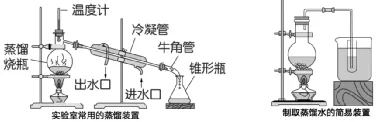
冷凝管中水下进上出:充分冷凝水蒸气;
简易装置的长导管相当于冷凝管:充分冷却水蒸气。
(5)各种净化方法除去的杂质的种类
难溶性杂质 | 可溶性杂质 | 降低水的硬度 | |
沉淀 | √ | ||
过滤 | √ | ||
吸附 | √ | √ | |
蒸馏 | √ | √ | √ |
水的净化效果由低到高的是:沉淀、过滤、吸附、蒸馏(均为物理方法),其中净化效果最好的是蒸馏;既有过滤作用又有吸附作用的净水剂是活性炭。
二、硬水和软水
1.定义:硬水是含有较多可溶性钙、镁化合物的水;软水是不含或含较少可溶性钙、镁化合物的水。
2.鉴别方法:加入等量的肥皂水
现象与结论:浮渣较多、泡沫较少的是硬水,泡沫较多、浮渣较少的是软水。
3.硬水软化的方法:实验室——蒸馏、生活中——煮沸
4.长期使用硬水的坏处:
浪费肥皂,洗不干净衣服;锅炉容易结成水垢,浪费燃料,还易使管道变形甚至引起锅炉爆炸。
知识点三水的组成及变化的探究
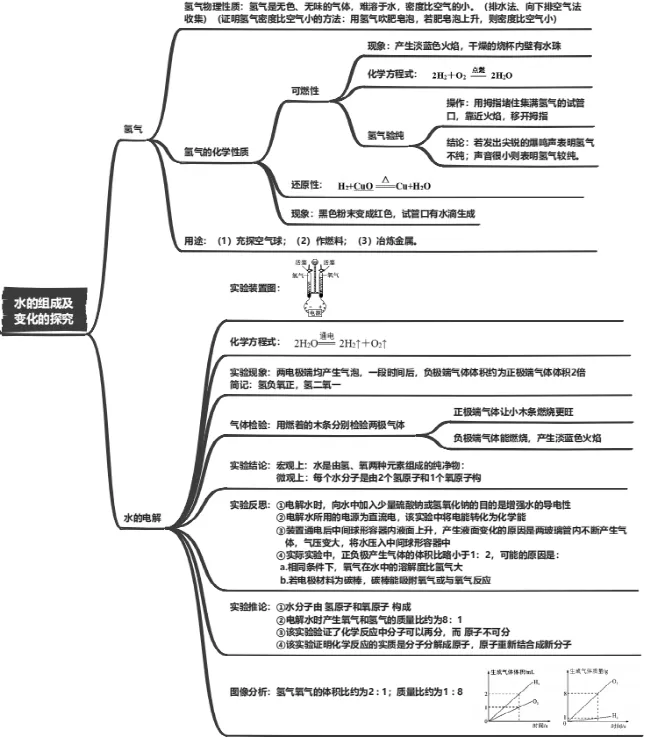
一、氢气
1.氢气物理性质:氢气是无色、无味的气体,难溶于水,密度比空气的小。(收集:排水法、向下排空气法)
(证明氢气密度比空气小的方法:用氢气吹肥皂泡,若肥皂泡上升,则密度比空气小)
2.氢气的化学性质:可燃性
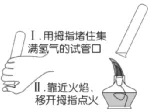
不纯的氢气(混有一定量空气或氧气)遇明火可能会爆炸,氢气的爆炸极限的体积分数为4%~74.2%,因此点燃前必须验纯(如图所示操作)。若发出尖锐的爆鸣声表明氢气不纯(此时点燃较危险);声音很小则表明氢气较纯。
3.用途:(1)充探空气球;(2)作燃料;(3)冶炼金属。
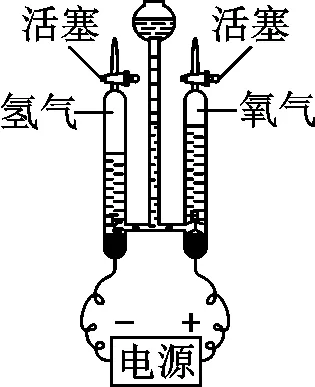
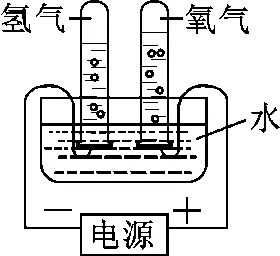
二、水的电解
1.水的电解实验分析简记:正氧负氢,氢二氧一或者(负氢多二)
实验装置 | 实验步骤 | 实验现象 | 现象分析 | |
| 1.接通电源 | 两电极端均产生气泡,一段时间后, 负极端气体体积约为正极端气体体积2倍 | 相同条件下,负极产生气体较快较多 | |
2.用燃着的木条 分别检验两极气体 | 正极端气体让小木条燃烧更旺, 负极端气体能燃烧,产生淡蓝色火焰 | 正极端气体具有助燃性 负极端气体具有可燃性 | ||
实验结论 | 反应表达式 | 注意事项 | ||
水通电生成氢气和氧气,说明水由氢元素和氧元素组成 | 文字表达式: 符号表达式: | 电源选择直流电;水中加入硫酸钠或氢氧化钠的目的:增强水的导电性 | ||
反思交流 | ||||
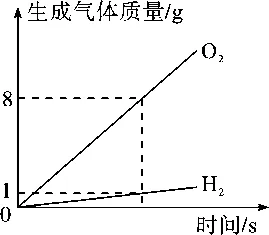
1.气体聚集在玻璃管上端,说明气体具有什么性质? 气体密度小于水,且溶解性不大 2.实验时正负极端产生的气体体积比小于1:2的原因? 氧气不易溶于水,氢气难溶于水;且氧气可能和金属电极发生反应。 | 3.本实验得到的气体体积比和质量比图像
氢气氧气的体积比约为2 : 1;质量比约为1 : 8 | |||
2.微观理解水的电解
化学反应前后原子种类不变,故反应前后元素种类不变

知识点四溶液的形成
一、溶液
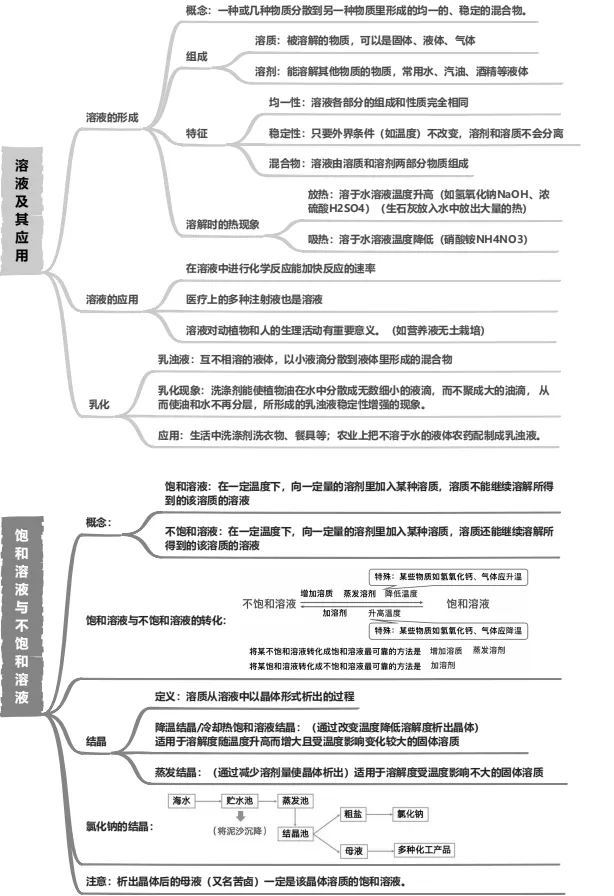
1.溶液:一种或几种物质分散到另一种物质里,形成均一的、稳定的混合物。
注意:
①溶液是澄清透明的,但不一定无色。 如CuSO4溶液(含有Cu2+) 为蓝色,FeSO4溶液(含有Fe2+) 为浅绿色,Fe2(SO4)3溶液(含有Fe3+)为黄色。
如CuSO4溶液(含有Cu2+) 为蓝色,FeSO4溶液(含有Fe2+) 为浅绿色,Fe2(SO4)3溶液(含有Fe3+)为黄色。
② 均一、稳定的液体不一定是溶液,如水,溶液必须是混合物。
均一、稳定的液体不一定是溶液,如水,溶液必须是混合物。
2.溶液特征:均一性、稳定性、混合物。
3.溶液的组成
①溶质:被溶解的物质,可以是固体、液体或气体。(一种溶液中的溶质可以是一种或几种)
②溶剂:能溶解其他物质的物质,水是最常用的溶剂,汽油和酒精也可以作溶剂。(一种溶液中的溶剂只有一种)
4.溶液的命名原则是“质+剂”(溶质名在前,溶剂名在后),如:把硝酸铵溶于水后所得的溶液,全称应叫“硝酸铵的水溶液”,碘溶于酒精和汽油所得溶液的全称叫“碘的酒精溶液”、“碘的汽油溶液”,即“非水溶剂”在名称中都是点明的,不是隐含的;但溶剂是水的时候一般不指出来,所以“硝酸铵的水溶液”简称“硝酸铵溶液”,“硫酸铜的水溶液”简称“硫酸铜溶液”。根据下列溶液的名称能判断出溶质和溶剂(溶质在前,溶剂在后):碘酒:碘、酒精;白磷的二硫化碳溶液:白磷、二硫化碳;稀盐酸:氯化氢气体、水;稀硫酸:硫酸、水;医用75%的酒精溶液:酒精、水;硝酸银溶液:硝酸银、水;生理盐水:氯化钠、水;葡萄糖注射液:葡萄糖、水;澄清石灰水:氢氧化钙、水;硫酸铜溶液:硫酸铜、水;氯化亚铁溶液:氯化亚铁、水。
5.悬浊液、乳浊液
常见混合物有溶液和浊液两大体系,溶液是均一、稳定的,浊液是不均一、不稳定的。浊液分为悬浊液和乳浊液,固体小颗粒悬浮于液体里形成的混合物叫做悬浊液,小液滴分散到液体里形成的混合物叫做乳浊液。悬浊液和乳浊液振荡后都呈浑浊状态,静置后都分为两层。
6.影响溶解的因素:
⑴高锰酸钾难溶于汽油而碘易溶于汽油,说明影响溶解的因素有溶质的性质。
⑵碘难溶于水却易溶于汽油,说明影响溶解的因素有溶剂的性质。
⑶在其他条件相同时,糖在热水中溶得的又快又多,说明影响溶解的因素有温度。
⑷在其他条件相同时,糖粉溶得比糖块快,说明影响溶解的因素有固体颗粒大小。
⑸在其他条件相同时,搅拌能加快溶解速率,说明影响溶解的因素有搅拌。
⑹影响溶解的因素:溶质性质、溶剂性质、溶剂用量、温度、固体颗粒大小、搅拌;其中,前四项既能影响溶解的速率,也能影响溶解的量;而后两项只能影响溶解的速率。
⑺生活中为使糖块快速溶解,方法有将糖块研碎、用热水溶解、搅拌。
7.溶解中的放热与吸热现象:物质溶解都有放热和吸热现象,只是大多数物质Q放=Q吸。
⑴溶于水能吸收大量热的物质是硝酸铵,用它可作人造小冰箱,原因是硝酸铵溶于水时能吸收大量热而使周围环境温度下降。
⑵溶于水能放出大量热使溶液温度升高的物质有生石灰、浓硫酸、固体氢氧化钠。
化学式依次为 [CaO] [H2SO4] [NaOH]
8.溶液的作用:
(1)能加快反应速度,原因是:溶解时,在水分子的作用下构成物质的微粒均匀的运动到水分子的间隔中去了,反应时能充分的接触。
(2)食物中的有些营养物质经过消化变成溶液才能被人体吸收。
(3)在医疗上配制药剂。
(4)在农业上配制无土栽培营养液。
9.物质溶于水时引起的特性改变:
①使水的沸点升高,从而得到较高温度的水。
②使水的凝固点降低,从而使海水在较低温度下也不易结冰、但会使冰雪在较低温度下就能融化。
③物质溶于水后会使所得溶液的密度变大,溶得越多,溶液浓度越大密度越大。
10.溶液的应用:
(1)冰雪路上撒盐是因为氯化钠溶于水时使水的凝固点降低,使冰雪在较低温度下融化,可防止发生事故。
(2)农业上常用浓的氯化钠溶液选种,原理是浓的氯化钠溶液密度大,倒入其中的种子所受的浮力大,不饱满的种子会浮起来而被除去。
(3)冬天河水冰厚而海水冰薄是因为海水含盐量高,而物质溶于水时能使水的凝固点降低,使海水在较低温度下也不易结冰,或冰层薄。
(4)煮饺子时加氯化钠可使饺子熟的快而透,因为氯化钠溶于水使水的沸点升高,从而得到较高温度的水,所以饺子熟的透而快。
(5)把鸡蛋浸入水中,不断加入氯化钠,现象是蛋会上浮,原因是物质溶于水使所得溶液密度变大,使蛋所受的浮力变大而上浮。
11.用微粒的观点解释下列溶解现象:
(1)物质溶于水后形成的水溶液有均一性的原因是:在水分子的作用下,构成物质的粒子均匀的运动到水分子的间隔中去了。
(2)葡萄糖注射液有均一性的微观原因是:在水分子作用下,葡萄糖分子均匀的运动到水分子的间隔中去。
(3)生理盐水注射液有均一性的微观原因是:在水分子作用下,氯离子和钠离子均匀的运动到水分子的间隔中去。
二、乳化
1.乳浊液:一种液体以小液滴形式分散到另一种不相溶的液体里形成的混合物,如牛奶和豆浆。乳浊液不均一不稳定,静置后会分层。
2.乳化剂:能使乳浊液稳定性增强的物质。
3.乳化现象:洗涤剂等乳化剂使植物油在水中分散成无数细小的液滴,而不聚成大的液滴,从而使油和水不再分层的现象。其中洗涤剂所起的作用叫乳化作用。
4.乳化现象应用:生活中洗涤剂洗衣物、餐具等;农业上把不溶于水的液体农药配制成乳浊液。
注意:用乳化剂去油污是利用了乳化剂的乳化作用;用汽油洗去衣物上的油渍用的是溶解原理;用氢氧化钠去油污利用的是氢氧化钠和油污能发生化学反应。
知识点五饱和溶液和不饱和溶液
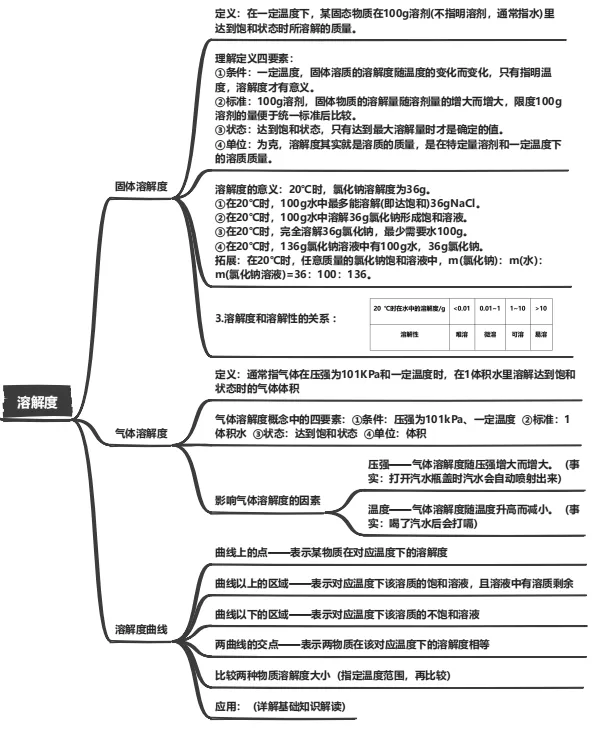
1.饱和溶液与不饱和溶液:
(1)由定义推理可知,判断饱和性的方法是向溶液中再加入该物质,充分搅拌后观察固体是否减少。
(2)由定义判断:向20℃时氯化钠的饱和溶液中加入氯化钠,充分搅拌后,溶液质量、溶剂质量、溶质质量、溶液浓度均不变。若原溶液不饱和,加入氯化钠充分搅拌后,结果是:溶剂质量不变,因固体溶解,所以溶质质量、溶液质量、溶液浓度均变大。
(3)分析:盐池中有氯化钠晶体析出的海水能不能再溶解氯化钠了:不能;像这样有晶体析出的溶液叫母液,因有晶体析出而无法再溶解该物质,所以母液都是饱和溶液。
2.饱和溶液和不饱和溶液的转化方法:
(1)在其他条件相同时,大多数物质在热水中溶的又多又快,但氢氧化钙(熟石灰)和气体类在热水中反而溶的少。由此归纳饱和溶液与不饱和溶液的转化方法为:
(加足量水)(升温)

(加足量溶质)(降温)(蒸发溶剂)
(2)小结强调:
①改变温度时,熟石灰[Ca(OH)2]和气体类特殊,即水温升高时,它们的溶解度反而减小,水温下降时,它们的溶解度反而变大,跟其他物质反过来了。
②某温度下(即不许改变温度时),由饱和溶液变为不饱和溶液,最稳妥的办法是加足量水;由不饱和溶液变为饱和溶液,最稳妥的办法是加足量溶质和恒温蒸发溶剂。
(3)应用:
①欲使接近饱和的硝酸钾溶液达到饱和,方法有加入足量硝酸钾、蒸发溶剂、降温。
②欲使接近饱和的石灰水达到饱和,方法有加入足量熟石灰、蒸发溶剂、升温。
③使饱和溶液中的硝酸钾固体溶解(即变为不饱和),方法有加足量水、升温。
④使石灰水中残留的Ca(OH)2固体溶解(即变为不饱和),方法有加足量水、降温。
知识点六溶解度曲线
1.固体溶解度[S]:
⑴定义:一定温度下,某固态物质在100g溶剂里达到饱和状态所溶解的质量。没指明溶剂时,通常所说的溶解度就是指在水中的溶解度。简而言之,溶解度就是一个“数”,这个“数”就是物质在一定温度下的“100g水”里所能溶解的“最大值”。
⑵溶解度含义及简单计算:20℃时氯化钠溶解度为36g,含意是20℃时100g水中最多溶解36g氯化钠。
20℃时,50g水最多溶解氯化钠18g,此时欲溶解36g氯化钠至少需水100g,欲溶解108g氯化钠至少需水300g。(饱和溶液中,质:剂==S:100)
⑶影响固体溶解度的因素:溶质的性质、溶剂的性质、温度。注意:颗粒大小和搅拌只能影响溶解的速率。
2.溶解度曲线应用:(注:A、B、C代表物质依次为——硝酸钾、氯化钠、熟石灰或气体)
⑴会比较S大小:0℃时溶解度大小顺序为B、C、A ,t2℃时三种物质溶解度大小顺序为A、B、C。
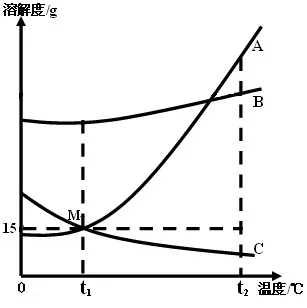
 2℃50g水中最多能溶解A物质25g。
2℃50g水中最多能溶解A物质25g。
②t2℃一瓶饱和A溶液的浓度为33.3%。
③t2℃把25gA物质放入100g 水中,所 得溶液质量为125g,
浓度为20%,所得溶液是否饱和:不是;降温至t1℃,所得溶液质量为115g,
此时溶液是否饱和:是。
⑶会判断饱和溶液浓度随温度变化情况:
①t2℃三物质的饱和溶液降温至t1℃,A溶液浓度将变小,B溶液浓度将变小,
C溶液浓度将不变。
②t1℃三物质的饱和溶液升温至t2℃,A溶液浓度将不变,B溶液浓度将不变,C溶液浓度将变小。
③t1℃三物质的饱和溶液(杯内有剩余晶体),升温至t2℃,A溶液浓度将变大,B溶液浓度将变大,C溶液浓度将变小。A溶液中能看到的现象是晶体减少,C溶液中能看到的现象是晶体增多。
④t1℃的三种物质饱和溶液,升温时浓度变小的是C,降温时浓度变小的是A、B。
⑤t2℃时三个物质饱和溶液的浓度大小顺序为A、B、C,降温至t1℃时溶液浓度的大小顺序为B、A、C(可画水平线判断:A溶解度虽下降但并没有低于C在t2℃的“高度”)。
⑷M点含义是:t1℃时A和C的溶解度相等都是15g(注意:纵坐标若给出数值需指出)。
⑸会观察溶解度曲线图选择合适的结晶方法:从溶液中析出A常用冷却热饱和溶液结晶法,从溶液中析出B常用蒸发溶剂结晶法,欲除去A中少量B常用冷却热饱和溶液结晶法,欲除去B中少量的A常用的方法是蒸发溶剂法后再趁热过滤。
⑹会判断饱和与不饱和转化方法:欲使C的溶液达到饱和方法有加入足量C、升温、蒸发溶剂;欲使A溶液达到饱和方法有加入足量A、降温、蒸发溶剂。
⑺在指定的温度下(即不许改变温度)考查饱和溶液与不饱和溶液的转化方法:t2℃时,使A、B、C不饱和溶液变为饱和溶液的方法依次是加入足量A、加入足量B、加入足量C,或恒温蒸发水;t2℃时,使A、B、C的饱和溶液变为不饱和溶液的方法均为加入足量水。
3.气体溶解度:
⑴气体溶解度的影响因素有温度、压强,其规律是:气体溶解度随温度升高而减小,随压强增大而增大。
⑵会用气体溶解度的影响因素解释简单实际问题:
①喝汽水易打嗝是因为:体内温度高,二氧化碳溶解度变小逸出。
②打开汽水瓶盖会冒出大量气泡是因为:打开瓶盖时瓶内压强变小,二氧化碳溶解度变小逸出。
④水沸腾前就会出现气泡是因为:温度升高,水中空气的溶解度变小逸出。
知识点七结晶的方法
1.结晶方法:(注:溶解度大的物质溶解能力就强,反之即弱)
(1)结晶含义:因水蒸发,或温度改变导致物质溶解度变小(溶解能力减弱),溶解在溶液中的溶质会以固体形式析出,这个过程叫结晶。这是从海水、湖水、或其他溶液中提取物质的常用方法。
(2)会根据物质溶解度差异(即溶解能力的差异)选择合适的结晶方法:像硝酸钾这样“随温度降低溶解度迅速减小至很小”的物质,欲使其从溶液中析出常用的结晶方法是冷却热饱和溶液法;像氯化钠这样“溶解度受温度影响不大(温度升高溶解度并没有迅速增大,低温下溶解度也不是很小)”的物质无法用冷却热饱和溶液法,只能用蒸发溶剂法使其从水溶液中析出。
(3)冷却热饱和溶液法也可以分离几种可溶物组成的混合物,但这类混合物的主要物质应是“溶解度受温度影响很大的”,所含的杂质应是“溶解度受温度影响不大的”,如硝酸钾中混有少量氯化钠可用冷却热饱和溶液法提纯得到硝酸钾。
(4)氯化钠中混有少量硝酸钾,因氯化钠是含量较多的主要物质,所以用冷却热饱和溶液法使氯化钠大量结晶析出是不可能的,所以提纯氯化钠之法应是蒸发溶剂法后趁热过滤。
2.用结晶法分离混合物:
(1)硝酸钾晶体中混有少量氯化钠,除去氯化钠的操作过程:
将固体溶解后加热蒸发至刚好有晶体析出制成热的硝酸钾饱和溶液,然后降温、结晶、过滤、用冷水洗涤晶体、干燥后即得硝酸钾晶体。
(2)氯化钠晶体中混有少量硝酸钾,除去硝酸钾的操作过程:
将固体溶解后加热蒸发至出现较多量固体,趁热过滤、洗涤、干燥后即得氯化钠晶体。
知识点八溶质质量分数
1.溶液浓度
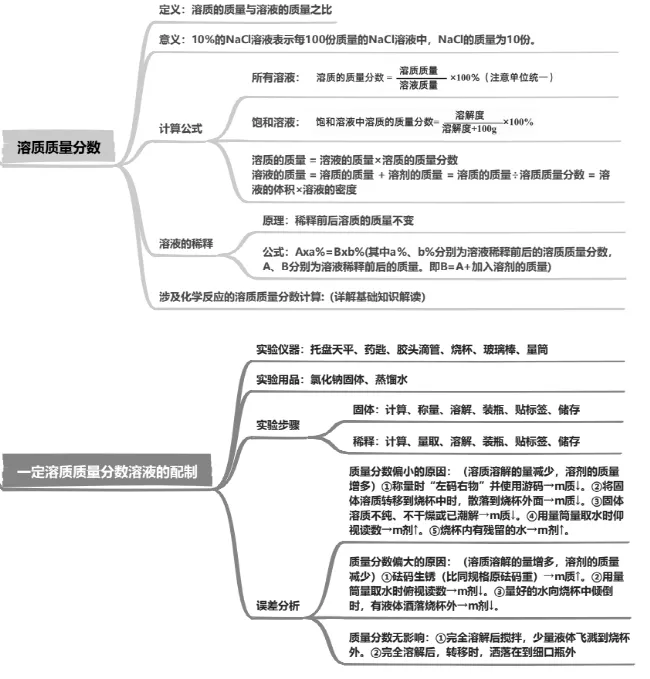
溶液中的溶质质量分数:溶质质量与溶液质量之比。
2.计算溶液浓度:
⑴把10g氯化钾溶液蒸干得到2g晶体,求此溶液溶质质量分数。
解: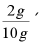 100%==20% 答:氯化钾溶液浓度为20%。[即]:浓度==
100%==20% 答:氯化钾溶液浓度为20%。[即]:浓度==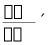 100%
100%
⑵会利用溶解度求饱和溶液浓度:甲物质在T℃时溶解度为50g,求T℃其饱和溶液浓度。
解: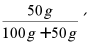 100%==33.3%答:此温度时该饱和溶液浓度为33.3% 。
100%==33.3%答:此温度时该饱和溶液浓度为33.3% 。
[即]:饱和溶液浓度=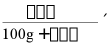 100%(溶解度代表100g水溶解的最大溶质量)。
100%(溶解度代表100g水溶解的最大溶质量)。
3.溶液稀释:
[思路]:加水稀释前后溶液中的“溶质”质量没变,以此即可设出X列出等量方程。
⑴50g溶质质量分数为98%的浓硫酸变为20%的稀硫酸,需加水多少g?
解:设需要水的质量为X 。
50g×98%=(50g+X)×20%X=195g
或法:设需浓硫酸质量为X。
50g×98%=X20%X=245g水=245g—50g==195g
或法:50g×98%=49g49g÷20%=245g水=245g—50g==195g 答:需要水195g。
⑵成倍数稀释的口算法:
[思路]:加水稀释浓度减半,则应加水使溶液变为原溶液2倍;浓度稀释为原1/5则加水使溶液变为5倍;浓度变为1/10则加水使溶液变为10倍……
例:100g溶质质量分数为20%的氢氧化钠溶液稀释成10%(稀释2倍)需加水100g,若变为2%(稀释10倍)则需加水900g,若变为1%(稀释20倍)则需加水1900g。
4.溶液变浓:
[思路]:溶液变浓的方法:一是加入溶质,主导思路是:原溶质+加入的溶质=所得溶液中的溶质。二是蒸发水,主导思路是:蒸发水前后溶液中溶质质量没变,以此即可设出X列出等量方程;但应注意所得溶液质量改变了。
⑴100g溶质质量分数为5%的氢氧化钠溶液变为10%,需加氢氧化钠或蒸发水各多少g?
解:设需要加入氢氧化钠的质量为x,或蒸发水的质量为y 。
100g×5%+x=(100g+x)×10%x=5.6g
100g×5%=(100g—y)×10%y=50g
答:需要加入5.6g的氢氧化钠或者蒸发50g的水。
⑵800g浓度为10%的氢氧化钠溶液变为20%,需加入氢氧化钠100g,或蒸发水400g。
[小结]:“10%变为20%”的情况,加入溶质的质量=原溶液质量的八分之一;蒸发掉水的质量=原溶液质量的一半。
5.混合问题:
[思路]:第一杯溶质加第二杯溶质等于混合后总溶质的质量,第一杯溶液加第二杯溶液等于混合后总溶液的质量。若“等质量混合”,所得溶液浓度=原两溶液浓度“和的一半”。
100g溶质质量分数为10%的氢氧化钠溶液与100g溶质质量分数为20%的氢氧化钠溶液混合,所得溶液溶质质量分数为15%。
解: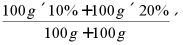 100%==15%答:混合后溶液浓度为15% 。
100%==15%答:混合后溶液浓度为15% 。
知识点九一定溶质质量分数溶液的配制
配制一定溶质质量分数的溶液
1.固体药品加水配制一定溶质质量分数的溶液 ( 固体 + 水 )
所用仪器:

实验步骤:
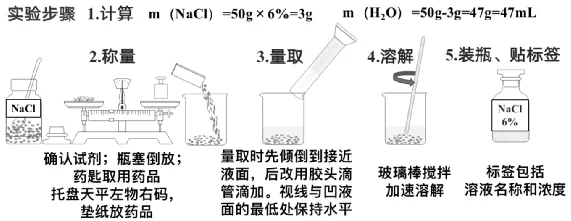
例.找出下列配置一定浓度氯化钠溶液的错误操作,并改正。
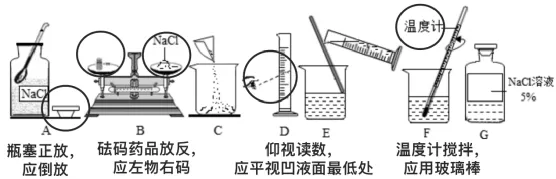
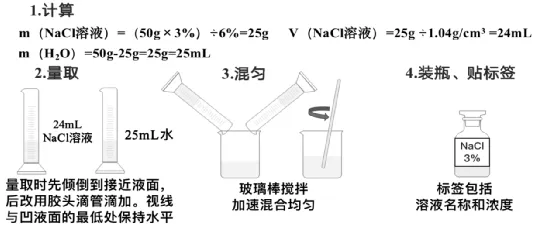
2.溶液加水稀释配制一定溶质质量分数的溶液 (液体+水)
3.误差分析
质量分数偏小的原因:
①称量时“左码右物”并使用游码→m质↓。
②将固体溶质转移到烧杯中时,散落到烧杯外面→m质↓。
③固体溶质不纯、不干燥或已潮解→m质↓。
④用量筒量取水时仰视读数→m剂↑。
⑤烧杯内有残留的水→m剂↑。
质量分数偏大的原因:
①砝码生锈(比同规格原砝码重)→m质↑。
②用量筒量取水时俯视读数→m剂↓。
③量好的水向烧杯中倾倒时,有液体酒落烧杯外→m剂↓。
质量分数无影响:
①完全溶解后搅拌,少量液体飞溅到烧杯外。
②完全溶解后,转移时,洒落在到细口瓶外。
电子版下载方式:
2.扫码: