
电子版下载方式在文章最后面!!!

【2026中考复习系列】化学——物质的多样性

知识点一物质的分类
一、纯净物和混合物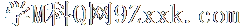
1.纯净物和混合物的比较
混合物 | 纯净物 | |
定义 | 两种或多种物质混合而成的物质叫混合物。 | 只由一种物质组成的物质叫纯净物。 |
特点 | 组成混合物的各种成分之间没有发生化学反应,它们各自保持着原来的性质。 | 纯净物可以用化学式来表示。但是,绝对纯净的物质是没有的。 |
常见实例 | 空气、溶液、合金、铁锈、加碘盐、天然气、自来水、矿泉水等 | 能用化学式表示的所有物质 冰水混合物、水蒸气、铜锈也是纯净物 |
2.纯净物与混合物的相互转化

①从宏观上来说,纯净物由一种物质组成,有固定的组成和性质,可以用化学式表示,如氢气、蒸馏水等;混合物由两种或两种以上的物质组成,没有固定的组成和性质,如空气、矿石、溶液、合金等。
②从微观上来说,由同种分子构成的物质属于纯净物,由不同种分子构成的物质属于混合物。
二、单质、化合物、氧化物
1.单质
概念:同种元素组成的纯净物是单质。如金属单质:如Mg、Fe、Cu、Ag等,非金属单质:如C、S、H2、O2等,稀有气体:如He、Ne、Ar等
2.化合物
概念:不同种元素组成的纯净物是化合物。如氯化钠(NaCl)、高锰酸钾(KMnO4)
3.氧化物
概念:氧化物是指由两种元素组成,其中一种是氧元素的化合物。如金属氧化物,如CuO、MgO等;
非金属氧化物,如CO2、CO、P2O5、SiO2等
4.单质、化合物、氧化物、含氧化合物的联系:
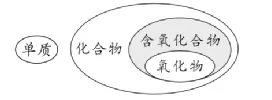
5.物质之间的关系:
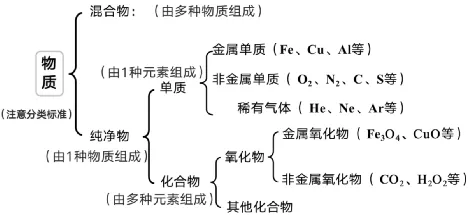
三、酸、碱、盐
1.酸:物质溶于水时,形成的阳离子全部是H+的化合物。
例:H2SO4(硫酸)、H2CO3(碳酸)、HNO3(硝酸)、HCl(盐酸,学名氢氯酸)
2.碱:物质溶于水时,形成的阴离子全部是OH-的化合物。
例:KOH(氢氧化钾)、NaOH(氢氧化钠)、Ca(OH)(氢氧化钙)、Ba(OH)2(氢氧化钡)
3.盐:由金属离子(或NH4+)和酸根离子形成的化合物。
例:NaCl(氯化钠)、Na2CO3(碳酸钠)、NaHCO3(碳酸氢钠)、CaCO3(碳酸钙)
4.酸碱盐之间的关系:

四、有机化合物
化合物可分为有机化合物和无机化合物,有机化合物都含有碳元素。
1.有机化合物:含有碳元素的化合物称为有机化合物。
例如甲烷(最简单的有机物、相对分子质量最小的有机物)、乙醇(俗名:酒精)、乙酸(俗名:醋酸)、葡萄糖、蔗糖、蛋白质、淀粉等
2.无机化合物:不含碳元素的化合物称为无机化合物。
例如水(H2O)、硫酸(H2SO4)、氢氧化钠(NaOH)等
3.碳的氧化物、碳酸、碳酸盐等具有无机化合物的特点,属于无机化合物。
知识点二物质的性质
物理性质 | 化学性质 | |
定 义 | 物质不需要发生化学变化就可以表现出来的性质 | 物质在化学变化中表现出来的性质 |
实 例 | 颜色、状态、气味;硬度、密度、燃点、沸点、熔点;溶解性、挥发性、导电性、导热性、吸附性等 | 可燃性、助燃性;氧化性、还原性; 稳定性、活泼性;酸性、碱性、毒性等 |
区 别 | 某种性质是否需要经过化学变化才能表现出来 | |
注 意 | 物质的性质受外界条件影响,在描述物质性质时注明条件。(如液体沸点受大气压影响) |
知识点三性质与用途之间的关系
单 质 | 氧气 | 助燃性(支持燃烧)——炼钢、气焊 供给呼吸——医疗急救、潜水 |
氮气 | 化学性质不活泼(稳定)——填充食品包装袋保鲜 | |
氢气 | 可燃性——高能燃料 能与某些金属氧化物反应——冶炼金属 | |
金刚石 | 硬度大——钻头、玻璃刀 金刚石薄膜透光性好、硬度大——作透镜等光学仪器的涂层 金刚石薄膜导热性好——用于集成电路基板散热,提高芯片性能 | |
石墨 | 灰黑色、质软——铅笔芯 有滑腻感——润滑剂 导电性——作电极 | |
铁 | 导热性——铁锅 遇水和氧气会生锈——作“双吸剂”,食品保质、“暖宝宝”的发热材料 | |
氧 化 物 | 二氧化碳 | 不燃烧,也不支持燃烧且密度比空气的大——灭火 能溶于水且与水反应——制汽水等碳酸饮料 干冰升华吸热——制冷、人工增雨 参与光合作用——作气体肥料、光合作用原料 化工产品的原料 |
一氧化碳 | 可燃性——气体燃料 与某些金属氧化物反应——冶炼金属 毒性——易与血红蛋白结合,造成人体缺氧 | |
氧化钙 | 与水反应——制氢氧化钙、干燥剂 | |
水 | 生命必需物质、最常用的溶剂 | |
二氧化锰 | 常见的催化剂 | |
酸 | 盐酸 | 与金属氧化物反应——金属除锈 人体胃液中含有盐酸,可帮助消化 |
硫酸 | 与金属氧化物反应——金属除锈 浓硫酸具有吸水性——实验室作干燥剂 | |
醋酸 | 除水垢 酸味调味品 | |
碱 | 氢氧化钠 | 吸水性——干燥剂 与二氧化碳反应——除二氧化碳 与油污反应——除油污(炉具清洁剂的主要成分) |
氢氧化钙 | 与CO2反应生成沉淀——检验CO2 与酸反应——改良酸性土壤 常用的建筑材料 | |
盐 | 碳酸钙 | 石灰石或大理石与盐酸反应——实验室制二氧化碳 石灰石高温分解——工业制二氧化碳和生石灰 大理石(主要成分是碳酸钙)——装饰、建筑材料(建筑材料的主要成分) 作补钙剂 |
氯化钠 | 调味、防腐、选种、融雪、医疗上配制生理盐水 | |
碳酸钠 | 工业上制取烧碱 广泛用于玻璃、造纸、纺织等行业及洗涤剂的生产 | |
碳酸氢钠 | 与盐酸反应——治疗胃酸过多症 制作面点所用发酵粉的主要成分之一 | |
其 他 | 甲烷 | 可燃性——作燃料 |
乙醇 | 可燃性——实验室用得最多的燃料 医疗上消毒杀菌 | |
活性炭 | 吸附性——吸附色素和异味 |
电子版下载方式:
2.扫码:








