九年级化学第一次中考模拟考试试题
相对原子质量: H 1O 16C 12Cl 35.5Na56Ca40
一、选择题(本题包括20小题,每小题2分,共40分。以下每题各只有一个正确答案,多选、错选均不得分;把正确答案的序号用铅笔涂在答题卡的规定位置)
1.放入足量水中能形成无色溶液的是()
A.冰B.蔗糖C.植物油D.氯化铜
2.下列关于常见酸和碱的说法中,错误的是( )
A.稀盐酸和稀硫酸都可以用来除铁锈
B.浓硫酸需要密封保存是为了防止其吸收空气中的水分
C.浓盐酸在敞口容器中放置一段时间后,其溶液质量减小
D.打开盛有浓盐酸和浓硫酸的试剂瓶瓶塞,在瓶口都有白雾
3.全面推进乡村振兴,大力发展农业生产,农业上常用溶质质量分数16%的氯化钠溶液来选种,溶液在日常生活、工农业生产和科学研究中具有广泛的用途,下列有关溶液的说法正确的是 ()
A.均一的、稳定的液体一定是溶液B.碳酸钙和水可以形成溶液
C.溶液一定是混合物D.医用酒精是75%的乙醇溶液,乙醇作溶剂
4.下图所示实验操作,正确的是 ()
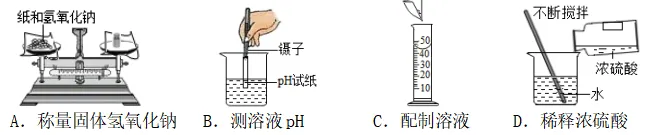
5.中和反应在生产、生活中应用广泛。下列应用的主要原理不涉及中和反应的是( )
A.用盐酸除去铁器表面的铁锈B.氢氧化铝用于治疗胃酸过多
C.熟石灰用于改良酸性土壤D.硼酸用于处理皮肤上沾有的碱
6.下列物质的化学式、俗称、类别完全一致的是
A.Ca(OH)2熟石灰氧化物B.Na2CO3纯碱碱
C.NaOH烧碱碱D.Ag水银单质
7.下图中能正确反映题中所描述的变化事实的( )
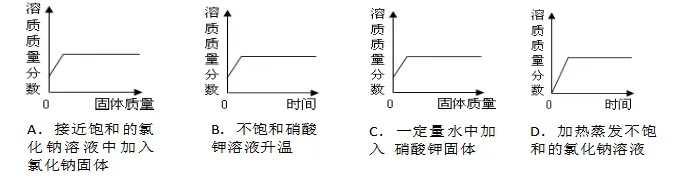
8.不同品牌的洗手液pH一般不同,25℃时四种洗手波的pH如图所示。下列说法错误的是( )
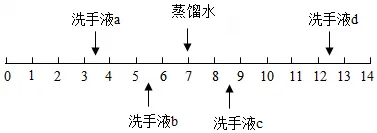
A.洗手液a用蒸馏水稀释后pH增大 B.洗手液b的酸性比a强
C.洗手液c能使石蕊试液变蓝色D.洗手液d和a混合液的pH可能等于7
9.化学与生活、健康、安全息息相关,下列做法不合理的是
A.适量补碘预防甲状腺肿大B.发现家中燃气泄漏,立即打开排气扇通风
C.炒菜时油锅着火,立即盖上锅盖灭火D.进入久未开封的地窖,要做灯火实验
10.如图所示,往固体中加入少量液体。能够使气球先膨胀,一段时间后又能恢复到原状的是(固体的体积变化忽略不计)
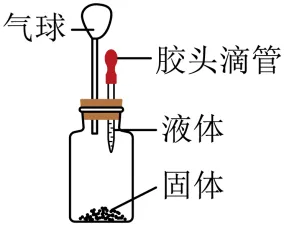
A.硝酸铵固体和水B.氯化钠固体和水
C.石灰石和稀盐酸D.生石灰固体和水
11.以下推理正确的是()
A. 酸中都含有氢元素,所以含有氢元素的化合物一定是酸
B. 碱性溶液能使酚酞试液变红,所以能使酚酞试液变红的溶液一定呈碱性
C. 中和反应生成盐和水,所以生成盐和水的反应一定是中和反应
D. 某固体与稀盐酸反应放出气体,所以该固体物质一定为碳酸盐
12.在Ca(OH)2的饱和溶液中加入下列物质,冷却至室温,溶液的pH没有改变的是 ()
A.CO2B.CaOC.CuCl2D.HCl
13.将密闭并相通的装置放在天平上,调节天平使之平衡(如下图所示)。经过一段时间后,下列有关叙述正确的是( )
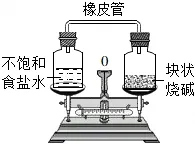
A.指针偏向左,食盐溶液变稀,烧碱潮解
B.指针偏向右,食盐溶液变稀,烧碱潮解
C.指针偏向左,食盐溶液变浓,烧碱潮解
D.指针偏向右,食盐溶液变浓,烧碱潮解
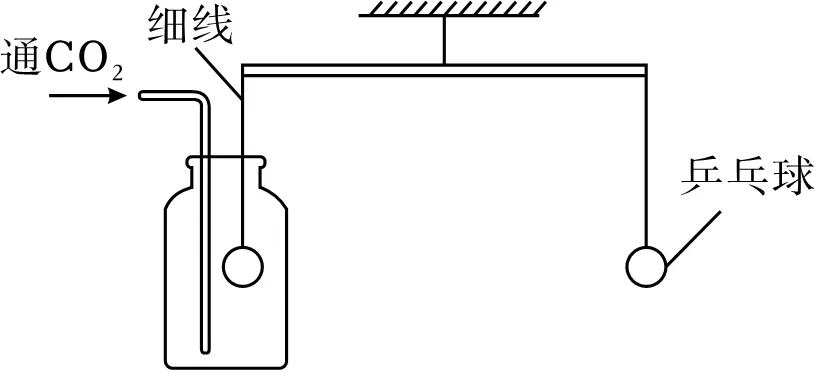
A.通入CO2气体后,左端乒乓球下降
B.整个过程中乒乓球位置始终没有变化
C.倒入浓NaOH溶液后,杠杆逐渐恢复原状
D.其他条件不变,将CO2换成H2会产生同样现象
15. 实验小组用如图装置进行微型实验。按下列表中选项加入试剂,实验时滴入甲,浸有丙的棉花不变红的是( )
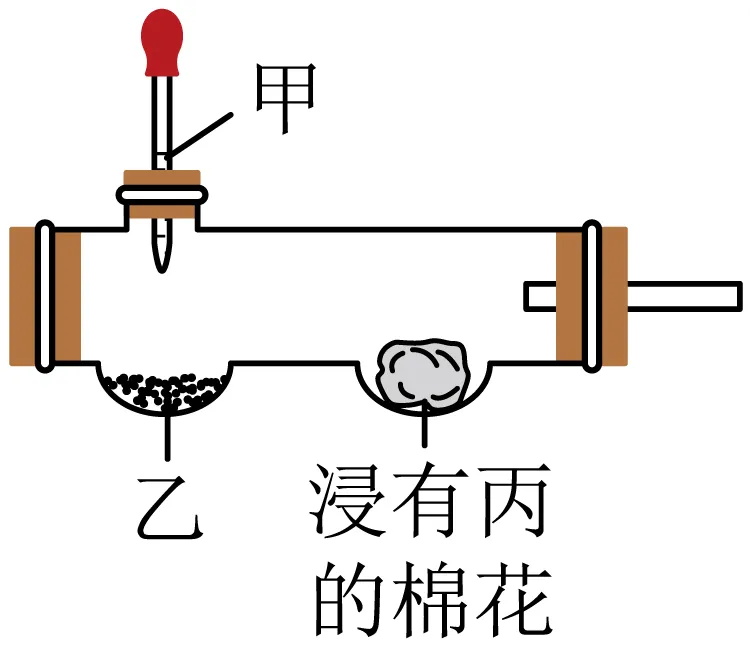
选项 | 甲 | 乙 | 丙 |
A | 石灰水 | 碳酸钠 | 无色酚酞溶液 |
B | 浓氨水 | \ | 无色酚酞溶液 |
C | 稀盐酸 | 石灰石 | 紫色石蕊溶液 |
D | 浓盐酸 | 铁粉 | 紫色石蕊溶液 |
16.下列验证“CO2与NaOH溶液反应”的装置中,不能观察到明显现象的是(装置气密性均良好)
A.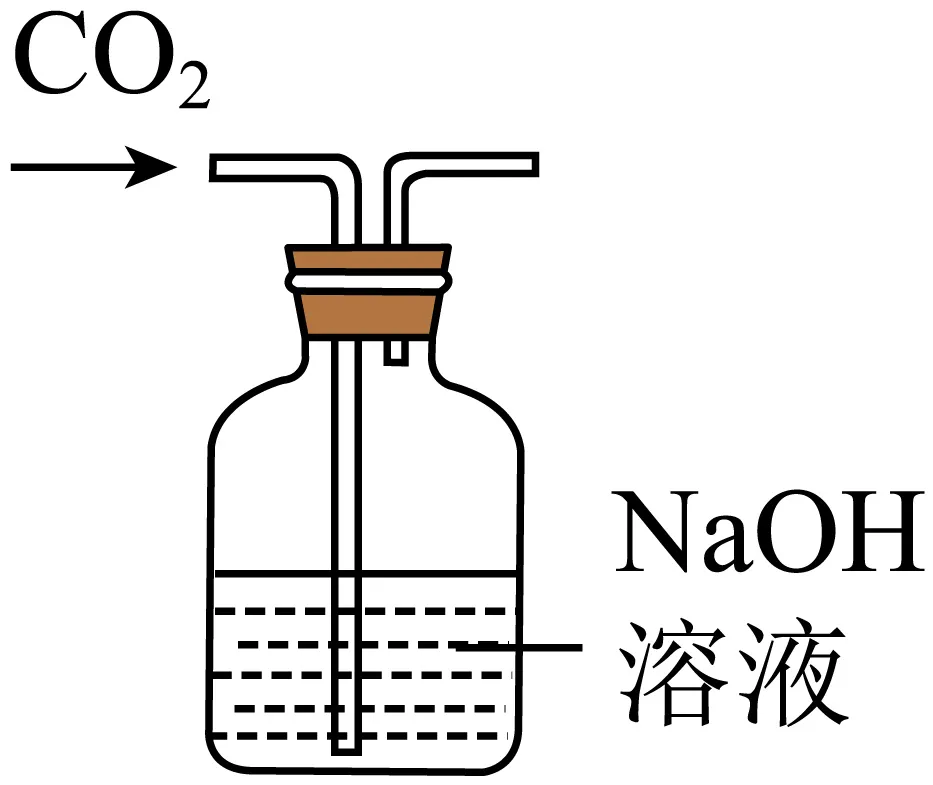 B.
B.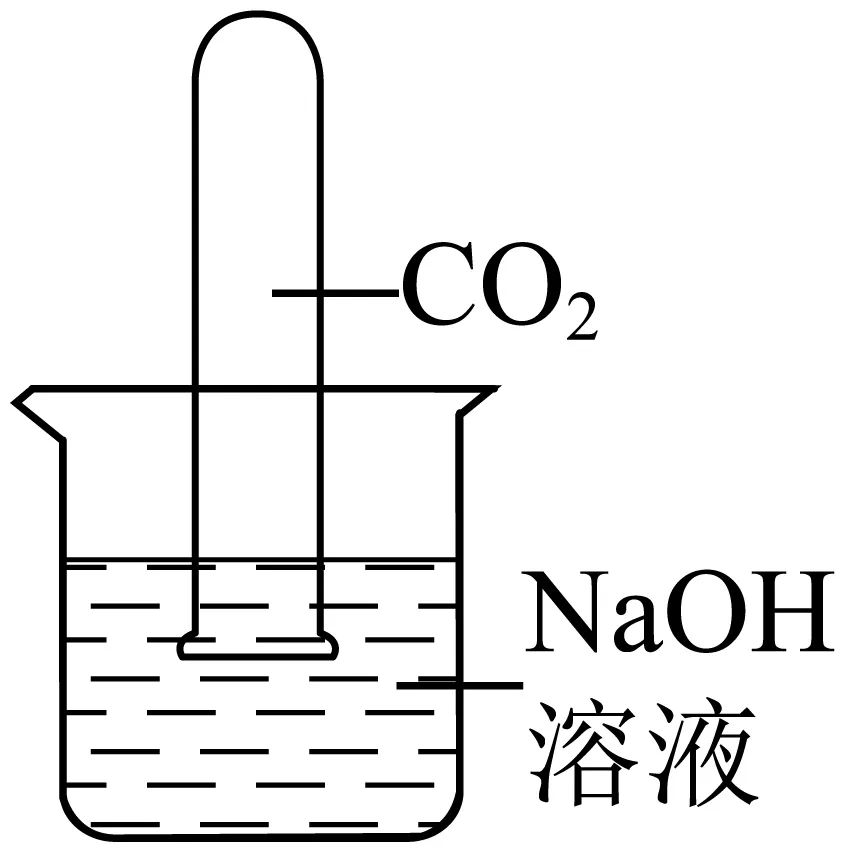 C.
C.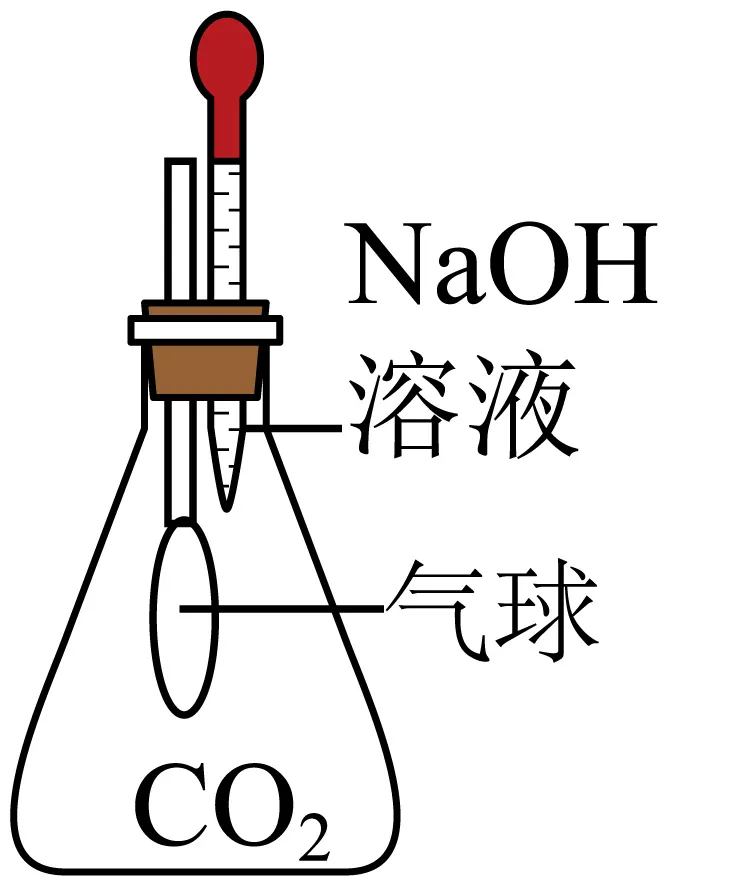 D.
D.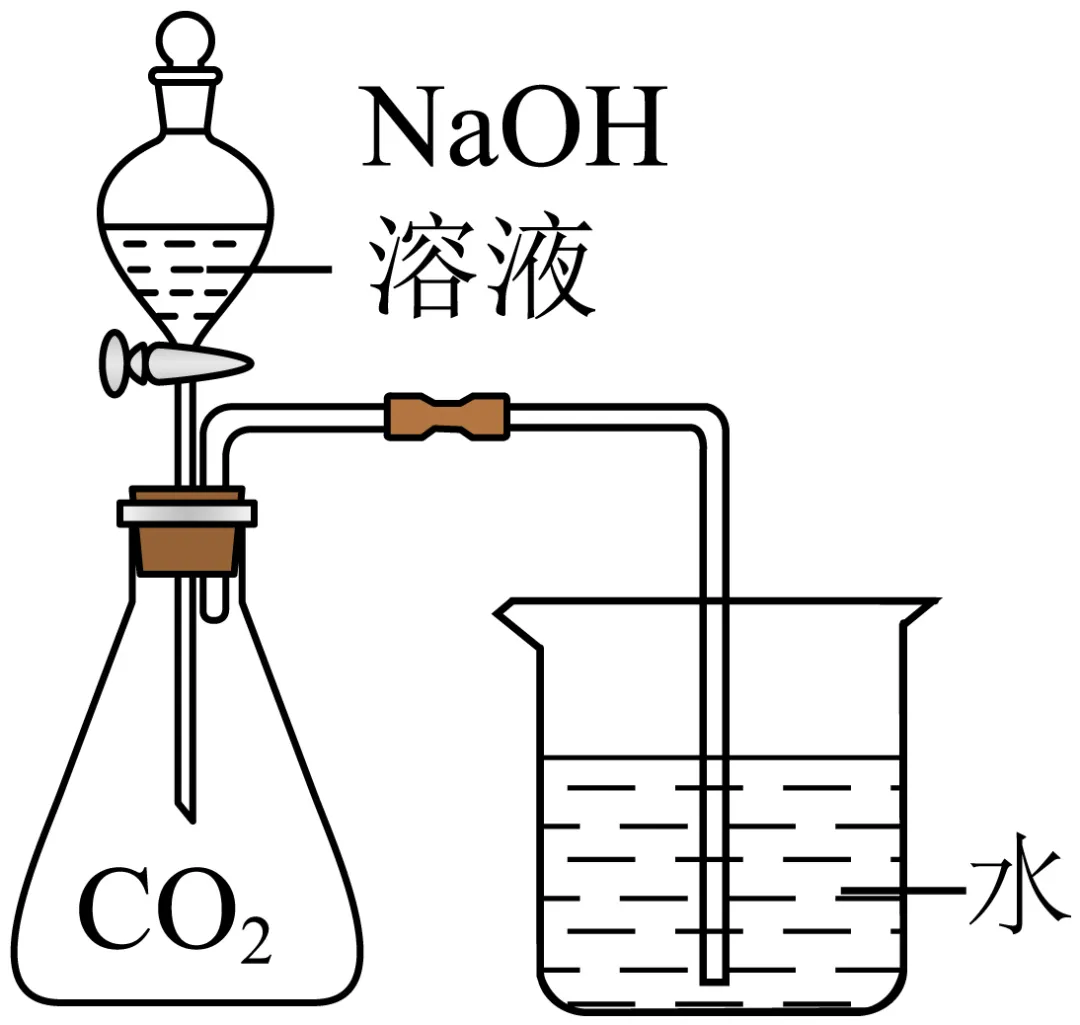
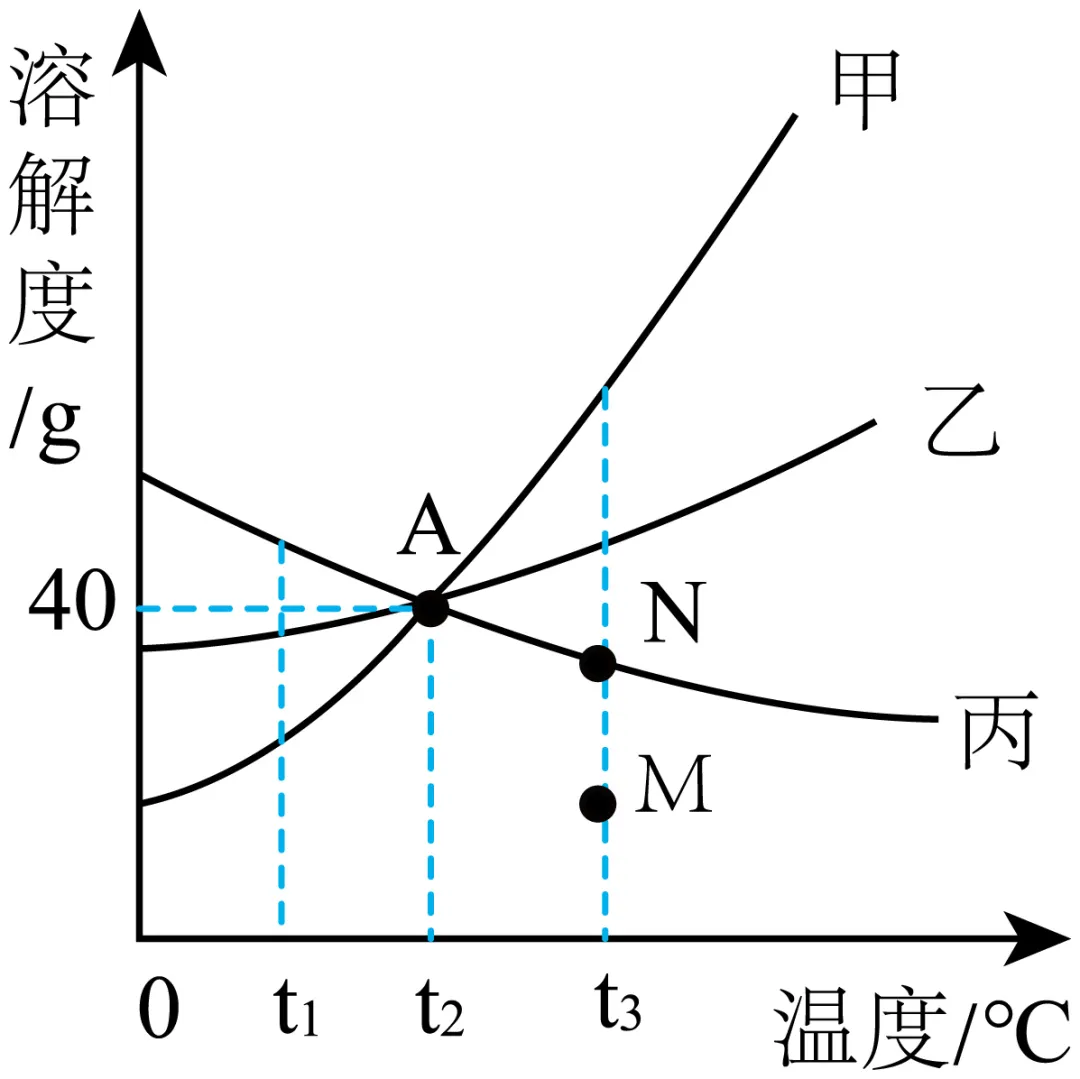
A. t2℃时,将25g乙加入到50g水中,充分溶解,所得溶液中溶质与溶液质量比1:3
B. t3℃时,在等质量的甲、乙、丙三种物质饱和溶液中,所含溶剂最多的是甲
C. 若将在N点的丙溶液转化为M点的丙溶液,可采用的方法是增加溶剂或降低温度
D. t1℃时,将甲、乙、丙三种物质的饱和溶液升温到t3℃,所得溶液的溶质质量分数由大到小的顺序是乙>丙>甲
18.生锈的铁钉放入盛有稀盐酸的密闭容器中,用压强传感器测得容器内气体压强和反应时间的变化曲线如图,说法正确的是( )
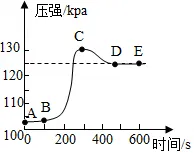
A.CD段压强变化的主要因素是反应速度减慢
B.BC段的化学反应是:Fe+2HCl═FeCl2+H2↑
C.D点反应结束D.E点温度大于A点
19.某小组同学对食品袋内生石灰干燥剂进行如下探究,下列说法正确的是( )
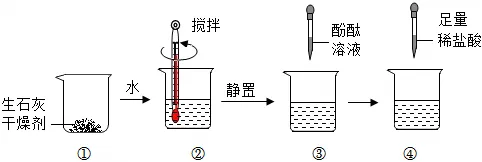
A.②中温度计示数不变可证明干燥剂没有变质
B.③中溶液变红可证明干燥剂中含有氧化钙
C.④中有气泡产生可证明干燥剂中含有碳酸钙
D.氢氧化钠固体可代替生石灰作食品干燥剂
20.将部分变质的氢氧化钠样品溶于水,向所得溶液中逐滴加入稀盐酸至过量,生成的与加入稀盐酸的质量关系如图所示(提示:碳酸钠与稀盐酸的反应分两步进行:第一步为;第二步为)。下列说法正确的是()
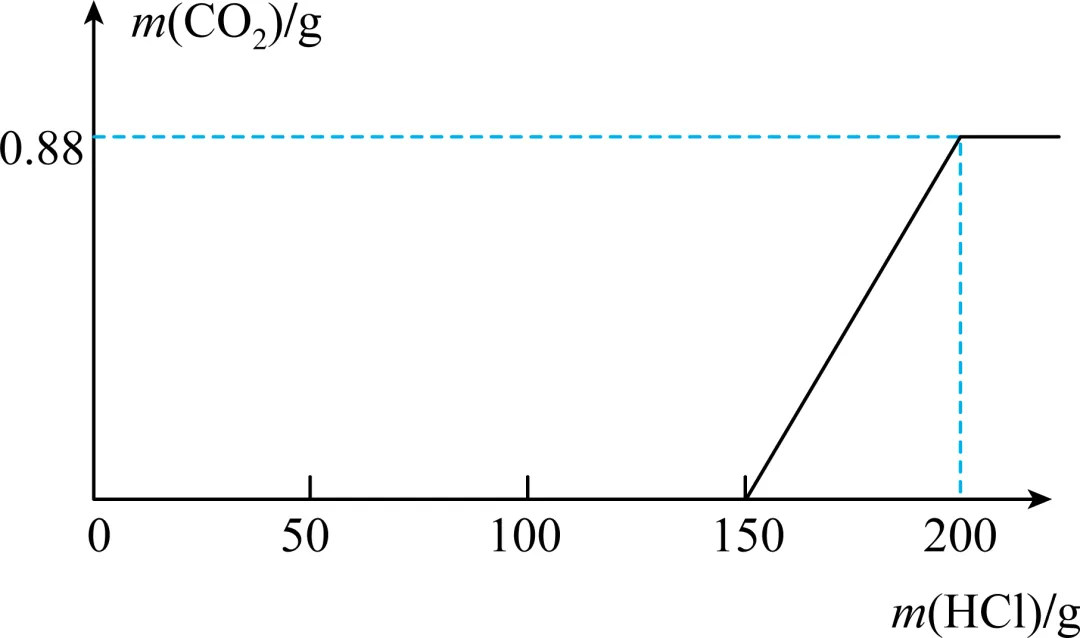
A.实验过程中共发生了两个反应
B.稀盐酸中溶质质量分数为1.46%
C.加入稀盐酸为150g时,溶液中的溶质为NaCl和
D.所取的氢氧化钠样品中,NaOH与的质量比为
二、填空题(本题共3小题,共28分)
21.(8分)(1)天然水是混合物,含有较多的Ca2+、Mg2+的水被称为硬水,日常生活中可通过煮沸方法降低水的硬度。硬水煮沸时会结水垢,水垢的主要成分为碳酸钙和氢氧化镁。用食醋除水垢时,发生的反应为
Mg(OH)2 + 2CH3COOH ===(CH3COO)2Mg + 2H2O 和。
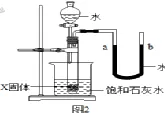
(2)如图2所示实验,将水加入到试管中,观察到A液面下降,B液面上升,
(3)饱和石灰水变浑浊,则X固体可能为、NaOH、CaO
(写出两种不同物质的化学式)。
(3)从H、O、C、Na、Cl、Ca六种元素中选择一种或多种按要求填写下列物质的化学式:
①可用作治疗胃酸过多的盐是;②可用于金属除锈的酸是
③可用于改良酸性土壤的碱是;④可作食品干燥剂的氧化物是。
22.(6分)下列框图中的物质均为初中化学常见的物质,其中A是建筑材料的主要成分,B属于氧化物,如图是它们之间的相互转化关系(部分产物略去).请回答:
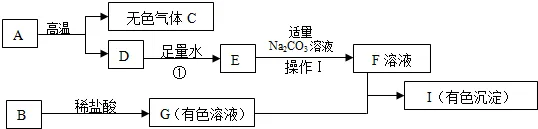
(1)写出下列物质的名称或化学式:A.(化学式);E.(名称)。
(2)若I是红褐色沉淀,请写出G+F→I的化学方程式:;
写出E + Na2CO3 →F的化学方程式:。
23.(14分)(一)小海用如图所示的思维导图总结了稀盐酸的五条化学性质,分析图示并回答问题:
(1)该同学向稀盐酸中滴入紫色石蕊溶液,发现紫色石蕊溶液由紫色变成 色;
(2)试写出用稀盐酸除铁锈的化学方程式 ;
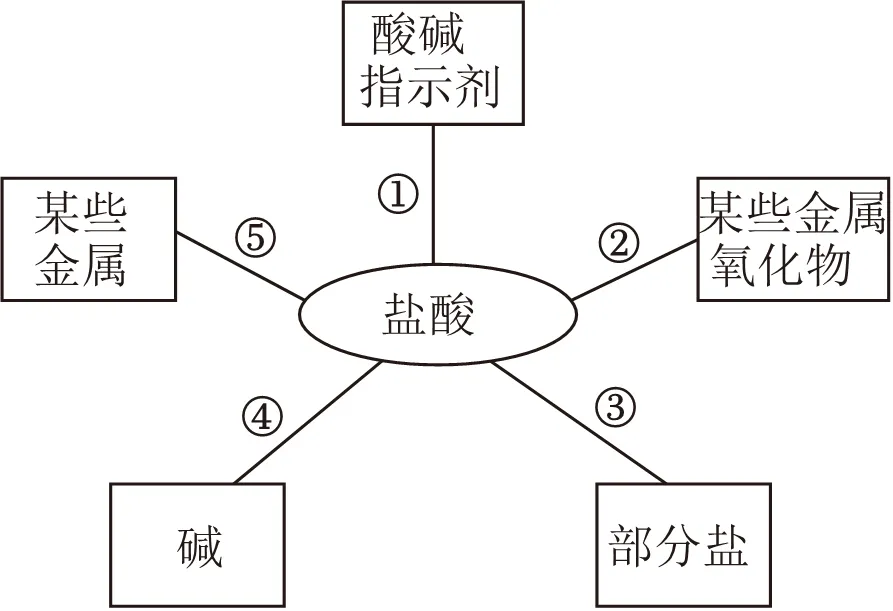 (填字母);
(填字母);
A.MgB.CO2C.Na2CO3D.Mg(OH)2
(4)小海把稀盐酸和氢氧化钠溶液混合后,发现无明显现象,再向溶液中滴入无色酚酞溶液,观察到无色溶液变成红色,则此时混合溶液中含有的微粒有(填化学符号,不考虑酚酞)。
(二)化学兴趣小组的同学在探究碱溶液的化学性质时,对碱的有关化学性质进行梳理和总结,并预测了陌生物的化学性质。请完成下列问题。
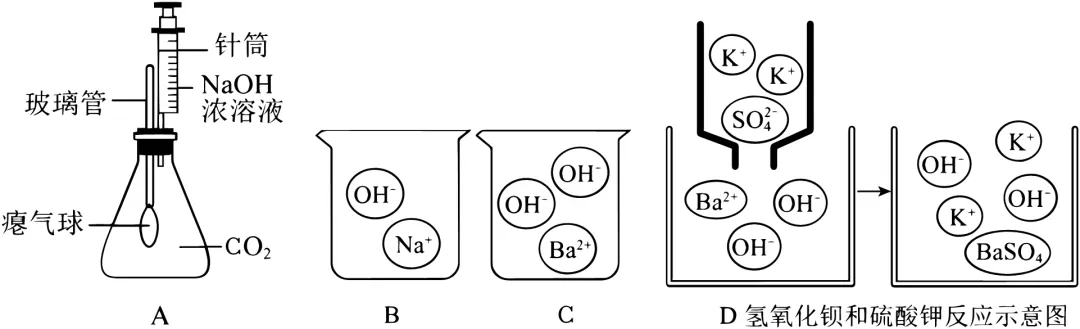
(1)基于宏观视角分析碱的化学性质:
①实验A中,推入NaOH浓溶液后,可观察到的现象是 。
②烧杯B和烧杯C中分别盛有氢氧化钠溶液和氢氧化钡溶液,向其中分别加入硝酸铜溶液,出现的相同实验现象是 。从微观角度分析上述现象相同的原因是二者的水溶液都含有 。(填化学符号)
(2)基于微观视角分析碱的差异性:向烧杯C中滴加硫酸钾溶液,反应的微观示意图如图D所示,该反应的现象为 ,化学方程式为 ;而向烧杯B中滴加硫酸钾溶液,无明显现象。
(3)基于“结构决定性质”预测陌生物质的化学性质:烧杯E中盛有某溶液,请根据所含的微粒,预测该溶液能与下列试剂发生化学反应的有 (填字母序号)。
A.硫酸钠溶液B.氯化钾溶液C.稀硫酸D.硝酸钠溶液
三、实验题(本题共2个小题,共26分)
24.(14分)在学习了常见的酸和碱后,某化学兴趣小组的同学围绕“酸碱中和反应”,在老帅引导下开展实验探究活动,请你参与下列活动。
【实验探究】将氢氧化钾溶液与稀硫酸混合,观察不到明显现象,为证明氢氧化钾溶液与稀硫酸发生了反应,三位同学进行了以下实验。
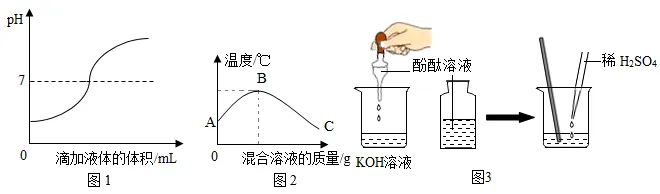
(1)测定溶液pH变化的方法
甲同学在实验过程中测得pH变化如图1所示,则该同学是将(填字母序号)。
a.氢氧化钾溶液滴入稀硫酸中 b.稀硫酸滴入氢氧化钾溶液中
(2)测混合过程中的温度变化
乙同学在实验过程中测得反应混合溶液的温度变化如图2所示,说明稀硫酸与氢氧化钾溶液发生的反应是(填“放热”或“吸热”)反应。
(3)借助于中和反应有水生成
丙为验证中和反应有水生成,小组同学在老师的指导下,进行如图所示的三个实验。
已知:①变色硅胶吸水后由蓝色变为红色;
②无水醋酸(液体)与氢氧化钠反应生成醋酸钠和水。
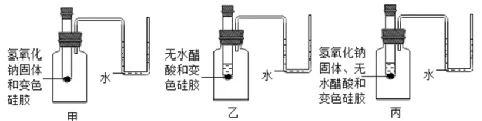
证明无水醋酸与氢氧化钠反应有水生成的现象是。
(4)借助于酸碱指示剂
丁同学通过图3所示实验,他观察到溶液由红色变成无色,也证明氢氧化钾溶液与稀硫酸发生了化学反应,反应的化学方程式为。
【提出问题】针对反应后溶液中溶质的成分,大家纷纷提出了猜想。
【猜想与假设】猜想一:只有K2SO4;猜想二:;猜想三:有K2SO4和KOH
行实验】为了验证猜想,学习小组选用Fe2O3粉末、BaCl2溶液,进行如下探究:
实验 方案 | 实验操作 | 实验现象 | 实验结论 |
方案一 | 取少量反应后的溶液于试管中,加入Fe2O3粉末 | ① | 溶液中有H2SO4猜想二正确 |
方案二 | 取少量反应后的溶液于试管中,滴加BaCl2溶液 | ②产生白色沉淀 | 溶液中有H2SO4,猜想二正确 |
【实验结论】通过探究,同学们一致确定猜想二是正确的。
【评价与反思】
③丁同学针对上述方案提出疑问,认为方案二是不合理的,理由是。
④同学们经过反思与讨论,最后认为方案一中的Fe2O3粉末可以用下列的某些物质代替,也能得到同样的实验结论,请你选出可用药品的字母序号。
A.MgB.CuOC.KClD.Na2CO3
25.(12分)(1)如图是对 20℃一定质量甲的溶液进行恒温蒸发的结晶实验过程,请回答:
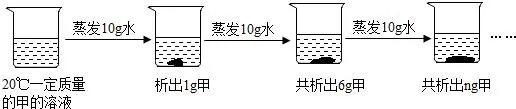
①蒸发前原溶液是(填“饱和”或“不饱和”)溶液,n 的数值是 ,该温度下,甲溶液的溶解度是 。
②依据上述实验,你认为甲的溶解度随温度变化的趋势是(填字母)的。
A.随温度升高而增大 B.随温度升高而减小 C.无法判断
③溶液中溶质质量分数的比较:第 2 个烧杯 第 3 个烧杯(填“>”、“=”或“<”)。
(2)若把硝酸钾的不饱和溶液变为饱和溶液,下列有关说法正确的是(填序号,下同)。
A.溶剂的质量一定变小B.溶质的质量可能不变
C.溶质的质量分数一定变大D.溶液的质量一定变小
E.该饱和溶液还可以溶解其他物质
(3)现要配制溶质质量分数为35%的硝酸钾溶液100g作为“水培溶液”,操作如图所示。
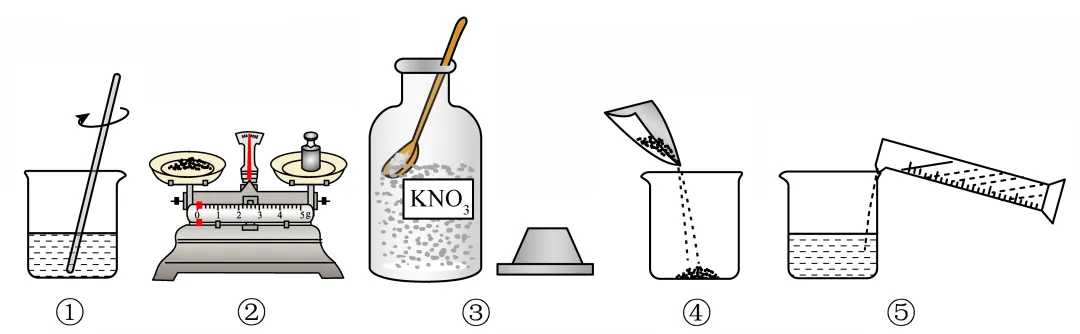
①配制步骤正确的 (填序号)。
A.③②④⑤①B.①③②④⑤
C.③④②⑤①D.③②①⑤④
②下列操作一定会导致配制溶液溶质的质量分数偏小的是 (填序号)。
A.称量时,左盘放砝码(1g以下用游码)
B.量取水时俯视读数
C.称量好的氯化钠未全部转移到烧杯中
D.溶解完全后,转移时部分液体洒出
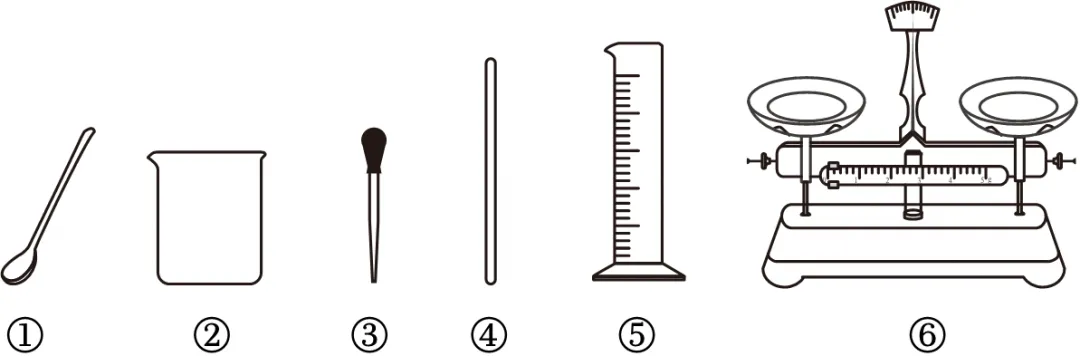
③将50g溶质质量分数为35%的硝酸钾溶液稀释为17.5%,需要加水的质量为 ,需使用如图中的 (填序号)。
四、计算题(本题包括1小题,6分)
26. (6分)化学兴趣小组整理药品时,发现一瓶标签受损的稀盐酸。为测定该稀盐酸的溶质质量分数,同学们进行了下图的实验(所选石灰石中的杂质不溶于水,也不与其他物质反应;生成气体全部逸出)。

请完成下列问题:
(1)生成二氧化碳的质量为g。
(2)计算稀盐酸的溶质质量分数(写出计算过程)。
九年级化学第一次中考模拟考试试题
参考答案
一、选择题(每题2分,共40分)
1—5BDCDA6—10 CABBD11—15 BBDCA16—20 ADBCB
二、填空题(本题共3个小题,共28分)
21.(8分)(1) CaCO3+ 2CH3COOH =(CH3COO)2Ca + H2O+ CO2↑(2分);
(2)NaOH、CaO(2分);
(3)① NaHCO3(1分)② HCl(1分)③Ca(OH)2(1分)④CaO(1分)。
22.(6分)(1) CaCO3(1分);氢氧化钙(1分);
(2)FeCl3 + 3NaOH= Fe(OH)3↓+ 3NaCl(2分);
Ca(OH)2 +Na2CO3 = CaCO3↓ + 2NaOH(2分)。
23.(14分)(一)(1)红(1分);
(2)Fe2O3+6HCl═2FeCl3+3H2O(2分);
(3)C(1分);
(4)Na、OH-、Cl-、H2O(2分)。
(二)(1)①瘪气球胀大(1分); ②都有蓝色沉淀生成(1分);OH﹣(1分);
(2)有白色沉淀生成(1分);Ba(OH)2+K2SO4=BaSO4↓+2KOH(2分);
(3)AC(2分)。
三、实验题(本题共2个小题,共26分)
24.(14分)(1)a(1分);
(2)放热(1分);
(3)丙中变色硅胶变红,甲乙中变色硅胶不变红(2分);
(4)2KOH+H2SO4=K2SO4+2H2O(2分);有K2SO4和H2SO4(2分);
①固体溶解,溶液成黄色(2分);
③若只有K2SO4 ,加入BaCl2溶液也会产生白色沉淀(2分);
④ABD(2分)。
24.(12分)(1)①饱和(1分);50g(2分);②C(2分);③=(1分);
(3)BE(2分);
(3)C(1分)50g(1分);②③④⑤(2分)
四、计算题(6分)
26.(1)4.4 ;(1分)
(2)解:设稀盐酸中HCl的质量为x…………………………………………… 1分
CaCO₃+2HCl=CaCl₂+H2O+CO₂↑……………………1分
7344
x4.4g………… 1分
73/44=x/4.4g x=7.3g…… 1分
溶质质量分数=7.3g/100g×100%=7.3%…………………………… 1分
答:稀盐酸的溶质质量分数为7.3%。







