今天为大家整理了物质元素组成、核外电子排布、离子与物质分类等高频考点,都是初中化学核心考查内容,知识点系统全面,适合收藏背诵,希望能帮助大家稳步提分。
(续上篇)
三、辨别物质的元素组成
1、元素(地壳中前五位:氧硅铝铁钙)
⑴.概念:元素是具有相同核电荷数(质子数)的同一类原子的总称。
◆元素只讲种类,不讲个数;
◆原子既讲种类又讲个数。
⑵.元素符号的书写:“一大二小”。
⑶.元素符号的意义:
①表示某种元素,如:H表示氢元素;
②表示该元素的一个原子,
如:H表示一个氢原子;
③在元素符号前加数字,表示几个原子;
如:3H只能表示3个氢原子;
◆注:金属、固体非金属、稀有气体元素,还表示一种物质,如:Fe表示铁元素、一个铁原子、铁这种物质;
⑷.元素的分类:
① 分为金属、非金属、稀有气体元素。
② 非金属元素:分为气态、液态、固态非金属。
⑸.元素周期表:(俄国化学家门捷列夫:元素周期表)
①7个周期16个族,同一周期,电子层数相同,即:周期数=电子层数;
同主族元素,最外层电子数相同,所以同主族元素化学性质相似。
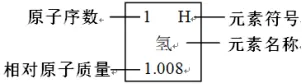
②元素方格提供的信息:原子序数、元素符号、元素名称、相对原子质量。
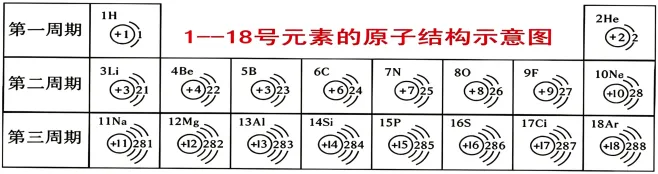
2、核外电子分层排布规律:
1-20号元素顺序:氢氦锂铍硼,碳氮氧氟氖,钠镁铝硅磷,硫氯氩钾钙
⑴.金属元素:最外层电子<4,不稳定,易失电子,带正电,形成阳离子;
⑵.非金属元素:最外层电子>=4,不稳定,易得电子,带负电,形成阴离子;
⑶.稀有气体元素:最外层电子=8(He=2),稳定结构,不容易得或失电子。
◆注:
①元素种类由质子数(核电荷数)决定;(质子数相同,元素种类就相同)
②元素化学性质由最外层电子数决定;(最外层电子数相同,化学性质相似)
3、离子:(带电的原子或原子团)
⑴.表示方法及意义:
如Fe3+:一个铁离子带3个单位正电荷。
⑵.离子所带的电荷数及电性跟化合价相同。
◆如:Mg元素的化合价是+2价,则镁离子(Mg2+)带2个单位的正电荷。
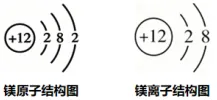
⑶.离子与原子结构图的区别:
①原子结构图:质子数=电子数
②离子结构图:质子数≠电子数
⑷.原子团(也叫做根):
氢氧根(OH-) , 硝酸根(NO3-) ,
碳酸根(CO32-), 硫酸根(SO42-),
铵根(NH4+)
4、物质的分类:
⑴.纯净物和混合物:(按物质种类来分)
①纯净物:只含一种物质。
◆如:水、冰水、蒸馏水、氧气、液态氧气、氯化钠、铜、水银等。
②混合物:含两种或两种以上物质。
◆如:空气、海水、矿泉水、澄清石灰水、碘酒、加盐碘、合金、溶液。
⑵.两者的区别:纯净物可用一个化学式表示所有成分,如:冰水(H2O);但混合物不能,如:空气、海水等。
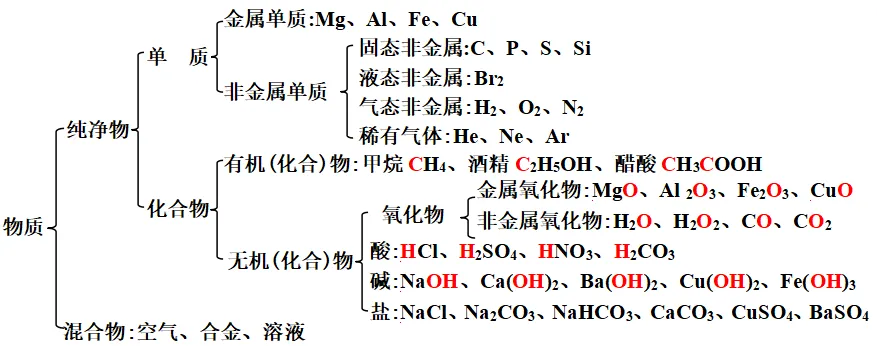
⑶.单质和化合物:(按元素种类分)
①单质:由一种元素组成的纯净物(化学式中只有一种元素符号)。
◆如:铝(Al)、 金刚石(C) 、氧气(O2)等。
②化合物:由两种或两种以上元素组成的纯净物(化学式有两种或以上元素符号)。
◆如:二氧化碳(CO2)等。
③氧化物:含两种元素且其中一种元素是氧元素的化合物。
◆如:二氧化碳(CO2)、氧化镁(MgO) 等是氧化物,但氧气(O2)、氯酸钾(KClO3)等不是氧化物。
四、跨学科实践活动:探究水的组成
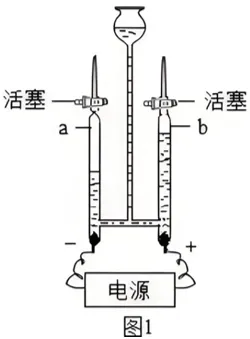
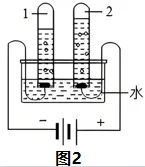
⑴.电解水的实验现象:负氢2,正氧1(体积比)。(氢1氧8质量比)
◆正极产生的气体能使带火星的木条复燃:是O2;
◆负极产生的气体能燃烧,火焰呈淡蓝色:是H2;
 |  |
⑵.电解水实验的结论:
①水是由氢元素和氧元素组成的。
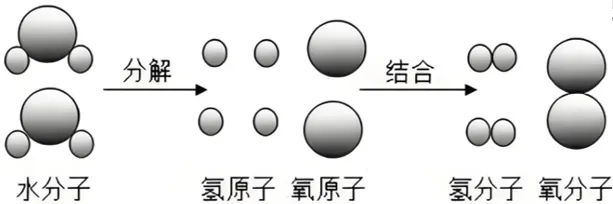
②一个水分子是由2个氢原子和1个氧原子构成的。
⑶.化学方程式:2H2O通电 2H2↑+ O2↑
【文字表达式:水通电氢气 + 氧气】
◆该反应中,发生改变的微粒:水分子;没有改变的微粒(最小微粒)是:氢原子、氧原子
⑷.注意:
①物质都是由元素组成的;
◆如:水是由氢元素和氧元素组成,铁是由铁元素组成。
②物质是由分子、原子、离子等微粒构成的;
◆如:水由水分子构成;铜由铜原子构成;氯化钠由钠离子和氯离子构成。
③分子是由原子构成的;
◆如:一个水分子由两个氢原子和一个氧原子构成。
以上就是初中化学物质组成全部核心考点总结。
🔰 往期精彩合集
知识整理不易,觉得有用可以点赞+收藏,也欢迎转发分享给身边正在学习化学的同学!后续将持续更新初中化学全册单元必背考点,敬请关注!✨








