中考临近,将陆续为各位同学整理各科必考知识点。
本期内容为:化学第四期:金属与金属矿物的必考知识点
知识点1金属材料
(1)金属的物理性质及用途
性质 | 用途 |
导电性 | 铜丝、铝丝作导线 |
导热性 | 用铁锅炒菜 |
延展性 | 铝压成铝箔等 |
有光泽 | 金、银作饰品等 |
(2)金属之最
①地壳中含量最高的金属——铝;
②人体中含量最高的金属——钙;
③目前世界年产量最高的金属——铁;
④导热性、导电性最好的金属——银;
⑤熔点最高的金属——钨
(3)合金
①定义:合金是在纯金属中加热熔合某些金属或非金属制得的具有金属特征的物质
②性能:一般情况下,与组成它的纯金属相比,合金的熔点更低、强度和硬度更大,抗腐蚀性更好
知识点2金属的化学性质
(1)与氧气反应
①条件:大多数金属能与氧气发生反应,但反应的难易程度不同
②通式:金属+氧气→金属氧化物
③举例:
a.镁:镁条在空气中剧烈燃烧,发出耀眼的白光,生成白色固体
发生反应的化学方程式:2Mg+O2 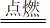 2MgO
2MgO
b.铝:常温下铝在空气中与氧气反应,其表面生成一层致密的氧化铝(Al2O3)薄膜,从而阻止铝进一步被氧化,因此,铝具有良好的抗腐蚀性能
发生反应的化学方程式:4Al+3O2=== 2Al2O3
c.铁:在氧气中剧烈燃烧,火星四射,放出大量的热,生成黑色固体
发生反应的化学方程式:3Fe+2O2 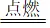 Fe3O4
Fe3O4
d.铜:在空气中加热,表面生成黑色固体
发生反应的化学方程式:2Cu+O2 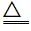 2CuO
2CuO
e.金:化学性质稳定,即使在高温条件下也不与氧气反应
(2)与酸反应
①条件:金属的活动性必须排在H(氢)之前(K、Ca、Na除外)
②通式:活泼金属+酸→盐+氢气
③举例:
a.镁与稀盐酸:Mg+2HCl === MgCl2+H2↑
现象:反应剧烈,有大量气泡产生
b.铁与稀硫酸:Fe+H2SO4 === FeSO4+H2↑
现象:有气泡产生,溶液由无色变为浅绿色
(3)与某些可溶性盐溶液反应
①条件:前置后(K、Ca、Na除外),盐必须可溶
②通式:金属+可溶性盐溶液→新金属+新盐
③举例:
a.铁与硫酸铜溶液:Fe+CuSO4===FeSO4+Cu
现象:铁表面有红色固体析出,溶液由蓝色变为浅绿色
b.铜与硝酸银溶液:Cu+2AgNO3=== Cu(NO3)2+2Ag
现象:铜表面有银白色固体析出,溶液由无色变为蓝色
(4)金属活动性顺序

金属活动性顺序的一般规律:
a. 金属的位置越靠前,它的活动性就越强;
b. 位于氢前面的金属能置换出稀盐酸、稀硫酸中的氢;
c. 位于前面的金属能把位于后面的金属从它们化合物的溶液里置换出来(K、Ca、Na除外)
知识点3金属资源的利用和保护
(1)金属矿物
①地球上的金属资源除了金、银等有单质形式存在外,金属多以化合物的形式存在。
②常见的几种金属矿物及主要成分
金属矿物 | 赤铁矿 | 磁铁矿 | 铝土矿 |
主要成分 | Fe2O3 | Fe3O4 | Al2O3 |
(2)铁的冶炼(高炉炼铁)
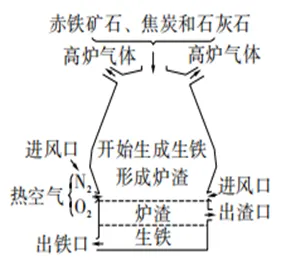
①原料:赤铁矿石、焦炭、石灰石、空气
②主要原理:在高温下,利用炉内反应生成的一氧化碳把
铁从氧化铁里还原出来
③产品:生铁(属于混合物)
④炼铁过程中发生的主要化学反应:
a.一氧化碳与氧化铁反应:3CO+Fe2O3 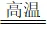 2Fe+3CO2
2Fe+3CO2
b.焦炭参与的反应:C+O2 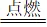 CO2 、 CO2+C
CO2 、 CO2+C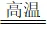 2CO
2CO
⑤焦炭的作用:a.生成CO;b.燃烧提供热量
(3)金属资源保护
①金属的腐蚀与防护
Ⅰ. 探究铁钉生锈的条件
【实验装置】
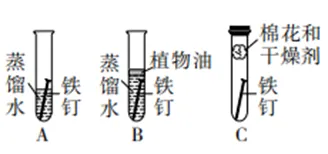
【实验现象】一周后,试管A中铁钉生锈,且接近水面与空气交界处的铁钉锈蚀严重,试管B、C中铁钉未生锈
【实验分析及结论】对比A、B可知,铁钉生锈需要与氧气(或空气)接触;对比A、C可知,铁钉生锈需要与水接触
Ⅱ.防止铁制品腐蚀
a.防锈原理:破坏铁锈蚀的条件,使铁制品与水或氧气(或空气)隔绝
b.防锈方法:保持铁制品表面清洁干燥;在铁制品表面覆盖保护层,如镀铬等;改变内部结构,制成耐腐蚀的合金,如不锈钢
②保护金属资源:防止金属腐蚀;回收利用废旧金属;有计划、合理地开采金属矿物;寻找金属的代用品
易错知识点整理(选择题要特别注意):
1.合金属于金属材料。
2.为防止铁生锈,只需使铁制品与水或氧气(或空气)隔绝。
3.真金不怕火炼说明金的化学性质稳定,不能说明金的熔点高。
4.铝具有良好抗腐蚀性的原因是铝在常温下与氧气反应生成一层致密的氧化铝薄膜,阻止内部的铝进一步被氧化。
【为及时收到每期更新内容,请添加 关注、收藏+分享  】
】





