Spontaneous Reaction
化学万事屋live

今天的封面特意选了「竹子」,虽然与液流电池的内容不怎么相关,但是我喜欢,尤其是这几天(所谓“宁可食无肉,不可居无竹”,出自苏东坡的诗,昨天和老江在群里蛐蛐,粽子给起的副标题)。
好了,抒发完开始干活。这篇文章梳理的是液流电池,在2025年的河南卷和山东卷中均有考查。关于液流电池,鲁科版教材是以全钒液流电池为例引出的,其应用重在储能。在我看来,液流电池的储液罐就相当于电池的“移动硬盘”,可以按需扩容。
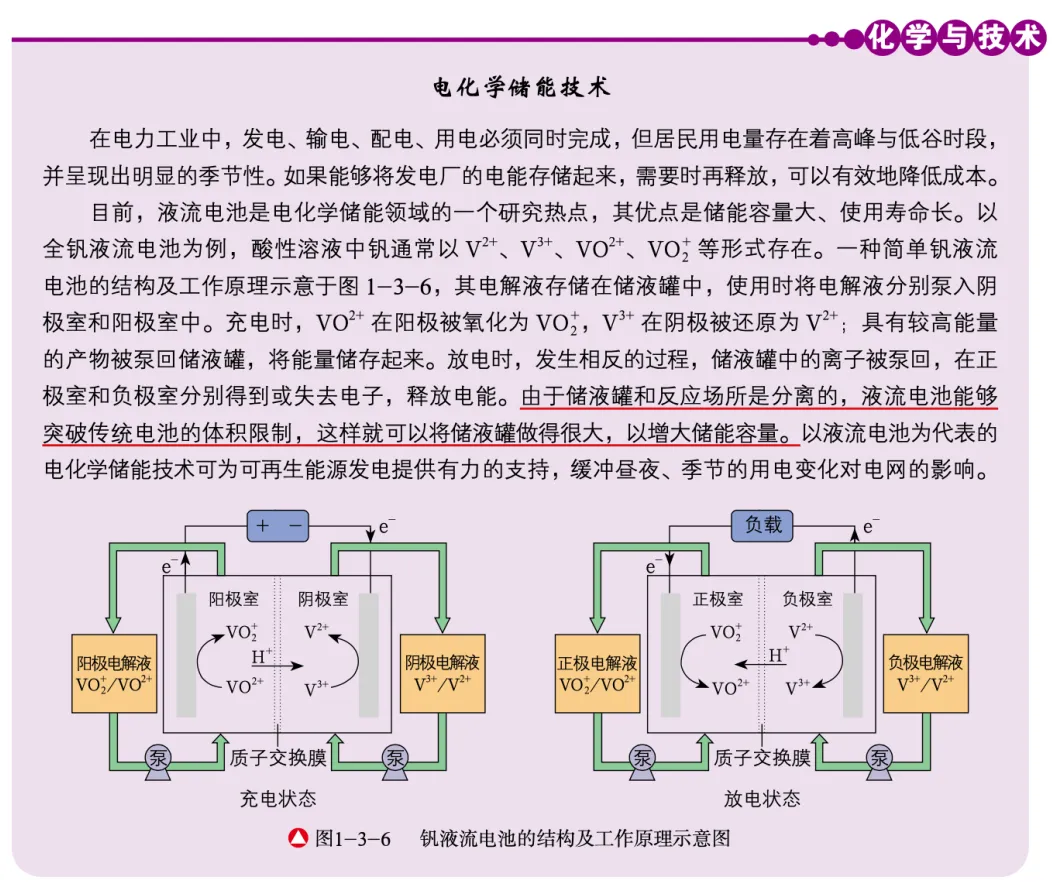
通常来说,液流电池会涉及充电、和放电两个过程。有些题目只考一个,比如河南卷考的是电解池,这种情况下电极作阴极,还是阳极,就比较好判断。
有些题目是两个都考,比如山东卷的全铁液流电池,这时就可能需要我们根据物质的变化来区分充电过程和放电过程。接下来就以山东卷为例,来梳理如何区分以上两个过程(题目本身不难,但重要的是角度)。
07 山东卷 | 全铁液流电池
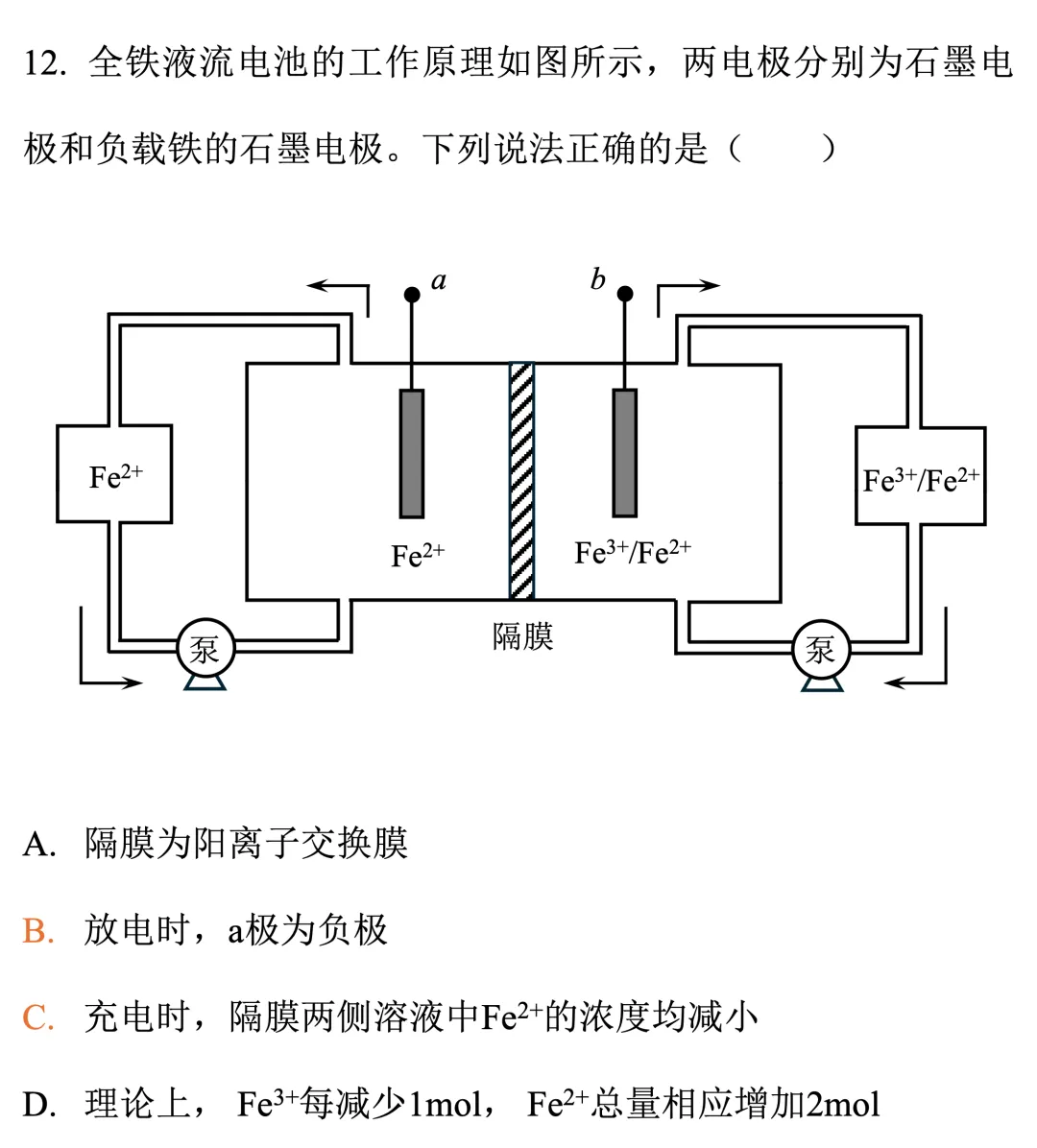
根据图示,a极进行Fe和Fe2+的相互转化,b极进行Fe3+和Fe2+的相互转化。当a极进行氧化反应时,b极进行还原反应,即Fe→Fe2+对应Fe3+→Fe2+。反之亦然,当a极进行Fe2+→Fe时对应b极进行Fe2+→Fe3+。这个逻辑很简单,但关键是,哪组氧化-还原反应对应放电过程呢?

放电要选自发的!根据氧化性的强弱,Fe3+可以氧化Fe,2Fe3++Fe=3Fe2+能自发进行,因此该总反应对应放电过程,反过来,3Fe2+=2Fe3++Fe为充电时的总反应。根据放电时2Fe3+~3Fe2+,每减少1mol Fe3+,理论上增加1.5mol Fe2+(D错误)。
此外,中间隔膜需为阴离子交换膜,防止Fe3+进入左室直接与负极上的Fe反应。想想看,如果是阳离子膜,那直接乱成一锅粥了……所谓原电池,氧化反应和还原反应还是分开的好(不是说不行)。
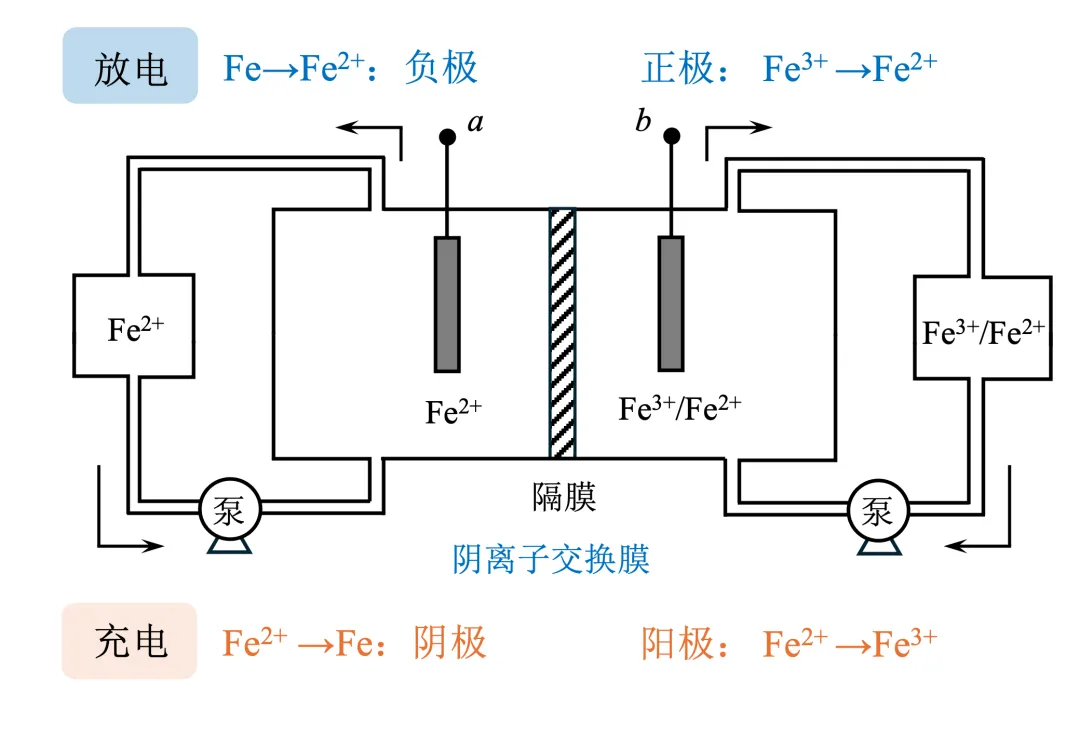
小结:关于液流电池,自发的氧化还原反应是判断放电过程的关键。从氧化还原能力→自发性,这条逻辑线其实很长:氧化还原能力→电极电势→电池的电动势E→ΔG与E的关系(能斯特方程)→自发性,高中化学没办法说清楚的细节,在大学里等你,以下是人教版教材的截图。

最后,祝各位假期愉快,劳动节不需要劳动最好!
🐳敬上~~~







