Active Hydrogen
化学万事屋live
这篇文章分享2025年四川卷对电化学的考查,其命题来源为以下论文:

同样是NO3-还原为NH3,这里涉及到了还原过程中H原子的介入,额……好好的,为什么要提H原子呢?这其中的历程如何?和之前一样,接下来先解析题目,然后是反应历程的梳理。
06 四川卷 | 真题解析
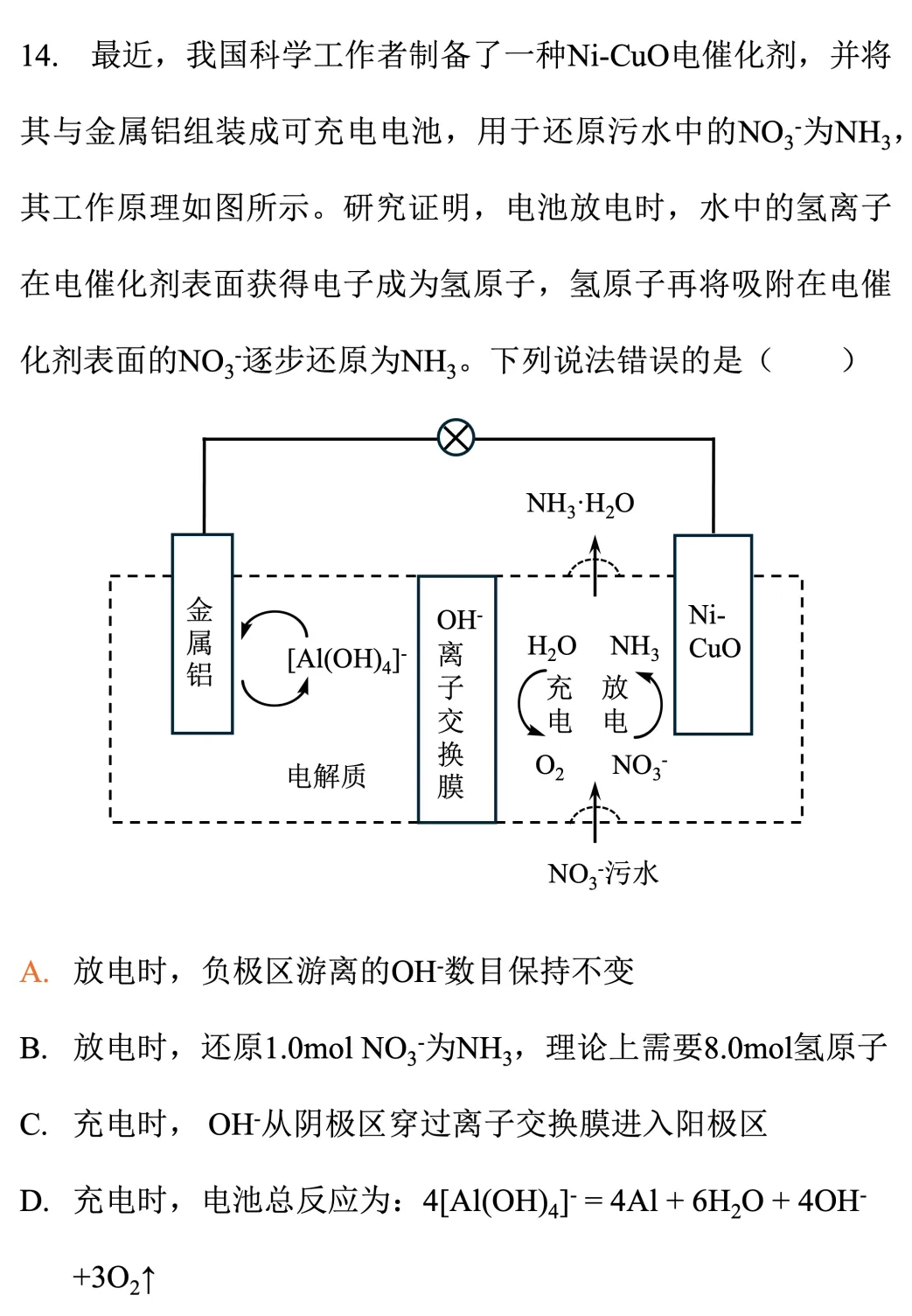
充电时:H2O→O2为氧化反应,Ni-CuO电极作阳极。放电时:NO3-还原为NH3,Ni-CuO电极为正极。
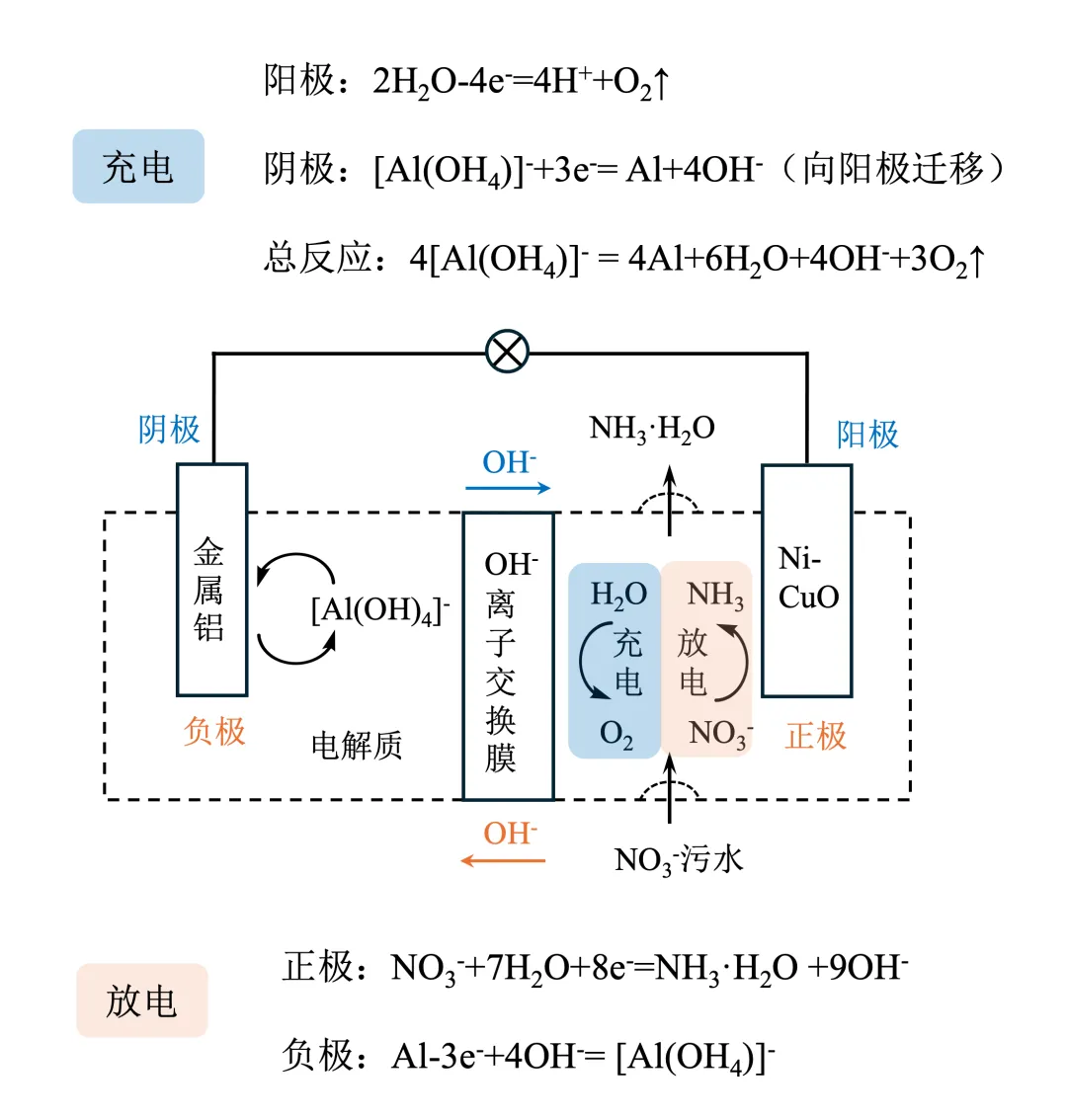
A选项:放电时,每转移24mol e-,负极需要32mol OH-,但正极只迁移过来27mol OH-,负极区还需自行准备OH-,即OH-的数目降低,A错误,这种考法与全国卷一致。
B选项:放电时,水中的氢离子得电子变成氢原子,氢原子将NO3-逐步还原为NH3。从NO3-到NH3,N从+5价降低到-3价,H从0价升高到+1价,因此,还原1mol NO3-为NH3,理论上需要8mol 氢原子。
注:关于放电时的正极反应,我看到有只写水解离的:8H2O+8e-= 8H+8OH-,这只是其中一个环节,NO3-还原为NH3的整个过程是文献中这样。

另附,真实的电化学装置长右图这样:
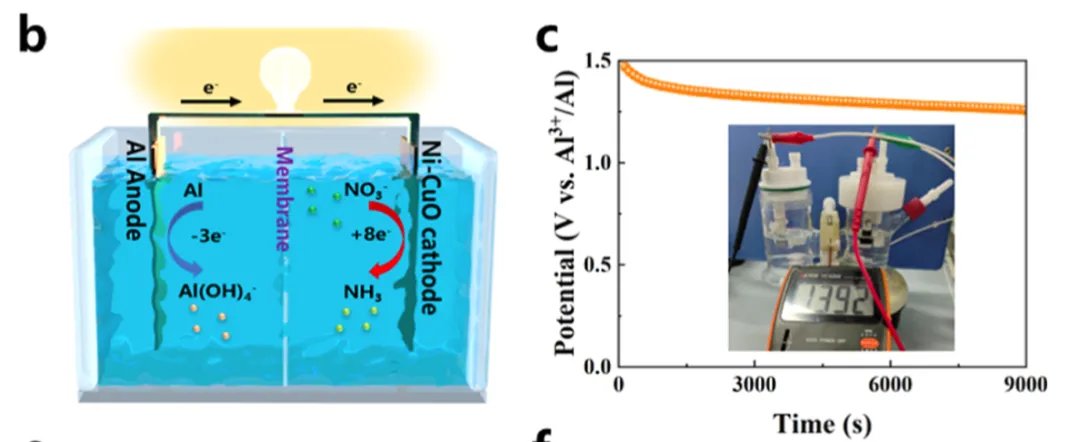
NO3-→NH3的反应历程
题目中之所以特意提到H原子,我猜……大概是想给我们透露一点反应机理,但又不能说得太彻底,主打一个类似启蒙的作用~~~
我看了文献原文之后,发现*H确实一个很好的切入点,这篇论文的亮点之一是hollow square的Ni-CuO催化剂,它可以提供双金属催化活性位点,尤其是Ni的加入。
研究发现,Ni既能加快水的解离,产生更多的活性*H,又能促进后续中间体*NOx的氢化,从而推动NO3-还原为NH3。
Ni加速水的解离
如下图,对比*H2O→*H+*OH这一步,以CuO作催化剂时需要吸热跨越能垒,以Ni-CuO为催化剂时则是放热,这在热力学上有利的,即Ni能促进水的电解。
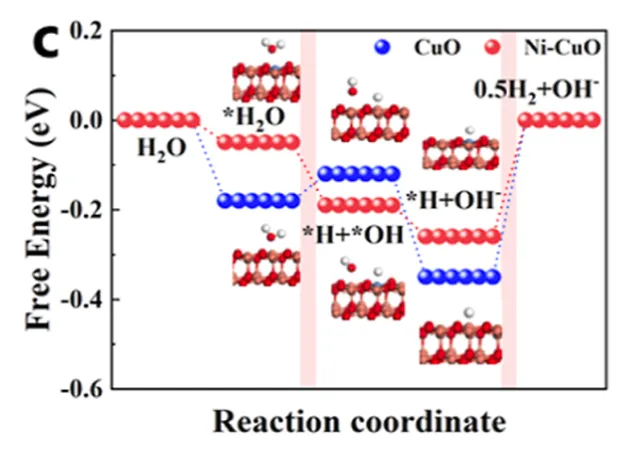
Ni加速中间体的氢化
如下图,从*NO3-到*NH3是一个复杂的过程,中间要经历很多个中间体。以CuO作催化剂时,可以看出*NO→*NOH、*NOH→*NHOH是非常关键的两步,能垒分别为0.05eV、0.12eV。
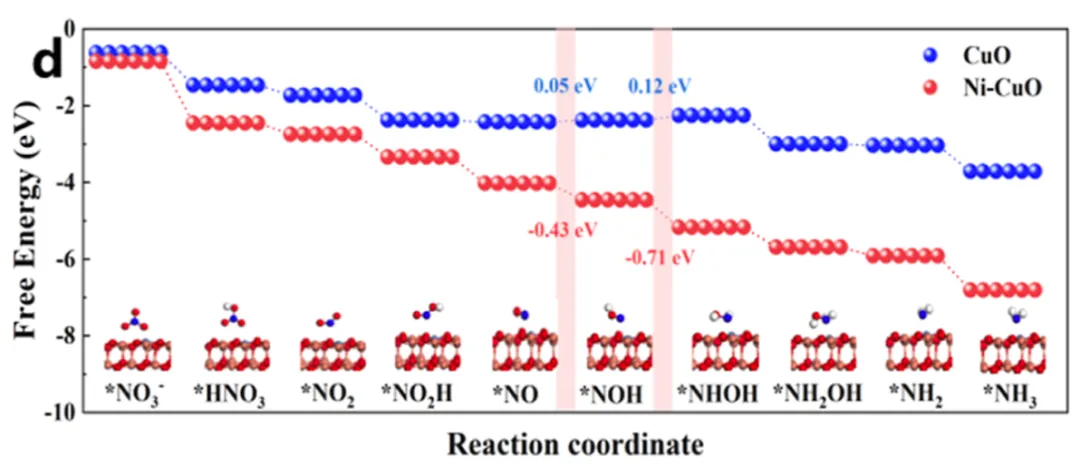
而以Ni-CuO为催化剂时,这两步的能垒则分别降为-0.43eV和-0.71eV,说明Ni的加入还可以促进中间体的氢化。
除此之外,Ni的加入可以增强催化剂表面的质子亲和力(proton affinity),为中间体提供更多的*H促进后续的氢化步骤,从而降低反应能垒、增强催化活性。
综上,Ni−CuO催化NO3-还原为NH3的反应机理如下,如果想了解更多,请参考原文献。
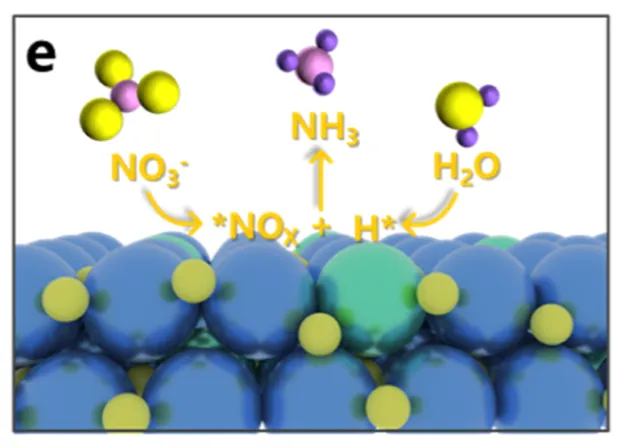
至此,电化学专题中NO3-的8电子还原过程完结,坐等它在2026年的新花样儿(大概率有的吧~hhh)。
🐳敬上~~~
特别备注:文中截图全部来自以上文献。






