苏北高三化学模考深度解析!考点全覆盖+重难点梳理,南京高三生直接抄作业
各位南京高三的同学、家长们好,我是南京化学邵老师~







近期苏北多地高三化学模拟联考正式结束,作为高三复习关键节点的大型联考,这套试卷命题质量极高,精准贴合新高考江苏卷命题趋势,既是检验复习成果的“试金石”,也是南京高三生查漏补缺、把握备考方向的优质参考资料。
今天邵老师就给大家带来这套苏北高三化学模考卷全方位深度解析,难题逐题拆解、好题精准赏析、核心考点全覆盖,还附上专属备考建议,干货拉满,同学们直接收藏学习!
一、试卷整体难度与命题特点
本次苏北高三化学模拟卷整体难度适中偏难,完全对标新高考江苏卷命题风格,注重基础知识落地、能力综合运用、化学核心素养考查,无偏题怪题,却在细节处设置考点,区分度极强,完美适配高三复习阶段性检测需求。
试卷整体呈现三大特点:
1. 基础题占比稳定:选择题前8题、非选择题基础设问,聚焦教材核心知识,考查化学基本概念、物质性质、基础实验操作,意在夯实学生知识底盘,杜绝基础失分;
2. 中档题侧重综合:中间梯度题目将多模块知识点融合考查,如物质结构+元素周期律、化学反应原理+化工流程、有机基础+实验操作,考验知识迁移与融会贯通能力;
3. 难题突出素养:压轴选择、化工流程、实验探究、原理综合题,侧重陌生情境分析、数据处理、逻辑推理、规范表述,是高考拉开分数差距的核心题型。
二、试卷难题逐题深度拆解+详细解题步骤
(一)选择题压轴难题
1. 新型钒电池电化学综合题
题目核心:以钒系新型充电电池为载体,考查充放电原理、电极判断、离子移动、电极反应、定量计算
解题步骤:
① 判断电极:放电时左槽溶液变蓝,VO₂⁺→VO²⁺(V元素化合价降低,发生还原反应),确定左槽为正极,右槽为负极;充电时电极反转,左槽为阳极,右槽为阴极。
② 充电连接:充电时阴极(原电池负极)接电源负极,阳极(原电池正极)接电源正极,即b电极接电源负极。
③ 电极反应:放电正极(a极):VO₂⁺ + 2H⁺ + e⁻ = VO²⁺ + H₂O(还原反应);充电阳极:VO²⁺ + H₂O - e⁻ = VO₂⁺ + 2H⁺。
④ 定量计算:充电时每转移1mol电子,左槽生成2mol H⁺,同时H⁺通过交换膜移向右槽,转移0.5mol电子时,左槽H⁺物质的量变化量为-1mol。
易错点:混淆充放电电极对应关系、忽略离子移动对微粒浓度的影响、化合价计算错误。
2. 草酸钙沉淀溶解平衡综合题
题目核心:结合CaCl₂与Na₂C₂O₄滴定图像,考查离子浓度比较、Ksp计算、平衡常数换算、守恒关系
解题步骤:
① 离子浓度比较:Na₂C₂O₄溶液中C₂O₄²⁻分步水解,第一步水解为主,离子浓度:c(Na⁺)>c(C₂O₄²⁻)>c(OH⁻)>c(HC₂O₄⁻)>c(H⁺)。
② 等量点分析:加入10mL Na₂C₂O₄时,溶质为NaCl和CaC₂O₄沉淀,电荷守恒:c(Na⁺)+c(H⁺)+2c(Ca²⁺)=c(Cl⁻)+c(HC₂O₄⁻)+2c(C₂O₄²⁻)+c(OH⁻),结合物料守恒推导微粒关系。
③ Ksp计算:加入15mL Na₂C₂O₄时,C₂O₄²⁻过量,先计算过量C₂O₄²⁻浓度,再通过c(Ca²⁺)=Ksp(CaC₂O₄)/c(C₂O₄²⁻) 计算钙离子浓度。
④ 平衡常数换算:反应CaC₂O₄+2H⁺⇌Ca²⁺+H₂C₂O₄的K=Ksp(CaC₂O₄)÷[Ka₁(H₂C₂O₄)×Ka₂(H₂C₂O₄)],代入数值计算即可。
易错点:图像坐标点理解错误、平衡常数公式记错、忽略沉淀对溶液微粒浓度的影响。
3. CO/CO₂加氢合成甲烷平衡综合题
题目核心:结合多反应竞争、转化率-温度图像,考查盖斯定律、平衡移动、定量收率计算
解题步骤:
① 盖斯定律:根据已知热化学方程式,通过加减运算推导目标反应焓变,注意焓变符号与系数匹配。
② 图像分析:温度升高,CO₂转化率降低,说明反应为放热反应;压强增大,反应i、ii均正向移动,CO₂转化率曲线向上平移。
③ 定量计算:设定初始投料量,根据CO转化率计算反应量,再结合平衡收率公式,判断各物质平衡物质的量,核心是理清多反应之间的物质转化关系。
易错点:多反应平衡叠加分析混乱、收率计算公式理解错误、温度/压强对平衡影响判断失误。
(二)非选择题压轴难题
1. 钴酸锂正极材料回收化工流程题
题目核心:废旧LiCoO₂回收工艺,考查氧化还原反应、配位平衡、晶胞计算、煅烧反应
详细解题步骤:
① 浸出阶段:草酸还原LiCoO₂,Co元素从+3价降至+2价,草酸被氧化为CO₂,液固比过大时,过量草酸与Co²⁺形成可溶性配合物,导致沉淀率下降。
② 离子方程式书写:[CoCl₄]²⁻与水反应生成[Co(H₂O)₆]²⁺,属于配位平衡转化,直接配平即可:[CoCl₄]²⁻ + 6H₂O = [Co(H₂O)₆]²⁺ + 4Cl⁻。
③ 煅烧反应:Li₂CO₃、CoCO₃与O₂在700-900℃下反应生成LiCoO₂,根据化合价升降配平:2Li₂CO₃ + 4CoCO₃ + O₂ = 4LiCoO₂ + 6CO₂。
④ 晶胞计算:确定晶胞中Co²⁺、Mg²⁺、O²⁻的数目,Mg²⁺替代部分Co²⁺,根据替代比例计算微粒个数比,先算总微粒数,再算各离子数量。
易错点:陌生氧化还原反应配平、配位化合物影响分析、晶胞微粒计数错误。
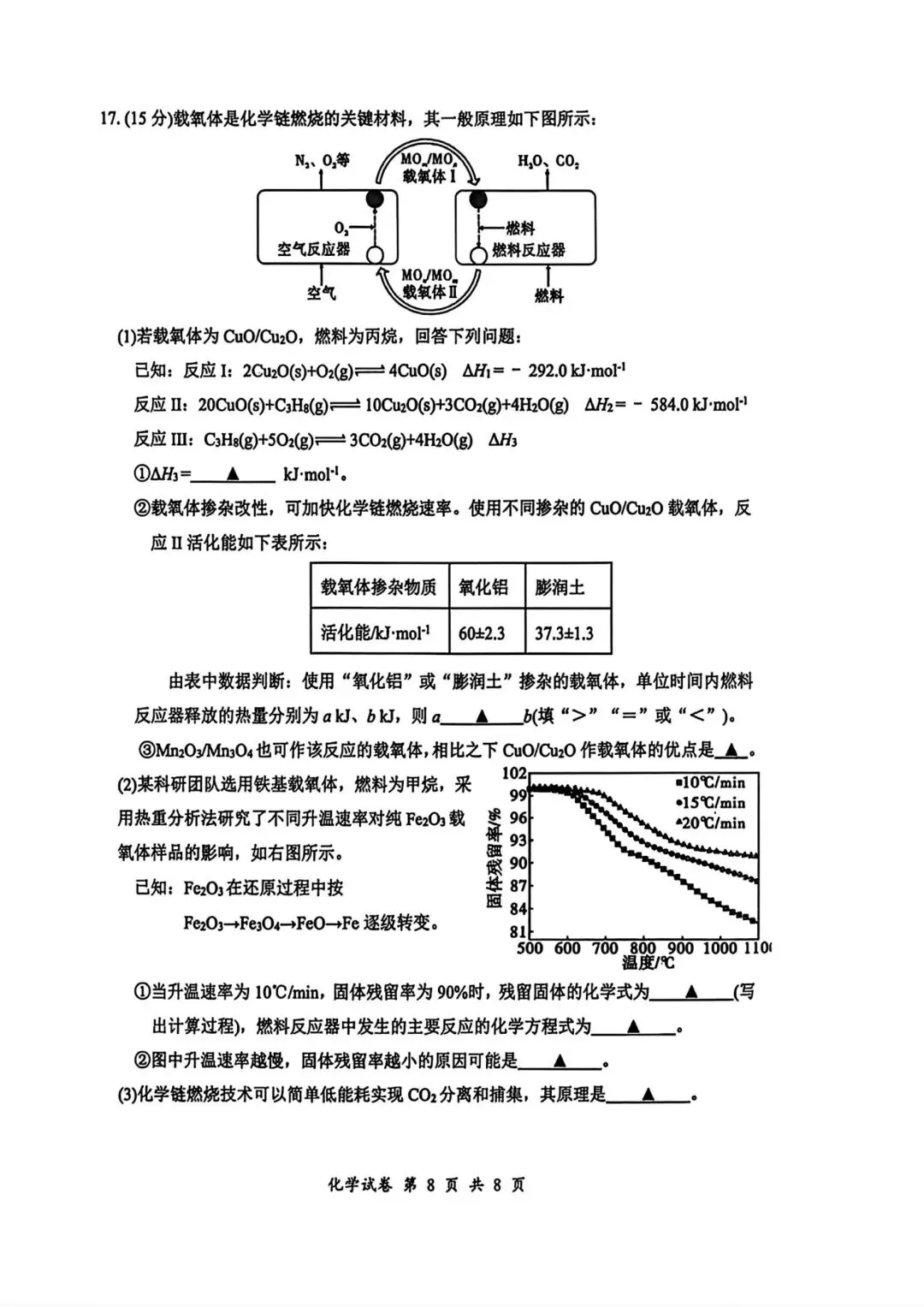
2. 载氧体化学链燃烧原理综合题
题目核心:工业化学链燃烧工艺,考查盖斯定律、活化能、反应历程、工艺评价
详细解题步骤:
① 焓变计算:根据目标反应,整合已知反应,消去中间产物,计算ΔH,注意反应方向与系数。
② 活化能分析:膨润土掺杂后,反应活化能降低,反应速率加快,活化能数值a<b。
③ 固体还原反应:根据固体残留率,判断850℃下Fe₃O₄被CH₄还原为FeO,配平反应方程式:4Fe₃O₄ + CH₄ = 12FeO + CO₂ + 2H₂O。
④ 工艺评价:从能耗、CO₂捕集、环保、反应效率角度作答,规范文字表述,避免口语化。
易错点:反应历程梳理不清、活化能与反应速率关系混淆、工艺评价答题不规范。
三、试卷优质好题赏析(备考必刷)
这套试卷命题经典,紧扣高考高频考点,多道题目堪称“高考母题”,南京高三生一定要反复研究:
1. 化学用语基础题:覆盖电子云轮廓图、电子式、电子排布式、空间填充模型,直击教材基础易错点,帮同学们规范化学用语表述;
2. 实验装置判断题:涵盖气体体积测量、反应速率测定、酸碱滴定、金属腐蚀探究,全面考查实验装置合理性,贴合高考实验选择题命题思路;
3. 物质结构综合题:杂化轨道判断、空间构型、配位键、第一电离能、晶格能,考点全面,精准对接高考物质结构核心考法;
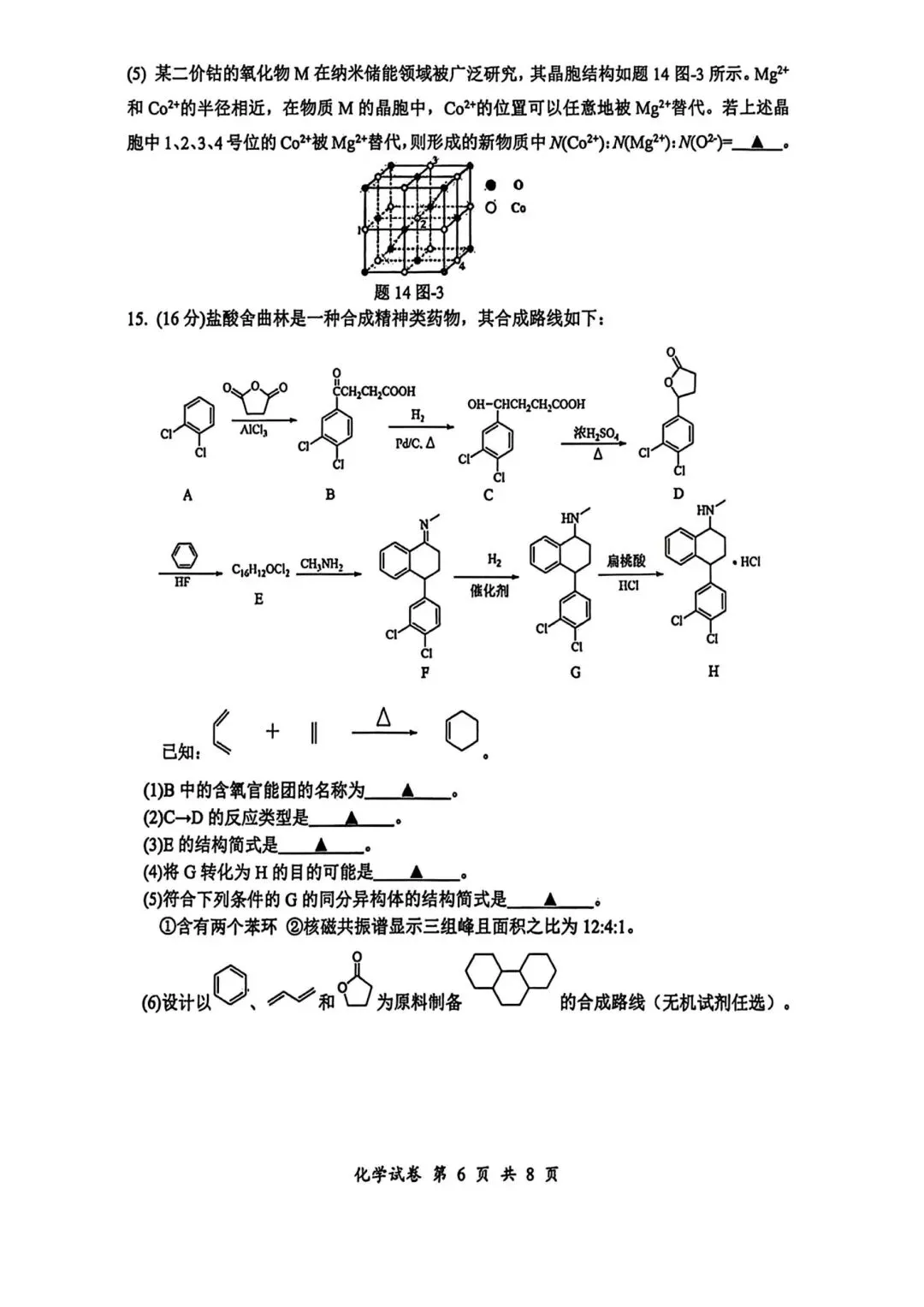
4. 有机合成推断题:官能团识别、反应类型判断、同分异构体书写、合成路线设计,梯度合理,锻炼有机化学逻辑推理能力;
5. Fe₃O₄纳米材料实验题:融合溶液配制、离子方程式书写、分离提纯、性质探究,实验与原理深度结合,适配高考实验综合题命题逻辑。
四、试卷核心考点/知识点全覆盖梳理
(一)选择题核心考点
1. 化学与STSE、物质分类、化学发展史
2. 化学用语规范(电子式、电子排布式、电子云、空间模型)
3. 化学实验基础操作、装置评价、误差分析
4. 元素周期律、电离能、晶格能、非金属性比较
5. 物质结构:杂化类型、配位键、晶体类型、化学键类型
6. 离子方程式、热化学方程式正误判断
7. 新型原电池、电解池综合原理
8. 沉淀溶解平衡、弱电解质电离、离子浓度图像分析
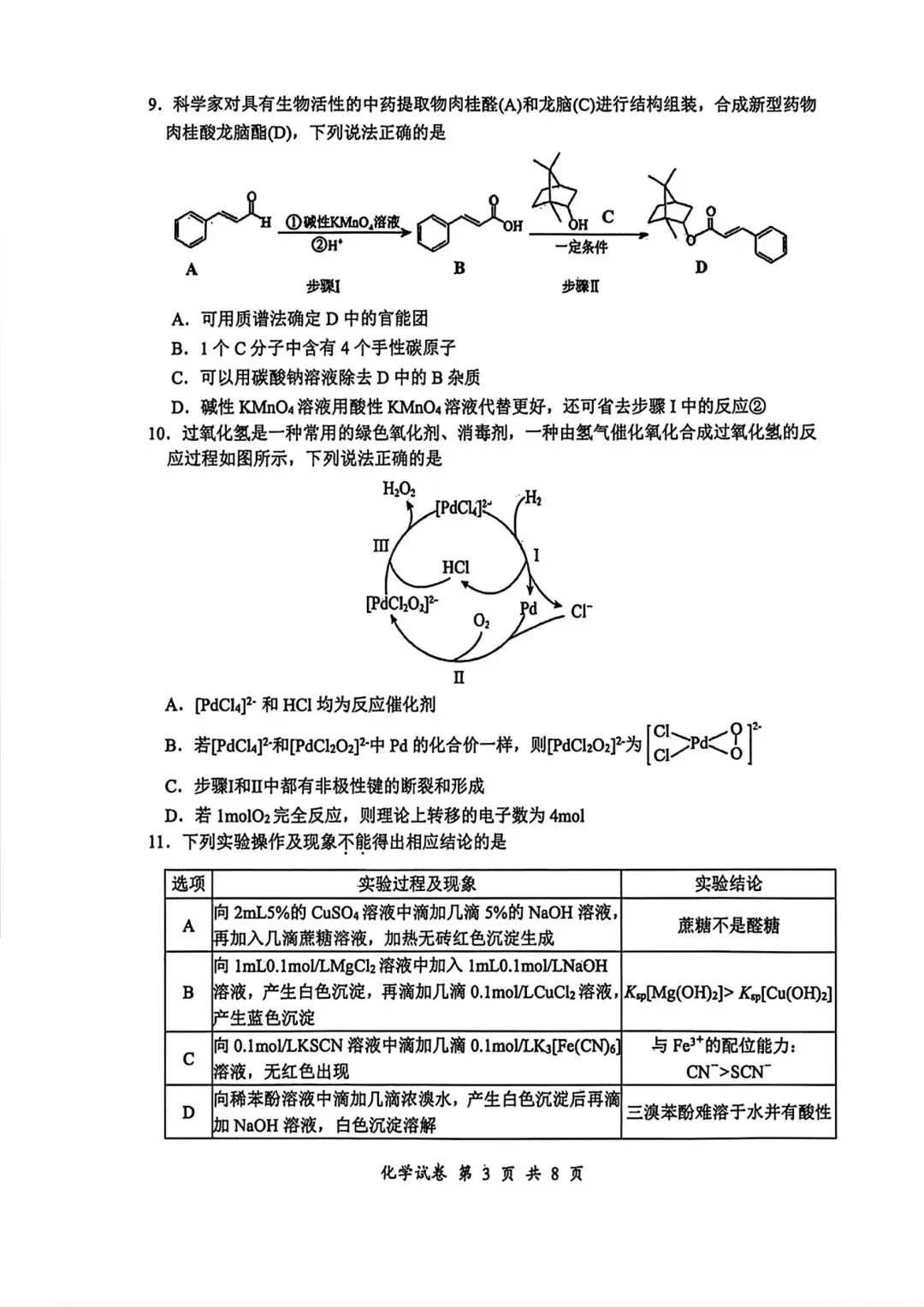
9. 有机化学基础:官能团、反应类型、同分异构
10. 化学反应机理、催化剂作用、电子转移计算
(二)非选择题核心考点
1. 化工流程:氧化还原反应、分离提纯、工艺条件分析、晶胞计算
2. 有机合成:结构简式推导、反应类型、同分异构体、逆合成路线
3. 综合实验:离子方程式、溶液配制、纳米材料制备、性质探究
4. 化学反应原理:盖斯定律、化学平衡、活化能、工业工艺评价
5. 电解质溶液:平衡常数、离子守恒、定量计算
五、针对南京高三生的备考建议
结合本次苏北模考命题趋势,邵老师给南京高三同学整理了超实用的化学备考攻略,照着做稳步提分:
1. 回归教材,筑牢基础:高考化学70%为基础题,务必吃透教材概念、方程式、实验步骤、物质性质,整理基础易错点,杜绝低级失分;
2. 专项突破,攻克压轴:重点攻克电化学、水溶液平衡、化工流程、原理综合四大难点,整理同类题型解题模板,总结解题思路;
3. 强化计算,规范答题:模考中平衡常数、晶胞、电子转移计算失分率极高,平时加强计算练习,答题步骤完整、文字表述精准,按点得分;
4. 精刷真题,贴合考情:优先刷江苏新高考真题、苏北/南京等地模考题,熟悉本地命题风格,针对性训练陌生情境解题能力;
5. 错题复盘,查漏补缺:建立错题本,标注错题考点、错误原因、解题方法,定期复盘,避免同类题目重复出错。
六、写在最后
苏北高三化学模考是高三复习的重要参考,分数只是暂时的,通过试卷找到知识漏洞、调整复习节奏才是核心目的。同学们不用因难题失分焦虑,针对性补齐短板,稳步推进复习即可。
后续邵老师会持续更新江苏各地高三模考化学深度解析、高考化学解题技巧、高频考点总结、错题专项训练,助力南京高三生攻克化学难关,冲刺高考高分!
需要这份试卷完整答案+高清原题+详细解题步骤文档的同学,直接后台留言【苏北模考】,即可免费获取,方便打印复习!





