中考临近,将陆续为各位同学整理各科必考知识点。
本期内容为:化学第三期:二氧化碳的必考知识点
知识点1 溶液的形成
1.溶液
(1)概念:一种或几种物质分散到另一种物质里,形成均一的、稳定的混合物。
(2)特征:均一性、稳定性
(3)组成:
①溶质:被溶解的物质,可以是固体、溶液、气体
②溶剂:能溶解其他物质的物质。水是最常用的溶剂,汽油、酒精等也可以作溶剂
(4)应用:
①动植物的生理活动:人的各种体液都是含有多种溶质的溶液
②工农业生产:无土栽培的蔬菜营养液等
③科学研究:化学实验室中使用的溶液等
④医疗:常用的葡萄糖溶液、生理盐水和各种眼药水等
2.溶解
(1)吸热:一些物质溶于水后,整个过程中溶液温度降低,如NH4NO3(或硝酸铵)固体。
(2)放热:一些物质溶于水后,整个过程中溶液温度升高,如NaOH固体、浓H2SO4。
(3)吸放热不明显:多数物质溶于水后,整个过程中溶液温度变化不明显,如NaCl固体。
知识点2 饱和溶液与不饱和溶液
1.概念
(1)不饱和溶液:在一定温度下,一定量溶剂里,还能继续溶解这种溶质的溶液
(2)饱和溶液:在一定温度下,一定量溶剂里,不能继续溶解这种溶质的溶液
2.判断依据

3.转化
(1)对于溶解度随温度升高而增大的物质(如KNO3等):

(2)对于溶解度随温度升高而减小的物质[如Ca(OH)2等]:
改变温度的方式与①相反。
知识点3 结晶
1.概念:溶质从溶液中以晶体的形式析出的过程
2.方法:
(1)蒸发结晶:通过蒸发溶剂的方法使溶质析出,适用于溶解度受温度影响较小的物质,如氯化钠
(2)降温结晶(冷却热饱和溶液):通过降温的方法使溶质析出,适用于溶解度随温度升高而明显增大的物质,如硝酸钾
知识点4 溶解度
1.定义:在一定温度下,某物质在100g溶剂(通常为水)中达到饱和状态时所溶解的最大质量为该物质在这种溶剂里的溶解度
2.四要素:条件:一定温度、标准:100g溶剂、状态:达到饱和、单位:g(或克)
3.影响因素:
(1)内因:溶质和溶剂的性质
(2)外因
①温度:固体物质:a.大多数固体物质溶解度随温度升高而增大,如KNO3等;b.少数固体物质溶解度受温度变化影响不大,如NaCl等;c.极少数固体物质溶解度随温度升高而降低,如Ca(OH)2等。气体物质:压强一定时,溶解度随温度的升高而减小
②压强:温度一定时,气体的溶解度随压强的增大而减小
4.溶解度的相对大小:
一般称为 | 难溶 | 微溶 | 可溶 | 易溶 |
溶解度/g | <0.01 | 0.01~1 | 1~10 | >10 |
知识点5 溶解度曲线(针对固体溶质)
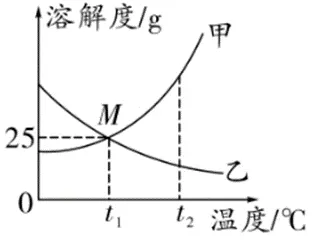
(1)概念:溶解度随温度变化的曲线。纵坐标表示溶解度,横坐标表示温度
(2)意义:
①点
曲线上的点:表示物质在对应温度下的溶解度
两曲线的交点:表示两物质在某温度下溶解度相等
②线
曲线的走向表示物质的溶解度随温度改变而变化的趋势
曲线的陡缓表示物质溶解度受温度影响的变化大小
知识点6 溶液的定量组成(浓度)
1.溶质质量分数的计算
(1)所有溶液:

(2)饱和溶液:
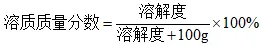
2.溶质质量分数的换算
(1)溶液质量(m)=溶质质量+溶剂质量=溶液体积(V)×溶液密度(ρ)
(2)
3.溶液的稀释
(1)依据:稀释前后,溶液中溶质的质量不变
(2)计算公式:m浓·w浓=m稀·w稀(w表示溶质质量分数)
【为及时收到每期更新内容,请添加 关注、收藏+分享  】
】





