2026年04月18日
上海初中化学中考趋势 | 2026年04月18日
今日主题
城市垃圾焚烧发电厂尾气脱酸工艺的物质转化与定量计算 · 现代城市干垃圾常送至焚烧发电厂处理。为防止二次污染,某环保企业采用'半干法脱酸'前沿技术,向高温烟气中雾化喷入溶质质量分数为20%的石灰浆,高效吸收HCl和SO₂等有害气体。若某监测时段内烟气中含73kg的HCl气体,需完全转化为CaCl₂和水。工程师需依据化学方程式精确计算所需石灰浆的最低质量,并控制喷入量以避免设备结垢,实现尾气达标排放。
核心知识点
• 碱的化学性质与酸性气体的吸收
• 质量守恒定律与化学方程式的定量计算
• 溶液溶质质量分数的综合计算
教育价值
通过垃圾焚烧尾气处理的真实工程情境,引导学生将抽象的酸碱中和原理与实际环保问题相结合,培养运用定量计算解决工程实际参数(如石灰浆用量)的能力,深刻理解'绿色化学'在社会可持续发展中的关键作用,提升科学探究与社会责任素养。
情景化题型精讲
【填空题】(中等程度,总分14分)
【情境背景】现代城市生活垃圾分类后,干垃圾常被送往焚烧发电厂进行资源化处理。垃圾焚烧过程中会产生含有氯化氢(HCl)和二氧化硫(SO₂)等酸性有害气体的尾气。为防止二次污染,实现尾气达标排放,某环保企业引入了前沿的'半干法脱酸'工艺(见图1)。该工艺的核心环节是将氢氧化钙质量分数为20%的石灰浆(石灰浆为氢氧化钙与水形成的悬浊液)通过旋转雾化器雾化成极细的液滴,喷入高温烟气反应塔中。氢氧化钙与酸性气体发生中和反应,生成氯化钙(CaCl₂)和水。由于水分在高温下迅速蒸发,最终反应产物以干燥的固体粉末形式排出,从而避免了设备内壁结垢和腐蚀问题。据系统监测数据显示,在某特定的运行工况时段内,进入脱酸塔的烟气中累计含有73kg的氯化氢气体。工程师需要依据化学方程式精确计算所需20%石灰浆的最低质量,以设定雾化喷嘴的喷射流量。同时,现场操作人员需要使用纯度为100%的熟石灰干粉和工业纯水,在搅拌罐中大批量配制这种20%的石灰浆备用。配制过程的规范与否直接影响脱酸效率,若浓度过低会导致脱酸不达标,浓度过高则容易堵塞雾化喷嘴。
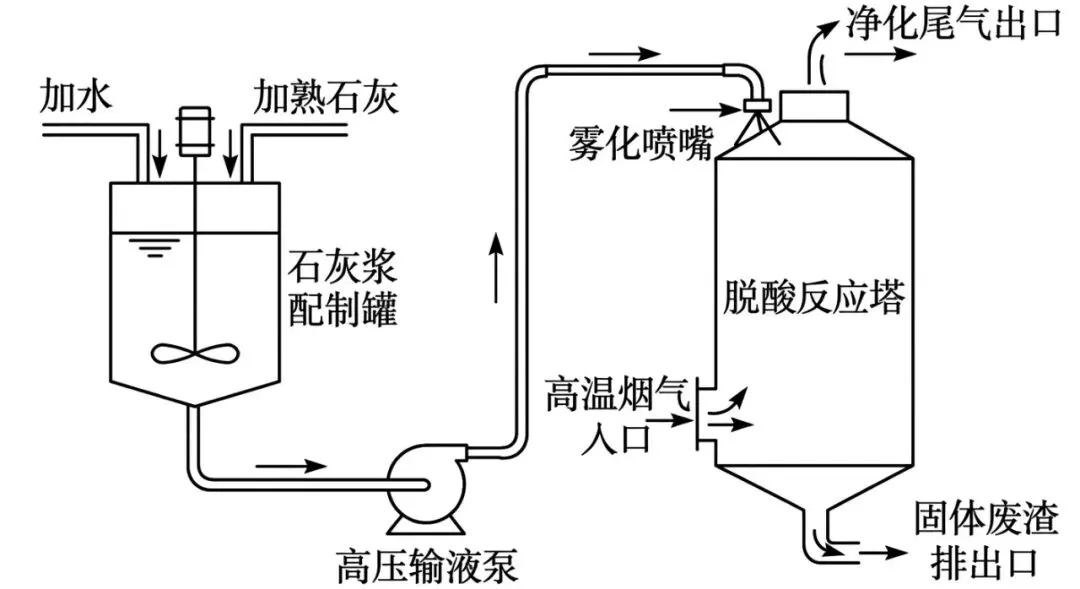
现代垃圾焚烧发电厂半干法脱酸工艺流程示意图。左侧为石灰浆配制罐,熟石灰粉末与纯水按比例在此混合搅拌均匀。配制好的石灰浆经高压泵输送至脱酸反应塔顶部的旋转雾化器,形成极细的雾滴。含有酸性气体的烟气从塔底进入,与下落的石灰浆雾滴逆流接触,发生中和反应,水分迅速蒸发,最终净化后的尾气从塔顶排出,干燥的固态反应产物从塔底收集。
(1)请根据化学方程式计算,为完全吸收该监测时段内的73kg氯化氢气体,理论上至少需要配制并喷入氢氧化钙质量分数为20%的石灰浆多少千克?(5分)
参考答案:
370kg
解析:
解析:设完全吸收73kg HCl需要纯氢氧化钙的质量为x。反应的化学方程式为:Ca(OH)₂ + 2HCl → CaCl₂ + 2H₂O。由相对分子质量可知,Ca(OH)₂与2HCl的质量比为74:73。列出比例式:(74)/(73) = (x)/(73 kg),解得x = 74 kg。根据质量分数公式,所需20%石灰浆的质量 = (74 kg)/(20%) = 370 kg。
(2)若现场操作人员要一次性配制上述计算所得质量的20%石灰浆,请简述其配制的主要操作步骤,并计算指出需要称量熟石灰干粉的质量和量取工业纯水的体积各是多少(水的密度按1.0kg/L计)?(4分)
参考答案:
需称量熟石灰干粉74kg,量取工业纯水296L。配制步骤依次为:计算、称量和量取、混合(搅拌成浆)。
解析:
解析:依据第(1)问结果,需配制370kg的20%石灰浆。所需熟石灰干粉质量为74kg;所需纯水的质量 = 石灰浆总质量 - 氢氧化钙质量 = 370 kg - 74 kg = 296 kg。由于水的密度按1.0 kg/L计,故需量取纯水的体积为296 L。工业配制步骤与实验室类似,第一步为'计算'所需物料;第二步为'称量和量取',使用大型电子磅秤称取74kg熟石灰干粉,并量取296L工业纯水;第三步为'混合',将熟石灰和纯水加入搅拌罐中,开启搅拌设备使其充分混合均匀。
(3)在实际工业配制过程中,请分析以下两种情况对所配制石灰浆中氢氧化钙质量分数的影响(填'偏大'、'偏小'或'无影响'),并简要说明理由。情况一:熟石灰干粉在露天堆放时间过长;情况二:向搅拌罐中加水时,实际加水量超过了计算值。结合情境,这两种情况分别会给'半干法脱酸'工艺带来什么隐患?(5分,答案不唯一,言之有理即可)
参考答案:
情况一:偏小;情况二:偏小。隐患分析需结合脱酸效率或设备运行状况作答(详见解析)。
解析:
解析:情况一:熟石灰干粉露天堆放易吸收空气中的二氧化碳变质生成碳酸钙(Ca(OH)₂ + CO₂ → CaCO₃↓ + H₂O),导致有效成分Ca(OH)₂质量减少,所配制石灰浆中氢氧化钙的质量分数偏小。带来的隐患:有效成分不足,无法完全吸收烟气中的酸性气体,导致尾气排放超标;同时不溶性杂质碳酸钙可能磨损或堵塞雾化喷嘴。情况二:加水量超标,水的质量增大,氢氧化钙质量不变,导致氢氧化钙的质量分数偏小。带来的隐患:喷入相同体积的石灰浆时,有效脱酸成分不足导致脱酸不达标;若为达到脱酸效果而强行增加喷浆量,会导致反应塔内水分过多无法迅速蒸发,可能引起设备内壁结垢或腐蚀,破坏'半干法'干燥出渣的优势。
知识点地图
化学方程式的定量计算 → 混合物中质量分数的综合计算 → 一定质量分数悬浊液的配制步骤 → 物质的变质(碱的化学性质) → 悬浊液配制的误差分析及工程评价
本题知识点之间的逻辑关联,帮助学生建立知识网络
思路拓展
1. 拓展问题1:如果尾气中不仅含有HCl,还含有同样质量的SO₂气体,若要完全吸收,所需的石灰浆质量会如何变化?请尝试写出相关的化学方程式并分析计算逻辑。
2. 拓展问题2:为了防止熟石灰干粉在储存过程中变质,环保企业应该采取哪些具体的储存措施?在配制前如何通过简单的化学实验检验熟石灰是否已经发生变质?
拓展问题不要求作答,目的是打开思路,培养发散思维
学习建议
1. 梳理'半干法脱酸'中的核心反应原理。请在纸上准确写出氢氧化钙与氯化氢、二氧化硫反应的化学方程式:Ca(OH)₂ + 2HCl = CaCl₂ + 2H₂O,Ca(OH)₂ + SO₂ = CaSO₃↓ + H₂O。建议采用'反应物-生成物-配平'三步法进行书写练习,特别注意非金属氧化物与碱反应时元素的化合价不变,以此夯实酸碱盐反应的物质转化基础。
2. 建立规范的化学方程式计算模板。针对情景中73kg的HCl气体,严格按照'设、方、关、比、算、答'六步格式进行训练。先写出反应方程式,在化学式下方准确标出Ca(OH)₂与2HCl的相对分子质量(分别为74和73)及已知量m(HCl)=73kg,列出比例式求出纯Ca(OH)₂的质量,养成严谨的解题习惯,避免因步骤跳跃或相对分子质量计算错误导致失分。
3. 攻克纯净物与混合物质量转换的计算难点。在求出纯Ca(OH)₂的质量后,务必结合公式'溶液质量 = 溶质质量 ÷ 溶质质量分数'进行二次计算。针对本题,需将计算得出的m(Ca(OH)₂)除以20%,才能得到所需石灰浆的最低质量。建议在平时练习中多画'质量关系转化图',理清化学方程式中纯净物质量与实际生产中溶液质量的包含关系。
4. 培养工程思维与实际应用能力。不要仅仅停留在算出正确答案,还要结合题干思考'控制喷入量以避免设备结垢'的工程意义。建议查阅资料或与同学讨论:若石灰浆喷入过量,水分蒸发后未反应的Ca(OH)₂结晶,或其吸收烟气中的CO₂生成CaCO₃沉淀(Ca(OH)₂ + CO₂ = CaCO₃↓ + H₂O),会导致设备发生怎样的故障?通过这种探究,深刻理解化学定量计算在环保工程中实现'精准投料、达标排放'的实际价值。
中考趋势分析
近期上海初中化学中考呈现以下趋势:
• 题目形式的变化:近年来上海中考化学在定量计算板块,逐渐从单纯的最后一道大计算题,向综合填空题或工艺流程题渗透。涉及'垃圾焚烧厂尾气脱酸'这类真实工业场景的计算,往往与物质转化流程图结合考查,选择题中也可能出现定性与半定量结合的判断题,纯计算题的比例相对下降,综合应用题比例上升。
• 知识考查的深度和广度:考查广度上,不再局限于单一的酸碱中和,而是拓展到混合气体的吸收(如同时处理HCl和SO₂),涉及Ca(OH)₂ + 2HCl = CaCl₂ + 2H₂O以及Ca(OH)₂ + SO₂ = CaSO₃↓ + H₂O等多重反应。深度上,将溶质质量分数(20%的石灰浆)与化学方程式的综合计算紧密结合,要求学生不仅能算出纯物质的质量,还要换算成实际工业溶液的质量。
• 情景化、应用性题目的特点:情景创设紧贴上海市'干垃圾处理'与'环保减排'热点,具有极强的真实性和时代感。题目常包含'半干法脱酸'、'雾化喷入'、'设备结垢'等工程术语,特点是'起点高、落点低',即利用前沿环保科技包装,实质依然考查初中核心的物质转化规律与质量守恒定律。
• 对学生能力要求的变化:对信息提取与建模能力的要求显著提升。学生需要从冗长的工业背景中剔除干扰信息,精准提取出'73kg的HCl'、'20%的石灰浆'等关键数据,并将其转化为数学计算模型。同时,要求学生具备一定的工程思维,例如理解控制喷入量以'避免设备结垢'背后的试剂过量问题,实现了从'解题'向'解决实际问题'的能力跨越。
• 备考建议和重点:备考时应重点强化酸碱盐的核心化学性质及方程式书写,熟练掌握Ca(OH)₂与非金属氧化物、酸反应的化学方程式。在定量计算训练中,要规范解题步骤,特别是m(HCl)与m(Ca(OH)₂)的比例关系换算。建议多做带有工业流程背景的综合题,提升将实际问题转化为化学方程式(如Ca(OH)₂ + 2HCl = CaCl₂ + 2H₂O)并结合质量分数进行综合计算的能力。
实际应用
垃圾焚烧发电厂的尾气净化系统、化工厂酸性废气的无害化处理、燃煤电厂的脱硫脱硝工程。
每日一题,助力中考
科学备考,稳步提升
更新时间: 2026-04-18 08:50:58
内容说明: 本栏目专注上海初中化学中考趋势分析,每日精选情景化题型,帮助学生掌握核心知识点和解题方法。



![备课资料:[2026]广西柳州市中考一模语文试卷 备课资料:[2026]广西柳州市中考一模语文试卷](https://sjds.net/zb_users/cache/thumbs/06f3dacb1a1576134fee805107ca979e-320-200-1.gif)



![[JLPT日语真题-N2]202107语言_问题6(地道用法)_1/5 [JLPT日语真题-N2]202107语言_问题6(地道用法)_1/5](https://sjds.net/zb_users/cache/thumbs/91120967c667b15f8559ede619f034b2-320-200-1.gif)