Electrode potential
化学万事屋live
在2025年所有的电化学真题中,与北京卷距离最近的,我认为是东北卷(主观观点)。从这两道题中,你能感觉到“电极电势”与“氧化(还原)性”联手的意图。
02 东北卷 | 储氯电池
题目如下,从素材上来看,这里的NaTi2(PO4)3 | Na3Ti2(PO4)3电极在2022年的辽宁卷就出现过,那是一个液流电池,感兴趣的读者可以自己去网上搜搜看。
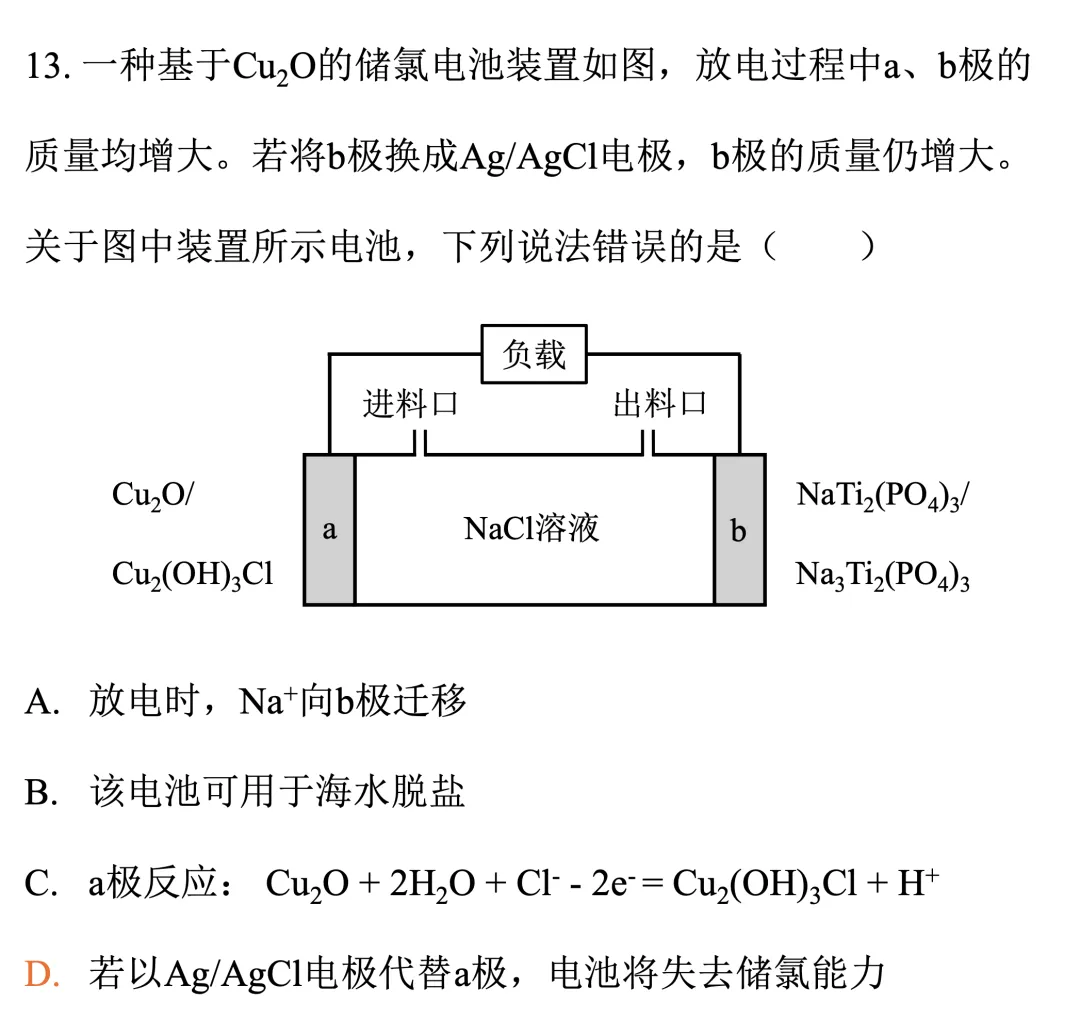
这道题选出答案不难,大致的思路如下:a、b极的质量增大→物质的转化方向→Cu和Ti的化合价变化→电源的正负极→离子迁移方向。根据电极反应,负极消耗Cl-,正极消耗Na+,由此实现海水脱盐,答案为D。
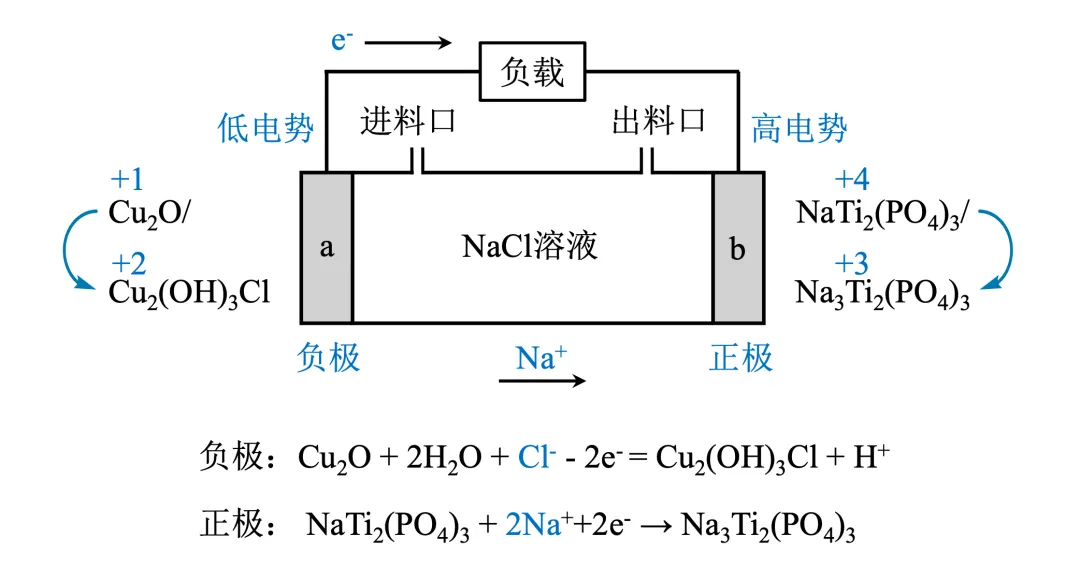
D选项的解释有两种角度:①氧化(还原)性,②电极电势。
① 氧化(还原)性
Cu系和Na系搭配时,NaTi2(PO4)3作氧化剂,Cu2(OH)3Cl为氧化产物,氧化性:NaTi2(PO4)3>Cu2(OH)3Cl。
Cu系和Ag系搭配时,Ag→AgCl(负极),质量增大。Cu2(OH)3Cl作氧化剂,AgCl为氧化产物,氧化性:Cu2(OH)3Cl>AgCl。
根据氧化性的排序:NaTi2(PO4)3>Cu2(OH)3Cl>AgCl,Na系和Ag系搭配时,NaTi2(PO4)3作氧化剂,Ag作还原剂,从Ag→AgCl,电池依旧具备储氯能力。
② 电极电势
Cu系和Na系搭配时,Cu系电极作负极。在原电池的外电路中,电子由低电势(负极)流向高电势(正极),因此有电极电势:ENa系>ECu系。
Cu系和Ag系搭配时,Ag→AgCl(负极),电极电势:ECu系>EAg系。
根据电极电势的排序:ENa系>ECu系>EAg系,Na系电极和Ag系电极搭配时,前者为电源正极,后者为电源负极,Ag失电子后转化为AgCl,电池依旧具备储氯能力。
小结:基于以上两种角度,可以构建起:“氧化性高→电源正极→电极电势高”的关系,相对应的,还有“还原性高→电源负极→电极电势低”的关系,即可用电极电势的数值来衡量氧化(还原)性的高低。
正如吸热反应对应△H>0,人们习惯将“得到……”规定为正值,因此,得电子能力越强→氧化性高→电极电势越大。
以上~~~







