
第四部分物质构成的奥秘核心知识清单
一、中考备考指南
1.中考考情分析
(1)核心题型:以选择题为主,高频出现在填空与简答题、微观示意图分析题中,是化学方程式书写、化学式计算、物质推断题的核心基础,贯穿中考全卷。
(2)分值占比:全国中考普遍为4~8分,是一轮复习的核心基础专题,属于“基础不牢,全卷不稳”的核心考点,无高难度计算,但概念辨析与规范表述要求极高。
(3)命题趋势:摒弃纯概念死记硬背,核心围绕4个方向命题:
①结合生活场景考查分子的基本性质;
②结合原子结构示意图、元素周期表单元格考查原子结构与元素规律;
③结合微观反应示意图综合考查物质构成、反应本质与化学式书写;
④结合化学式考查化合价计算与宏观微观表述辨析。
2.中考复习要求
(1)能准确掌握分子、原子、离子的定义、区别与联系,能用微观粒子的观点解释常见的生活现象与化学变化的本质;
(2)能清晰描述原子的构成,掌握原子结构示意图的书写与判断,明确质子数、中子数、电子数、核电荷数的数量关系;
(3)能精准区分元素与原子的概念,掌握元素符号的书写与意义,熟记元素周期表的基本规律与单元格信息提取;
(4)能熟练运用化合价规则,根据化学式计算元素化合价,或根据化合价书写规范化学式;
(5)能准确区分宏观与微观的规范表述,掌握化学式的宏观、微观、量的三层意义,能完成相对原子质量、相对分子质量的基础计算。
3.变式出题方向
(1)情境变式:结合端午粽香、气球压缩、品红扩散等生活场景,考查分子的基本性质;结合航天新材料、新发现元素,考查原子结构与元素周期表;
(2)易错变式:针对宏观微观表述混淆、元素与原子概念辨析、原子与离子结构差异、化合价与离子符号书写混淆等高频易错点设置辨析题;
(3)综合变式:通过微观反应示意图,综合考查物质构成、反应本质、化学式书写、化合价变化、反应类型判断全考点;
(4)反向变式:通过元素周期表规律反推未知元素的性质,通过化学式反推元素化合价,通过粒子结构示意图反推粒子种类与元素种类。
二、核心知识点梳理
1、分子
定义:由分子构成的物质,分子是保持其化学性质的最小粒子
基本性质:质量体积小、不断运动、有间隔、同种分子化学性质相同
构成:由原子构成
常见实例:水、氧气、二氧化碳、氨气
2、原子
定义:化学变化中的最小粒子
基本性质:同分子性质相同、质量体积小、不断运动、有间隔
构成:原子核(质子+中子)、核外电子
常见实例:金属、稀有气体、金刚石、硅
3、离子
定义:带电的原子或原子团
分类:阳离子(带正电)、阴离子(带负电)
形成:原子得失电子形成
常见实例:氯化钠、硫酸铜、氢氧化钠等离子化合物
核心区别:化学变化中,分子可分,原子不可分
4、原子的结构
原子结构:原子核(带正电,集中原子几乎全部质量)
质子:带1个单位正电荷,质子数=核电荷数=原子序数
中子:不带电,普通氢原子无中子
核外电子:带1个单位负电荷,质量极小,分层排布
5、原子结构示意图
圆圈:代表原子核,圈内数字为质子数
弧线:代表电子层,弧线上数字为该层电子数
最外层电子数:决定元素的化学性质
原子与离子的转化
失电子→阳离子(质子数>核外电子数)
得电子→阴离子(质子数<核外电子数)
元素与元素周期表
6、元素
定义:质子数(即核电荷数)相同的一类原子的总称
分类:金属元素、非金属元素、稀有气体元素
元素符号意义:
宏观表示一种元素,微观表示一个原子;
金属、稀有气体、固态非金属符号还可表示物质
地壳含量前四位:氧、硅、铝、铁
7、元素周期表
发明者:门捷列夫
结构:7个周期(横行)、16个族(纵行)
周期规律:同一周期电子层数相同,最外层电子数从左到右依次递增
族规律:同一主族最外层电子数相同,化学性质相似,电子层数从上到下依次递增
单元格信息:原子序数、元素符号、元素名称、相对原子质量
8、化学式
定义:用元素符号和数字的组合表示物质组成的式子
意义:宏观表示物质及元素组成,微观表示分子及分子构成,量的意义表示相对分子质量、元素质量比
9、化合价
规则:化合物中,各元素正负化合价的代数和为0;单质中元素化合价为0
表示方法:标在元素符号正上方,正负号在前,数字在后
常见化合价:一价氢氯钾钠银,二价氧钙钡镁锌等
应用:根据化合价写化学式,根据化学式计算元素化合价
✅ 高频考点:分子基本性质、原子结构示意图、元素周期表单元格、化合价计算、化学式意义、微观示意图分析
易错点:宏观微观表述混淆、元素与原子概念混淆、原子与离子结构判断、化合价与离子符号书写混淆、相对原子质量单位错误
三、中考典型例题
1.选择题
【例题1】(2025·四川成都中考改编)下列生活现象,不能用分子的基本性质解释的是( )
A.端午时节粽飘香
B.压缩气球体积变小
C.沙尘暴起尘土飞扬
D.品红在水中扩散
【解答】
选项A:粽飘香是因为粽子中的香味分子在不断运动,扩散到空气中,能用分子性质解释,不符合题意;
选项B:压缩气球体积变小,是因为压强增大,气体分子间的间隔变小,能用分子性质解释,不符合题意;
选项C:尘土是宏观的固体颗粒,不是微观的分子,尘土飞扬是宏观物体的机械运动,不能用分子的基本性质解释,符合题意;
选项D:品红在水中扩散,是因为品红分子在不断运动,分散到水分子之间,能用分子性质解释,不符合题意。
答案:C
【分析】
核心考点:分子的基本性质,是本专题中考最高频基础考点;
解题方法:明确分子是微观粒子,肉眼不可见,宏观物体的运动不能用分子性质解释;牢牢抓住分子的4个基本性质:质量体积小、不断运动、有间隔、同种分子化学性质相同;
易错点:易将宏观的颗粒运动误判为分子运动,需牢记“闻到气味、扩散、挥发、溶解”均对应分子不断运动,“热胀冷缩、体积压缩、三态变化”均对应分子间隔变化;
踩分点:快速锁定“尘土飞扬”是宏观机械运动,不属于分子运动,完成秒杀。
【例题2】(2025·山东济南中考改编)中国科学院院士张青莲教授主持测定了铟元素的相对原子质量新值。如图是铟元素在元素周期表中的单元格信息与原子结构示意图,下列说法错误的是( )
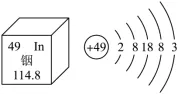
A.铟元素属于金属元素
B.铟原子的核电荷数为49
C.铟原子在化学反应中易失去电子
D.铟的相对原子质量为114.8g
【解答】
选项A:铟元素名称带“钅”字旁,属于金属元素,说法正确,不符合题意;
选项B:元素周期表单元格中,左上角数字为原子序数,原子序数=核电荷数=质子数,因此铟原子的核电荷数为49,说法正确,不符合题意;
选项C:铟原子的最外层电子数为3,小于4,在化学反应中易失去最外层电子形成阳离子,说法正确,不符合题意;
选项D:相对原子质量的单位是“1”,通常省略不写,不是“g”,因此铟的相对原子质量为114.8,说法错误,符合题意。
答案:D
【分析】
核心考点:元素周期表单元格信息提取、原子结构示意图的判断,是中考必考综合考点;
解题方法:
①单元格信息提取:左上角=原子序数=核电荷数=质子数,右上角=元素符号,中间=元素名称,下方=相对原子质量;
②原子结构示意图判断:最外层电子数<4,易失电子;>4,易得电子;=8(氦为2),达到相对稳定结构;
易错点:易忽略相对原子质量的单位,误写为“g”;易将最外层电子数与质子数混淆,错误判断粒子的化学性质;
踩分点:相对原子质量带“g”的选项一定错误,可快速锁定答案。
【例题3】(2025·广东广州中考改编)某化合物的化学式为K2FeO4,已知钾元素的化合价为+1价,氧元素的化合价为-2价,则铁元素的化合价为( )
A.+2
B.+3
C.+4
D.+6
【解答】
设铁元素的化合价为x,根据化合物中各元素正负化合价的代数和为0的规则,可得:
(+1)×2+x+(2)×4=0
解得:x=+6
答案:D
【分析】
核心考点:化合价规则的应用,根据化学式计算元素化合价,是中考必考基础考点,也是化学式书写、化学方程式配平的核心基础;
解题方法:先标出已知元素的化合价,设未知元素化合价为x,再根据“化合物中各元素正负化合价的代数和为0”列等式计算;
易错点:易忽略化学式中元素符号右下角的原子个数,导致计算错误;易混淆化合价的正负号,或误将单质中化合价为0的规则用到化合物中;
踩分点:严格遵循“先标已知、设未知、乘个数、代数和为0”的步骤,避免计算失误。
2.非选择题(微观示意图综合题)
【例题】(2025·重庆中考改编)下图是某化学反应的微观示意图,其中“●”代表氢原子,“○”代表氧原子,回答下列问题:
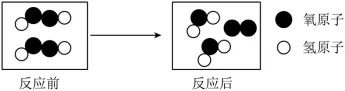
(1)该反应中,保持氧气化学性质的最小粒子是____(填粒子名称);化学变化中的最小粒子是____;
(2)该反应的反应物中,属于单质的是____(填化学式),属于氧化物的是____(填化学式);
(3)该反应的化学方程式为____,基本反应类型为____;
(4)反应前后,____(填“分子”或“原子”)的种类、数目、质量都不变;
(5)通过该微观示意图,可得出化学变化的本质是____。
【解答】
(1)保持氧气化学性质的最小粒子是氧分子;化学变化中的最小粒子是氢原子和氧原子(或原子);
(2)单质是由同种元素组成的纯净物,因此反应物中的单质是O2;氧化物是由两种元素组成,且其中一种是氧元素的化合物,因此反应物中的氧化物是H2O2;
(3)根据微观示意图,反应物是过氧化氢,生成物是水和氧气,反应条件是二氧化锰催化,化学方程式为2H2O2 MnO22H2O+O2↑;该反应符合“一变多”的特征,属于分解反应;
(4)根据质量守恒定律,反应前后,原子的种类、数目、质量都不变;
(5)化学变化的本质是:分子破裂成原子,原子重新组合成新的分子。
【分析】
核心考点:物质的构成、微观反应示意图分析、化学方程式书写、反应类型判断、化学变化的本质,是本专题的综合核心考法,每年中考必考;
解题思路:
①先根据图例,明确每个小球代表的原子,写出反应物和生成物的化学式;
②配平化学方程式,再依次分析物质分类、反应类型、粒子变化;
③紧扣分子、原子的定义与化学变化的本质,完成规范表述;
易错点:易写错化学式、未配平化学方程式;易混淆分子与原子的本质区别,误写化学变化中可分的粒子;易漏标反应条件与气体符号,导致扣分;
化学方程式书写不规范、化学变化本质的表述不完整、粒子名称写错别字,均会直接扣分。
四、易错警示与满分话术
1.高频易错点(错例+规范纠正)
易错类别 | 典型错例 | 规范纠正 |
宏观微观表述混淆 | 二氧化碳由碳原子和氧原子构成 | 宏观表述:二氧化碳由碳元素和氧元素组成;微观表述:二氧化碳由二氧化碳分子构成,二氧化碳分子由碳原子和氧原子构成 |
元素与原子概念混淆 | 水是由2个氢元素和1个氧元素组成 | 元素是宏观概念,只讲种类,不讲个数;纠正:水是由氢元素和氧元素组成;1个水分子由2个氢原子和1个氧原子构成 |
分子性质理解错误 | 热胀冷缩是因为分子的大小随温度变化而改变 | 热胀冷缩、三态变化、体积压缩,改变的是分子间的间隔,分子本身的大小、种类、质量都不会改变 |
原子结构认知错误 | 所有原子都由质子、中子、电子构成 | 普通氢原子(氕原子)的原子核内只有1个质子,没有中子,并不是所有原子都含有中子 |
相对原子质量单位错误 | 氧原子的相对原子质量为16g | 相对原子质量的单位是“1”,通常省略不写,不是“g”;纠正:氧原子的相对原子质量为16 |
化合价与离子符号书写混淆 | 镁离子:Mg2+; 镁元素化合价: | 离子符号:数字在前,正负号在后,标在元素符号右上角,如Mg2+;化合价:正负号在前,数字在后,标在元素符号正上方,如 |
2.中考满分表述模板
1.分子性质解释现象规范表述:
XX现象,是因为XX分子在不断运动或分子间有间隔,随温度或压强变化,分子间间隔发生改变。
示例:墙内开花墙外香,是因为花香分子在不断运动,扩散到空气中;夏天自行车轮胎易爆胎,是因为温度升高,气体分子间的间隔变大,压强增大。
2.元素周期表信息规范表述:
元素周期表单元格中,左上角的数字为原子序数,原子序数=核电荷数=质子数=原子核外电子数;最下方的数字为相对原子质量,单位为1,省略不写。
3.原子结构与元素性质规范表述:
元素的种类由质子数(核电荷数)决定;元素的化学性质由原子的最外层电子数决定;最外层电子数相同的原子,化学性质相似(氦原子除外)。
4.化学变化本质规范表述:
化学变化的本质是分子破裂成原子,原子重新组合成新的分子;化学变化中,分子的种类一定改变,原子的种类、数目、质量一定不变。
5.化合价计算规范步骤:
①标出已知元素的化合价;
②设未知元素的化合价为x;
③根据化合物中各元素正负化合价的代数和为0,列出等式;
④计算得出未知元素的化合价。
五、一轮核心必背清单
(一)基础必背(核心概念,必记)
1.分子:由分子构成的物质,分子是保持其化学性质的最小粒子。
2.原子:化学变化中的最小粒子;化学变化中,分子可分,原子不可分。
3.离子:带电的原子或原子团,分为阳离子(带正电)和阴离子(带负电);原子得失电子形成离子。
4.原子的构成:原子由带正电的原子核和带负电的核外电子构成,原子核由质子和中子构成;核电荷数=质子数=核外电子数=原子序数。
5.元素:质子数(即核电荷数)相同的一类原子的总称;地壳中含量前四位的元素:氧、硅、铝、铁。
6.元素周期表规律:同一周期的原子,电子层数相同,最外层电子数从左到右依次递增;同一主族的原子,最外层电子数相同,化学性质相似,电子层数从上到下依次递增。
7.化合价核心规则:化合物中,各元素正负化合价的代数和为0;单质中,元素的化合价为0。
8.化学式的意义:
①宏观:表示一种物质,表示该物质的元素组成;
②微观:表示该物质的一个分子,表示一个分子的原子构成;
③量的意义:表示该物质的相对分子质量,表示各元素的质量比。
9.化学变化的微观本质:分子破裂成原子,原子重新组合成新的分子。
10.决定关系:质子数决定元素的种类;最外层电子数决定元素的化学性质。
(二)易错必背(避坑关键,杜绝失分)
1.分子是保持物质化学性质的最小粒子,前提是“由分子构成的物质”;由原子构成的物质,保持其化学性质的最小粒子是原子;由离子构成的物质,保持其化学性质的最小粒子是阴、阳离子。
2.原子不一定都含有中子,普通氢原子(氕原子)的原子核内没有中子。
3.原子得失电子形成离子,过程中质子数不变,元素种类不变,核外电子数、最外层电子数改变,化学性质改变。
4.宏观概念(元素、物质)只讲种类,不讲个数;微观概念(分子、原子、离子)既讲种类,又讲个数,二者不能混淆。
5.最外层电子数相同的原子,化学性质不一定完全相似,如氦原子最外层2个电子,镁原子最外层2个电子,二者化学性质不相似。
6.相对原子质量不是原子的实际质量,是一个比值,单位是“1”,通常省略不写。
7.同种元素的原子和离子,质子数一定相同,核外电子数一定不同;质子数相同的粒子,不一定属于同种元素,如水分子和氖原子质子数均为10,不属于同种元素。
8.氧化物一定含有氧元素,但含有氧元素的化合物不一定是氧化物,如高锰酸钾、氢氧化钠都不是氧化物。
(三)技巧必背(解题秒杀,提速提分)
1.常见元素化合价口诀:
一价氢氯钾钠银,二价氧钙钡镁锌,
三铝四硅五价磷,二三铁、二四碳,
二四六硫都齐全,铜汞二价最常见,
单质零价永不变。
2.常见原子团化合价口诀:
负一硝酸氢氧根,负二硫酸碳酸根,
负三记住磷酸根,正一价的是铵根。
3.分子性质解题秒杀技巧:
闻到气味、扩散、溶解、挥发→分子在不断运动;
热胀冷缩、三态变化、体积压缩→分子间有间隔;
肉眼可见的宏观颗粒运动→不能用分子性质解释。
4.微观示意图解题步骤:
①标原子种类,写反应物、生成物的化学式;
②配平化学方程式;
③分析物质分类、反应类型、化合价变化、粒子变化规律。
5.化合价与化学式互写技巧:
正价在前,负价在后,交叉约简,个数定数;代数和为0,检验正误。
六、分层巩固专项训练
(一)基础题(5道,复习达标,考点全覆盖)
1.(考点:分子的基本性质)下列事实的微观解释错误的是( )
A.酒香不怕巷子深——分子在不断运动
B.6000L氧气可压缩入40L的钢瓶中——分子间有间隔
C.水结冰后体积变大——水分子的体积变大
D.湿衣服在阳光下比阴凉处干得快——温度越高,分子运动速率越快
2.(考点:原子结构与元素概念)决定元素种类的是( )
A.质子数
B.中子数
C.最外层电子数
D.相对原子质量
3.(考点:元素周期表信息提取)如图是钠元素在元素周期表中的单元格,下列说法正确的是( )
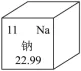
A.钠属于非金属元素
B.钠原子的核内质子数为11
C.钠的相对原子质量为22.99g
D.钠原子在化学反应中易得电子
4.(考点:化合价计算)二氧化氯(ClO2)是常用的饮用水消毒剂,其中氯元素的化合价为()
A.1
B.+1
C.+4
D.+5
5.(考点:分子、原子、离子的概念)下列关于分子、原子、离子的说法,正确的是( )
A.分子是化学变化中的最小粒子
B.原子得失电子形成离子
C.分子的质量一定比原子大
D.所有物质都由分子构成
(二)提高题(4道,易错突破,适配中考难度)
1.(考点:宏观微观表述辨析)下列关于葡萄糖(C6H12O6)的说法,正确的是()
A.葡萄糖由6个碳元素、12个氢元素、6个氧元素组成
B.葡萄糖由碳原子、氢原子、氧原子构成
C.葡萄糖中碳、氢、氧元素的质量比为1:2:1
D.1个葡萄糖分子由6个碳原子、12个氢原子、6个氧原子构成
2.(考点:原子结构示意图与离子判断)下列粒子结构示意图中,表示阴离子的是( )
A.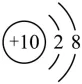 B.
B.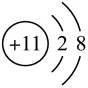 C.
C.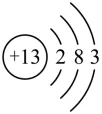 D.
D.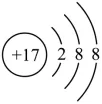
3.(考点:元素周期表规律)下列关于元素周期表的说法,错误的是( )
A.同一周期的元素,电子层数相同
B.同一主族的元素,最外层电子数相同
C.元素周期表中,金属元素都在左下方,非金属元素都在右上方
D.原子序数=核电荷数=质子数=原子核外电子数
4.(考点:微观示意图综合分析)如图是某化学反应的微观示意图,下列说法错误的是( )
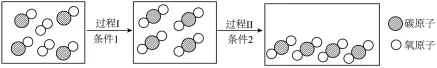
A.该反应属于化合反应
B.反应前后原子的种类、数目不变
C.反应前后分子的种类不变
D.该反应中,反应物的分子个数比为2:1
(三)拓展题(1道,能力拔高,综合应用)
(考点:物质构成的奥秘全专题综合应用)结合所学知识,回答下列问题:
(1)现有以下粒子:①H2O ②Ne ③Mg2+ ④NH3 ⑤NH4+,
其中属于阳离子的是____(填序号,下同),
与氖原子电子层结构相同的粒子是____,
由分子构成的物质是____。
(2)某元素的原子结构示意图为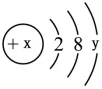 ,若该原子为第三周期的铝原子,则x=____,y=____,该原子在化学反应中易____(填“得到”或“失去”)电子,形成的离子符号为____。
,若该原子为第三周期的铝原子,则x=____,y=____,该原子在化学反应中易____(填“得到”或“失去”)电子,形成的离子符号为____。
(3)已知某化合物的化学式为Na2SeO3,其中钠元素为+1价,氧元素为2价,则硒元素(Se)的化合价为____。
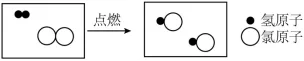
(4)下图是氢气在氯气中燃烧的微观示意图,写出该反应的化学方程式____,该反应中,不变的粒子是____(填粒子名称)。
【解答提示】
(1)阳离子是带正电的粒子,先判断各粒子的带电情况;氖原子的核外电子数为10,找出核外电子数为10的粒子;由分子构成的物质,化学式对应分子;
(2)铝元素的原子序数为13,原子序数=质子数=x,第三周期原子有3个电子层,铝原子最外层电子数为3;最外层电子数<4,易失电子,形成带3个单位正电荷的铝离子;
(3)根据化合物中各元素正负化合价的代数和为0,列等式计算;
(4)根据微观示意图,反应物是氢气和氯气,生成物是氯化氢,反应条件是点燃,配平化学方程式;化学变化中原子的种类不变。
【参考答案】
基础题:1.C 2.D 3.B 4.C 5.B
提高题:1.D 2.C 3.C 4.C
拓展题:(1)③、⑤;③;①、④;
(2)13;3;失去;Al3+;
(3)+4;
(4)H2+Cl2点燃2HCl;氢原子和氯原子







