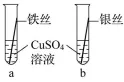
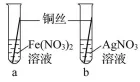
金属活动性顺序的验证与探究的中考命题特点
金属活动性顺序是贯穿中学化学教学的核心概念之一,它为学生理解金属的化学性质、预测置换反应的可能性提供了直观的工具,承载对元素观、变化观等化学观念的考查,区分度高,是中考化学的热门考点。往往置于真实问题情境中,结合生活实际、工业生产,考查控制变量法、对比实验法、分类讨论等科学方法的运用,涉及科学探究、证据推理、模型认知、逻辑推理等综合能力的考查。
中考命题具有以下特点:
题型 | 难度 | 考查重点 |
定性判断、反应原理 | 基础 | 根据反应现象判断金属活动性顺序,书写反应 |
方案设计与评价类 | 重点 | 设计实验方案、评价方案合理性 |
滤液滤渣成分分析类 | 难点 | 综合考查逻辑推理与分类讨论,回收工艺 |
数字化实验类 | 创新 | 借助传感器分析数据,考查信息迁移能力 |
命题趋势:
1.重视能力立意与素养导向
科学思维培养:证据推理(从实验现象推断活动性);模型认知(构建滤液成分分析模型)。
探究实践能力:变量控制(考查酸浓度、金属形状等变量对反应速率的影响);方案优化(评价实验设计缺陷)。
2.情境设计与跨学科融合
生活与科技情境:金属蚀刻画、航母电缆材料、龙鳞钢性能等真实案例融入命题。
环保主题:废液回收(如将含Cu²⁺废液转化为FeSO₄)体现绿色化学理念。
这些特点体现了中考命题对化学学科核心素养的重视,旨在考查学生在真实情境中运用化学知识解决问题的能力。
教学突破
培养学生能运用研究物质性质的一般思路与方法,从物质类别的视角,依据金属活动性顺序等,初步预测常见的金属的主要性质,设计实验方案,分析、解释有关的实验现象,进行证据推理,得出合理的结论。
常见金属的活动性顺序:
1.常见金属活动性顺序表

2.验证与探究依据
(1)在金属活动性顺序表里,位于 氢 前面的金属能与稀盐酸、稀硫酸发生 置换 反应;位于氢后面的金属不与稀盐酸、稀硫酸发生反应。
(2)在金属活动性顺序表里,位于前面的金属(K、Ca、Na除外)能把后面的金属从它的 盐溶液 中置换出来。
设计实验方案验证已知金属的活动性:
1.两种金属的活动性
判断方法 | 操作方法 | 预期现象与结论 |
金属能否与稀硫酸或稀盐酸反应 | 将金属片插入稀硫酸或稀盐酸中,观察 是否产生气泡 | 若有 气泡 产生,说明该金属在金属活动性顺序中排在 氢之前 ,否则排在 氢之后 (有无气泡) |
金属能否与盐溶液发生置换反应 | 将金属插入某盐溶液中,观察现象(金属表面是否有 另一种金属析出 及溶液 颜色变化 ) | 如果能将盐溶液中的金属置换出来,说明插入溶液中的金属的活动性较盐溶液中所含金属的活动性 强 ,否则相反 |
注意:实验前,需先将金属进行打磨,以除去金属表面的氧化物或污物。
2.三种金属的活动性
思路 | 两金夹一盐 | 两盐夹一金 |
设计 方案 | 选用三种金属中活动性最 强 和最 弱 的两种金属的 单质 及活动性介于两种金属之间的金属的 盐溶液 作为试剂 | 选用三种金属中活动性排在 中间 的金属单质及其他两种金属的 盐溶液 作为试剂 |
举例 |
|
|
结论 | 金属活动性顺序:Fe>Cu>Ag |
注意:比较金属活动性时需要注意控制变量,如酸的浓度、金属的形状和大小需保持一致。
3.多种金属的活动性
(1)将多种金属分别放入 稀盐酸或稀硫酸 中,比较并将其分为氢前金属和氢后金属两类;
(2)根据比较两种或三种金属活动性的方法,分别比较氢前金属和氢后金属的活动性,然后进行综合排序。
金属与盐溶液反应后溶质、滤渣成分的探究:
(1)多种金属与一种盐溶液反应, 最活泼 的金属先反应。
例:锌和铁同时放入硫酸铜溶液中, 锌 先反应。
(2)一种金属与多种盐溶液反应,金属先和 最不活泼 的金属的盐溶液反应。
例:铁放入硫酸铜与硝酸银的混合溶液中,铁先与 硝酸银 反应。
(3)反应混合物过滤后,滤渣中一定有 最不活泼 的金属单质,滤液中一定有 最活泼 的金属的离子。
(4)滤渣与滤液中的物质不能发生反应。
常见错误汇总
易错点 | 正确理解 |
金属与酸反应越剧烈=活动性越强 | 错误:不能用金属与盐溶液反应的剧烈程度判断活动性 |
所有金属都能置换酸中的氢 | 错误:只有位于氢前面的金属才能与酸反应生成氢气 |
所有金属都能置换盐溶液中的金属 | 错误:K、Ca、Na等非常活泼的金属除外,它们会先与水反应 |
盐溶液随便选都可以 | 错误:必须是可溶性盐溶液,不溶于水的盐无法发生置换反应 |
典型考题(转载)
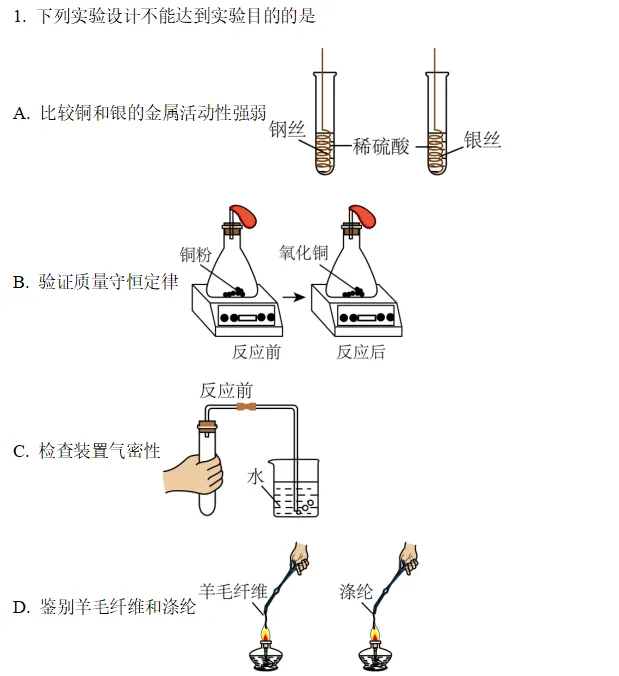
【答案】A
【解析】A、铜和银的金属活动性都在氢之后,将铜丝和银丝分别放入稀硫酸中,二者都不与稀硫酸反应,均无明显现象,无法比较铜和银的金属活动性强弱,该实验设计不能达到目的;
B、铜粉在空气中加热与氧气反应生成氧化铜,反应在密闭装置中进行,根据反应前后天平是否平衡,可以验证质量守恒定律,该实验设计能达到目的;
C、检查装置气密性时,将导管一端浸入水中,用手紧握试管,若导管口有气泡冒出,松开手后导管内形成一段水柱,说明装置气密性良好,该实验设计能达到目的;
D、羊毛纤维的主要成分是蛋白质,灼烧时有烧焦羽毛的气味;涤纶属于合成纤维,灼烧时有特殊气味,通过灼烧闻气味可以鉴别羊毛纤维和涤纶,该实验设计能达到目的。
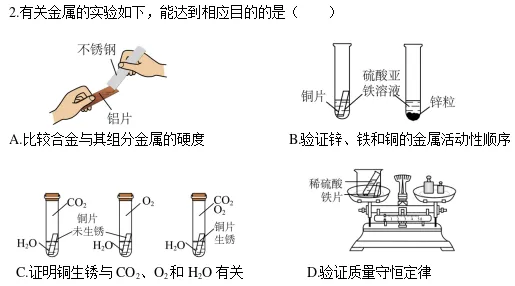
【解答】A、0~15s,压强迅速上升是因为向锥形瓶中注入了液体,气体被压缩从而引起气体压强增大,故A正确;
B、根据题干信息,锥形瓶内集满二氧化碳,如果100s时二氧化碳被完全吸收,此时气体的压强应变为接近0(存在少量水蒸气),但100s时瓶内气体压强仍较大,说明二氧化碳没有被完全吸收,故B错误;
C、实验a中的反应是水和二氧化碳反应生成碳酸,碳酸能使紫色石蕊溶液变红,故C正确;
D、对比三组实验,实验c中压强变化最大,故氢氧化钠溶液吸收二氧化碳的效果最好,故D正确。
故选:B。
3.镍是一种重要的金属。将废旧坡莫合金(含镍、铁和铜等)浸入800℃液态镁中形成镁镍合金,再经如右下图所示的真空蒸馏,可实现镁和镍的分离与回收。下列说法正确的是
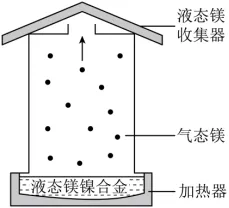
A. 合金的硬度一般比其组成金属的小 B. 镁的沸点比镍的高
C. 真空蒸馏过程中,镁原子间的间隙发生改变D. 坡莫合金可完全溶于足量稀硫酸中
【答案】C
【解析】A、合金的硬度一般比其组成金属的大,而不是小,A错误。
B、从真空蒸馏能够分离镁和镍,且镁以气态形式被收集,可推断出镁的沸点比镍的低,B错误。
C、真空蒸馏过程中,镁由液态变为气态,物质的状态发生变化,分子(原子)间的间隙会发生改变,C正确。
D、坡莫合金中含铜,铜不与稀硫酸反应,所以坡莫合金不能完全溶解于足量稀硫酸中,D错误。
4.下列实验方案合理的是( )
选项 | 实验目的 | 实验方案 |
A | 鉴别生理盐水、葡萄糖溶液 | 观察溶液颜色 |
B | 鉴别C、Fe、CuO粉末 | 取样,分别加入足量稀硫酸,观察现象 |
C | 除去CuSO4溶液中的少量FeSO4 | 加入足量Fe粉,充分反应后过滤 |
D | 除去NaOH溶液中的少量Na2CO3 | 加入适量CaCl2溶液,充分反应后过滤 |
A.A B.B C.C D.D
【解析】解:A、生理盐水、葡萄糖溶液均为无色液体,用观察溶液颜色的方法不能鉴别,故选项实验方案不合理。
B、稀硫酸与氧化铜反应生成硫酸铜和水,会观察到黑色粉末溶解,溶液变蓝色;与铁粉反应生成氢气,会观察到产生气泡;与碳不反应,无明显现象,能出现三种明显不同的现象,可以鉴别,故选项实验方案合理。
C、足量Fe粉能与CuSO4溶液反应生成硫酸亚铁溶液和铜,反而会把原物质除去,不符合除杂原则,故选项实验方案不合理。
D、Na2CO3能与适量CaCl2溶液反应生成碳酸钙沉淀和氯化钠,能除去杂质但引入了新的杂质氯化钠,不符合除杂原则,故选项实验方案不合理。
故选:B。
5.废弃的镍锌电池中含有锌、铜、银、镍四种金属。为探究镍的金属活动性顺序并回收银,某校化学兴趣小组的同学设计了如图所示实验流程(反应条件已略去)。已知镍的相对原子质量为59。
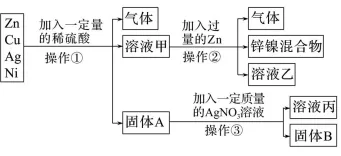
(1)固体A的成分是铜、银。
(2)实验流程中,操作①②③为过滤。
(3)向固体A中加入一定量的AgNO3溶液后发生反应的化学方程式为Cu+2AgNO3===Cu(NO3)2+2Ag。
(4)由该实验可知,锌、铜、银、镍的金属活动性顺序由大到小为锌>镍>铜>银。
6. 废金属是宝贵的资源。
(1)废铜块能制成薄铜片,利用了铜的________性。
(2)用废铜生产硫酸铜的过程中,涉及反应:CuO+ H2SO4=CuSO4+ H2O,该反应的实验现象:黑色固体逐渐溶解,________。
(3)利用废锌与含硫酸镍的废液反应回收镍,反应的化学方程式:Zn+ NiSO4=Ni + ZnSO4由此判断Zn、Ni两种金属中,金属活动性较强的是________。
(4)我国科学家利用废弃金属资源,合成了催化剂(含镍、钙、铁复合金属氢氧化物),将CO2和电解水产生的H2催化转化为CH4和CO等物质,实现CO2的捕集和应用。
①反应3CO2+6H2催化剂CH4+2CO+4X中,X为______。
②CO2的捕集是应对气候变化的措施之一。请你提出另一种捕集CO2的方法:______。
【答案】(1)延展(或良好的延展)
(2)溶液由无色变为蓝色
(3)Zn或锌(4)①. H2O②. 用水吸收CO2(或其他合理答案)
7.云南斑铜“妙在有斑,贵在浑厚”,其制作技艺是国家非物质文化遗产。
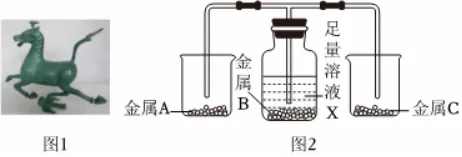
(1)《滇南闻见录》记载:“自来铜(铜基合金),不可经火,须生锤成器”,通过捶打将斑铜塑成不同形状,体现了金属的______性。斑铜的熔点比纯铜______ (填“高”或“低”)。
(2)斑铜主要含有铜、锌、锡、铁等。用如图2所示装置及试剂,通过一次实验验证锌、铁、铜的金属活动性,回答下列问题。
①组装好装置,装入试剂前,应先______。
②集气瓶中金属B和溶液X可能的组合为______(任填一组)。
【解答】解:(1)通过捶打将斑铜塑成不同形状,体现了金属的延展性。斑铜是铜基合金,其熔点比纯铜低,因为合金的熔点通常低于其组成的纯金属的熔点。故答案为:延展;低。
(2)①在装入试剂前,应先检查装置的气密性,确保装置不漏气,以保证实验结果的准确性。故答案为:检查装置的气密性;
②为了验证锌、铁、铜的金属活动性,可以选择铁(Fe)与足量硫酸(H2SO4)反应生成硫酸亚铁,硫酸亚铁和铜不反应,铜和硫酸不反应,硫酸亚铁和锌反应,锌与硫酸反应,可以说明活动性:锌>铁>铜。故答案为:Fe和H2SO4(答案不唯一)。
8.金属矿物是宝贵的自然资源。
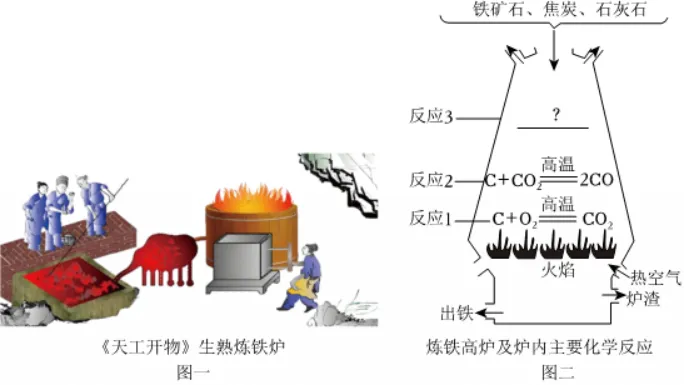
(1)图一展示了古代炼铁的过程,其中将生铁炼成熟铁(钢)的原理是______。
(2)图二是现代高炉炼铁的过程,写出反应3的化学方程式______。
(3)世界上每年因腐蚀而报废的金属相当于年产量的20%﹣40%,请你提出一种预防金属锈蚀的具体方法______。
(4)某化工厂为回收废旧金属,向含有AgNO3和Cu(NO3)2的废液中加入一定质量的锌粉,充分反应后过滤,得到无色滤液和滤渣,滤渣中可能含有______(填化学式,下同),滤液中的溶质是______。
【答案】降低含碳量; 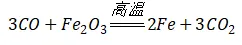 ; 刷漆或涂油; Zn ; Zn(NO3)2;
; 刷漆或涂油; Zn ; Zn(NO3)2;