
一、真题拆解:一道题,藏着酸碱盐教学的 3 个关键盲区
我们先来看这道题的核心设问,拆解它背后的命题逻辑:
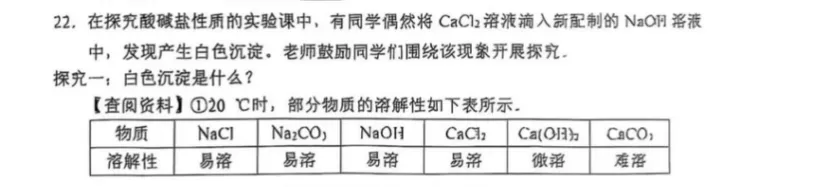
(1)白色沉淀是什么?—— 打破 “思维定式”,理解物质溶解性的本质很多学生看到 CaCl₂和 NaOH 反应,第一反应是 “生成 CaCO₃沉淀”,但题目给的溶解性表中,Ca (OH)₂微溶、CaCO₃难溶,结合 “新制 NaOH 溶液” 这一条件,就能判断沉淀是 Ca (OH)₂。
教学反思: 很多时候,我们的教学太依赖 “复分解反应生成沉淀的常见组合”,却忽略了溶解性表的灵活应用。学生只会背 “Cl⁻和 Ag⁺生成沉淀、SO₄²⁻和 Ba²⁺生成沉淀”,却不会根据题目给的溶解性信息,分析微溶物也可能形成沉淀。这提醒我们,在复习时要带着学生 “读透溶解性表”,不仅要背常见沉淀,更要理解 “微溶物在浓度较高时也会形成沉淀” 的本质。
(2)用热水洗涤沉淀的目的是什么?—— 用温度影响溶解度,解决 “异常现象”
题目中提到 “Ca (OH)₂的溶解度随温度升高而降低”,用热水洗涤,是为了降低Ca(OH)₂的溶解度,同时除去沉淀表面的杂质,避免杂质对后续实验造成干扰。
教学反思: 我们在复习溶解度时,大多聚焦 “温度对硝酸钾、氯化钠溶解度的影响”,却很少强调 “Ca (OH)₂溶解度随温度升高而降低” 这一特殊规律。而这道题,把这一规律和实验除杂结合起来,提醒我们:溶解度的特殊性质,是解决实验异常现象的关键,复习时要把 “溶解度规律” 和 “实验操作” 结合起来,而不是孤立地讲概念。
(3)久置 NaOH 溶液溶质成分探究 —— 复分解反应的除杂干扰,是学生最容易踩的坑这道题的核心难点,是步骤①中 “加入过量 CaCl₂溶液” 的目的,以及后续酚酞检验 NaOH 的严谨性。
加入过量 CaCl₂,是为了完全除去溶液中的Na₂CO₃,避免其碱性对后续 NaOH 的检验造成干扰;
但原方案中,CaCl₂和 Na₂CO₃反应会生成 NaCl,NaCl 溶液呈中性,看似不影响,却有一个隐藏漏洞:如果 NaOH 已经完全变质,生成的 Na₂CO₃和过量 CaCl₂反应后,溶液中没有 NaOH,酚酞不会变红;但如果 NaOH 部分变质,反应后溶液中既有 NaCl,也有 NaOH,酚酞会变红。可为什么说原方案不严谨?
这里的关键是:CaCl₂和 NaOH 也可能生成微溶的 Ca (OH)₂沉淀,如果 CaCl₂过量,可能会和 NaOH 反应,消耗 NaOH,导致后续酚酞检验出现偏差。
教学反思: 这也是酸碱盐教学中最容易忽略的点:在除杂时,除了要考虑杂质离子,还要考虑除杂试剂和原物质是否会发生反应,尤其是微溶物的干扰。学生会背 “用 CaCl₂检验并除去 Na₂CO₃”,却不会考虑 CaCl₂和 NaOH 的反应,这也是后续优化方案的核心。
二、酸碱盐复习,要跳出 “死记硬背”,走向 “证据推理”
这道题给了我 3 个非常深刻的教学启示:
1.不要让学生只背 “结论”,要教他们用 “证据” 推理
很多学生做这道题时,会直接把沉淀当成 CaCO₃,就是因为他们习惯了 “Ca²⁺和 CO3²⁻生成沉淀” 的结论,却没有根据题目给的 “新制 NaOH 溶液”“溶解性表” 这些证据,进行推理。我们在复习时,要多给学生做 “证据推理” 训练,比如让他们根据溶解性表、实验现象,一步步推导沉淀成分,而不是直接给出答案。
2.把 “异常实验现象” 当成复习的切入点
这道题的题干,就是一个真实的实验异常现象:CaCl₂滴入 NaOH 溶液,居然出现了白色沉淀。我们在教学中,也可以多引入这样的异常现象,比如 “NaOH 溶液滴入酚酞后,先变红又褪色”“敞口放置的澄清石灰水,变浑浊后又变澄清”,让学生带着问题去探究,比单纯讲知识点更有代入感。
3.除杂与检验,要讲清 “严谨性”,不是只讲 “方法”
很多学生背熟了 “检验 NaOH 是否变质,先加 CaCl₂除 Na₂CO₃,再加酚酞”,却不知道为什么要加过量 CaCl₂,也不知道这个方案的漏洞在哪里。我们在复习时,要带着学生 “找茬”:如果 CaCl₂不足,会有什么影响?如果用 Ca (OH)₂代替 CaCl₂,会引入什么杂质?只有把这些 “为什么” 讲透,学生才能真正掌握实验探究的严谨性。
三、适配好题:一道改编题,帮学生巩固 “NaOH 变质探究” 的核心考点
改编题:某化学兴趣小组的同学,在实验室发现一瓶敞口放置的 NaOH 溶液,对其溶质成分产生了好奇,开展了如下探究:
【查阅资料】
① 20℃时,Ca (OH)₂微溶于水,CaCO₃难溶于水;② CaCl₂溶液、NaCl 溶液均呈中性,Na₂CO₃溶液呈碱性;
③ CaCl₂和 NaOH 反应可能生成微溶的 Ca (OH)₂沉淀。
【提出猜想】
猜想 Ⅰ:溶质为 NaOH(未变质);
猜想 Ⅱ:溶质为 NaOH 和 Na₂CO₃(部分变质);
猜想 Ⅲ:溶质为 Na₂CO₃(完全变质)。
【实验探究】
(1)甲同学取少量溶液,滴加足量稀盐酸,观察到有气泡产生,说明猜想______不成立。
(2)乙同学设计了如下方案:取少量溶液,加入过量 CaCl₂溶液,充分反应后过滤,向滤液中滴加酚酞溶液。
① 加入过量 CaCl₂溶液的目的是______;
② 若观察到______,说明猜想 Ⅱ 成立;若观察到______,说明猜想 Ⅲ 成立。
(3)丙同学认为乙同学的方案不够严谨,理由是______。请你优化该方案:取少量溶液,加入过量的______溶液(填 “CaCl₂” 或 “BaCl₂”),充分反应后过滤,向滤液中滴加酚酞溶液,若溶液变红,说明猜想 Ⅱ 成立。
【反思拓展】敞口放置的 NaOH 溶液容易变质,原因是______(用化学方程式表示),因此 NaOH 溶液需要______保存。
参考答案:
(1)Ⅰ;
(2)① 完全除去溶液中的 Na₂CO₃,防止其碱性干扰 NaOH 的检验;② 产生白色沉淀,滤液变红;产生白色沉淀,滤液不变红;
(3)CaCl₂和 NaOH 反应可能生成微溶的 Ca (OH)₂沉淀,干扰实验;BaCl₂;
【反思拓展】
CO₂ + 2NaOH = Na₂CO₃ + H₂O;密封。
说明:本次【好题+反思】由本工作室许青霞老师提供,仅供教学参考。







