
1. 下列说法不正确的是( )
A. 铁制品在潮湿的空气中比在干燥的空气中易生锈
B. 葡萄糖(C6H12O6)中C、H、O元素的质量比为1:2:1
C. 地壳中含量最多的金属元素是Al
D. 分子都是由原子构成的
【答案】B

2.我国自主建造的第一艘航母下海,为保证航母的使用寿命,下列防锈措施不可行的是( )
A.用抗锈蚀性能优异的合金制造航母零部件
B.刷防锈漆
C.船体表面镀一层黄金
D.给某些部位涂油
3.保护金属资源的有效途径,不包括下列的( )
A.合理开采矿物 B.寻找金属替代品
C.回收利用金属 D.禁止使用铁制品
4.下列关于金属的说法中,错误的是( )
A.铜有良好的导电性,常用于制作导线
B.所有的金属都能与稀盐酸反应
C.铁制品在干燥的空气中不易生锈
D.不能用铁桶盛放硫酸铜溶液
5.“宏观辨识与微观探析”是化学学科的核心素养之一。对下列事实或做法的解释正确的是( )
A.铁质水龙头表面镀铬可防锈--改变了金属的内部结构
B.众人拾柴火焰高--可燃物越多,着火点越低,越易燃烧
C.用明矾净水--明矾可降低水中钙、镁离子的含量
D.氧气能被液化贮存于钢瓶--分子间有间隔且间隔能改变
6.下列关于铁、锌、铜三种金属及其合金的说法错误的是( )
A.铁在潮湿的空气中易生锈
B.黄铜(铜与锌的合金)的硬度大于纯铜
C.可以用铁桶盛放硫酸铜溶液
D.可以用稀硫酸鉴别锌与铜的金属活动性强弱
7.铝和铁是两种常见的活泼金属,生活中铝制品不易被腐蚀,原因是其表面生成致密的Al2O3薄膜,氧化铝中铝元素的化合价为 +3价。铁制品易生锈,防止铁生锈很重要,请写出一种防止铁生锈的方法。
【解答】解:氧元素显-2价,设铝元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:2x+(-2)×3=0,则x=+3价。
为了防止钢铁的锈蚀,人们常采用在其表面刷漆、涂油或镀上其他金属等覆盖保护膜的方法,这些方法都能够防止锈蚀的共同原理是隔绝氧气和水。
故答案为:+3;刷漆等。
8.炼铁的主要原料是赤铁矿(主要成分是Fe2O3)、焦炭、空气等,转化过程如图:

(1)②中,反应为CO2+C 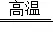 2CO,其中化合价发生改变的元素是 碳 。
2CO,其中化合价发生改变的元素是 碳 。
(2)③中,CO与Fe2O3反应的化学方程式为 Fe2O3+3CO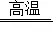 2Fe+3CO2。
2Fe+3CO2。
【解答】解:(1)反应为CO2+C 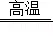 2CO,二氧化碳、碳、一氧化碳中碳元素的化合价分别是+4价、0、+2价,故化合价发生改变的元素是碳。
2CO,二氧化碳、碳、一氧化碳中碳元素的化合价分别是+4价、0、+2价,故化合价发生改变的元素是碳。
(2)③中,CO与Fe2O3反应生成铁和二氧化碳,反应的化学方程式为Fe2O3+3CO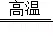 2Fe+3CO2。
2Fe+3CO2。
故答案为:(1)碳;(2)Fe2O3+3CO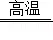 2Fe+3CO2。
2Fe+3CO2。
9.古往今来,金属材料和制品在我们的社会生活中一直起着非常重要的作用。
(1)考古工作者发现铁质的出土文物往往锈蚀严重,铁生锈的条件是 铁与氧气、水同时接触 。在实验室常用稀盐酸清除铁锈,化学方程式为 Fe2O3+6HCl═2FeCl3+3H2O 。
(2)近年来,我国高铁建设促进了经济、社会的快速发展。制造铁轨的材料是合金钢,主要原因是合金钢具有 硬度大(或机械强度好、或韧性好等) 的优越性能(要求只答一条)。
(3)某同学在实验室进行了两个有关金属性质的实验:
实验Ⅰ:硫酸铝溶液和铁粉混合
实验Ⅱ:硫酸铜溶液与铁粉混合
在上述两个实验结束后,该同学将实验Ⅰ和Ⅱ的物质全部倒入同一个烧杯中,发现烧杯内的红色固体明显增多,原因是 实验Ⅱ中硫酸铜溶液有剩余,而实验Ⅰ中的铁粉又能与实验Ⅱ中剩余的硫酸铜发生置换反应生成铜和硫酸亚铁 (用文字说明)。一段时间后过滤,向滤渣中滴加盐酸,结果没有气泡产生。那么,滤液中所含金属离子的情况可能是②⑤〔填写序号)。
①A13+②A13+、Fe2+③A13+、Fe3+④Fe2+、Cu2+⑤A13+、Fe2+、Cu2+
【解答】解:(1)铁在与氧气、水共存时会发生锈蚀;铁锈的主要成分是氧化铁,与盐酸反应生成氯化铁和水,反应的化学方程式是:Fe2O3+6HCl═2FeCl3+3H2O;故填:铁与氧气、水同时接触;Fe2O3+6HCl═2FeCl3+3H2O;
(2)合金钢的主要成分是铁、锰、碳,其韧性好,硬度大,纯铁硬度小且脆;所以铁轨用合金钢;故填:硬度大(或机械强度好、或韧性好等);
(3)在金属活动性顺序中,铁排在铝后面,排在铜前面,所以实验Ⅰ中硫酸铝溶液和铁粉不反应;实验Ⅱ中铁能置换出硫酸铜中的铜,同时生成硫酸亚铁;将实验Ⅰ和Ⅱ的物质全部倒入同一个烧杯中,发现烧杯内的红色固体明显增多,这是因为实验Ⅱ中硫酸铜溶液有剩余,而实验Ⅰ中的铁粉又能与实验Ⅱ中剩余的硫酸铜发生置换反应生成铜和硫酸亚铁;一段时间后过滤,向滤渣中滴加盐酸,结果没有气泡产生,说明铁粉已经完全反应,滤渣为铜,滤液中一定含有硫酸铝、硫酸亚铁,可能含有硫酸铜,即滤液中含有的金属离子有一下几种可能:铝离子、亚铁离子;铝离子、亚铁离子和铜离子,故填:实验Ⅱ中硫酸铜溶液有剩余,而实验Ⅰ中的铁粉又能与实验Ⅱ中剩余的硫酸铜发生置换反应生成铜和硫酸亚铁;②⑤。
10.根据图7所示的实验回答问题。
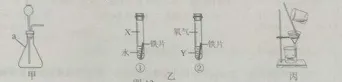
(1)甲装置中仪器a的名称是______;该装置作为气体发生装置对反进物状态和反应条件的要求是_________。
(2)乙是探究影响铁锈蚀快慢因素的实验,为探究氯化钠是否可以加快铁的锈蚀,试管①中的物质X和试管②中的物质Y分别是______________。
(3)丙是粗盐提纯实验中的过滤操作。过滤时,最好先将上层液体倒入过滤器,然后再倒入混有沉淀的液体,以免________,使过滤速度过慢。在粗盐提纯实验中,若倾倒液体时液面高于滤纸边缘(其他操作均正确)。则得到的精盐质量会_____(选镇 “偏大”“不变”或“偏小”)。
【答案】(1)锥形瓶;固-液或液-液不加热;(2) X是氧气,Y是氯化钠溶液;(3)沉淀堵塞滤纸;偏大。
【解析】(1) 仪器a是锥形瓶;甲装置固-液或液-液不加热;(2) 铁生锈是铁与氧气、水共同作用形成的,即X是氧气,Y是氯化钠溶液;(3)液体中的沉淀溶液堵塞滤纸,影响过滤速率;倾倒液体时液面高于滤纸边缘,部分待测液会直接进入烧杯中,使过滤后食盐质量增加,使得到的精盐质量偏大。






