
酸碱盐的中考命题特点
酸碱盐的性质及应用既是物质的分类与性质、复分解反应及发生条件等核心概念的集大成者,也是连接实验操作、生活应用(如改良土壤、清洁剂原理、胃酸中和)的关键枢纽。近年命题更强调“用知识解决真实问题”,而非孤立记忆。中考化学中,酸碱盐相关知识点的直接考查与综合延伸题型占比高,涉及选择、实验探究、除杂鉴别、图像信息等题型,命题高度生活化、情境化、综合性强。
中考酸碱盐的命题“以生活情境为壳、以反应规律为核、以能力应用为标”,其命题呈现三大鲜明特点:
1.高度综合化:串联金属、氧化物、离子反应、实验操作等全链条知识,极少孤立考查单一性质;
2.题型生活化、情境化:常结合土壤改良、废水处理、厨房灭火器、肥料施用、清洁剂成分等真实场景命题;
3.重视能力素养考查:融合跨学科知识,从基础记忆(如指示剂变色)逐步升级为证据推理、方案设计(如除杂/鉴别)和定量分析(如pH变化曲线)等。
考查方向主要有:
1.溶液酸碱性判断:pH试纸使用、指示剂变色(石蕊红/蓝、酚酞仅碱红)、酸雨标准(pH<5.6);
2.酸碱盐特性、通性与反应条件:基本实验操作(稀释浓硫酸)、实验现象分析、化学方程式书写、反应能否发生判断、无明显现象实验探究;
3.物质的变质、物质鉴别与除杂:实验探究;利用特征现象区分(如CO₃²⁻加酸冒泡);除杂“不增、不减、不变、易分”原则;
4.常见物质俗称与用途:NaOH(烧碱/火碱/苛性钠)、Ca(OH)₂(熟石灰/消石灰)、Na₂CO₃(纯碱/苏打)、NaHCO₃(小苏打)及其对应用途等。
这些特点旨在考查学生在真实情境中运用化学知识解决问题的能力。
教学突破
物质 | 阳离子 | 阴离子 | 主要物质 |
酸 | H+ | 酸根离子 | H2SO4、HCl |
碱 | 金属离子 | OH- | NaOH、Ca(OH)2 |
盐 | 金属离子 | 酸根离子 | NaCl、Na2CO3 |
酸碱盐看似复杂,其实只要联系生活,把性质和用途绑定,复习时多结合生活场景思考,找准物质类别、溶液酸碱性和反应规律,问题就能迎刃而解。
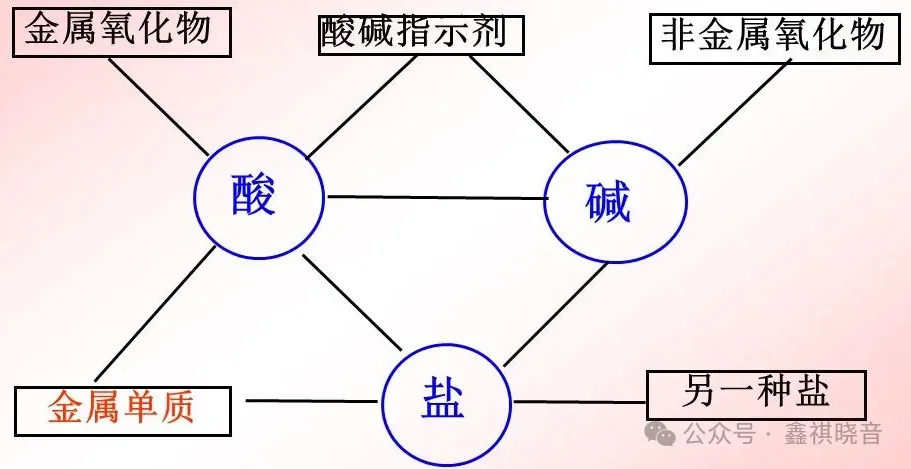
酸碱盐反应规律:
(1)金属单质 + 酸→盐 + 氢气 (置换反应)
金属活动性顺序排在氢前的金属能从酸(盐酸和稀硫酸)溶液中把氢置换出来
(2)金属单质 + 盐(溶液) →另一种金属 + 另一种盐(置换反应)
金属活动性顺序排在前面的金属(K、Ca、Na除外)能把排在后面的金属从它的盐溶液里置换出来。
(3)金属氧化物 +酸 →盐 + 水(复分解反应)
(4)非金属氧化物 +碱 → 盐 + 水
(5)酸 + 碱 → 盐 + 水(复分解反应)
(6)酸 + 盐 → 另一种酸 + 另一种盐(复分解反应)
(7)碱 + 盐 →另一种碱 + 另一种盐(复分解反应)
参加反应的碱和盐必须都能溶于水,生成物中有一种是难溶性的碱(或氨气)或盐
(8)盐 + 盐→两种新盐(复分解反应)
参加反应的两种盐必须都能溶于水,生成物中有一种是难溶性的盐。
溶液酸碱性与pH:溶液有酸碱性,可以用酸碱指示剂、pH试纸检验溶液的酸碱性,酸碱性对人体健康和农作物生长有重要影响。
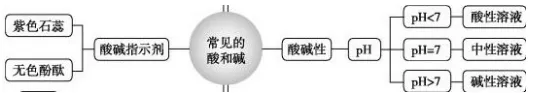
核心知识:

常见酸的性质及应用:
①与指示剂作用:酸能使石蕊溶液变红,不能使酚酞溶液变色生活应用:辨别变质食品、检测水质酸碱性。
②与活泼金属反应:酸+活泼金属→盐+氢气生活应用:不能用铁桶盛放食醋,铁会和醋酸反应被腐蚀;实验室制氢气用锌和稀硫酸,不用铁/铝,反应速率不合适。
③与金属氧化物反应:酸+金属氧化物→盐+水生活应用:除铁锈神器!生锈的铁钉泡在食醋里,铁锈慢慢消失;家里水壶的水垢(主要成分碳酸钙),用白醋浸泡就能轻松去除,比钢丝球擦更省力。
④与碱反应:酸+碱→盐+水生活应用:用氢氧化铝治疗胃酸过多,蚊虫叮咬涂抹肥皂水;用熟石灰改良酸性土壤;处理工厂废水。
⑤与盐反应:
酸+盐→新酸+新盐 ,以碳酸盐为例:酸+碳酸盐→盐+水+二氧化碳生活应用:小苏打+白醋能疏通下水道、清洁油污;蒸馒头放小苏打,遇面粉里的酸产生二氧化碳,馒头变得松软多孔。
①与指示剂作用:碱能使石蕊溶液变蓝,能使酚酞溶液变红
生活应用:检测水质酸碱性
常见盐的性质及应用:
1. 盐+金属→新盐+新金属(金属活动性顺序应用,前置后,盐可溶)2. 盐+酸→新盐+新酸3. 盐+碱→新盐+新碱(反应物都可溶,生成物有沉淀)4. 盐+盐→两种新盐(反应物都可溶,生成物有沉淀)生活应用:用食盐腌制食物,抑制细菌生长,延长保质期;纯碱能去除油污,厨房清洁超好用;碳酸钙是钙片和大理石的主要成分,补钙、建筑两不误。
物质鉴别和检验:根据物质的某一特性,用化学方法来确定物质的组成。
1.用酸碱指示剂进行鉴别溶液的酸碱性。
例:如何鉴别氢氧化钠溶液、稀盐酸、氯化钠溶液。
解:取样分别加入三支试管,分别滴加等量紫色石蕊溶液,变红的是稀盐酸、变蓝的为氢氧化钠溶液、还是紫色的是氯化钠溶液。常见指示剂:紫色石蕊溶液、酚酞溶液
常见碱性溶液:碱溶液、碳酸钠溶液、草木灰(主要成分K2CO3)溶液、碳酸氢钠溶液。
常见酸性溶液:稀盐酸、稀硫酸、硫酸铜溶液、硫酸氢钠溶液。
除杂:
主要物质(杂质) | 试剂名称 | 化学方程式 |
Cu(Fe) | 过量稀盐酸 | Fe+2HCl===FeCl2+H2↑ |
FeCl2(CuCl2) | 足量铁粉 | Fe+CuCl2===FeCl2+Cu |
主要物质(杂质) | 试剂名称 | 化学方程式 |
NaCl溶液 (Na2SO4) | 适量BaCl2 | Na2SO4+BaCl2===BaSO4↓+2NaCl |
NaOH溶液 (Na2CO3) | 适量 Ca(OH)2 | Na2CO3+Ca(OH)2===CaCO3↓+2NaOH |
CaCl2溶液 (HCl) | 适量 Ca(OH)2 | 2HCl+Ca(OH)2===CaCl2+2H2O |
NaCl溶液 (Na2CO3) | 适量 稀盐酸 | Na2CO3+2HCl===2NaCl+H2O+CO2↑ |
注意:①找到杂质与主要物质结构上的不同,选取试剂与杂质发生复分解反应。
②杂质离子转化为沉淀、气体或水除去,保留离子生成溶液的主要成分。此方法会使主要成分的质量增大。
不能共存的离子:
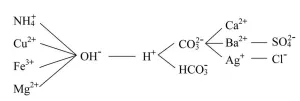
典型考题(转载)
1.生活中处处有化学,在家就可以体验化学的魅力。
(1)制碱:将蛋壳(主要成分为CaCO3)灼烧成灰,加水,搅拌,静置,(填操作名称),得到碱溶液A,灼烧时CaCO3发生反应的化学方程式是。
(2)制酸碱指示剂:将紫薯切碎泡水,获得的紫色溶液可做酸碱指示剂。分别向食醋、碱溶液A、苏打溶液中加入该指示剂,溶液颜色依次为红色、绿色、绿色,据此推测,苏打溶液的pH(填“>”或“<”)7。
(3)除锈:①将两根生锈的铁钉分别放入盛有洁厕灵(有效成分为盐酸)、食醋的塑料杯中,均能观察到铁锈溶解。从微观角度解释两者均可以除铁锈的原因是。
②一段时间后,两个塑料杯中都有气泡产生。用化学方程式解释盛有洁厕灵的杯中产生气泡的原因:。
【答案】(1)过滤 (2)> (3)盐酸、食醋中都含有H+,能与铁锈(主要成分Fe2O3)反应 Fe+2HCl=FeCl2+H2↑
2.生活中的酸和碱无处不在。
(1)在日常生活中,下列物质呈碱性的是______。
A.白醋(pH约为2~3) B.橘子汁(pH约为3~4)
C.番茄汁(pH约为4~5)D.炉具清洁剂(pH约为12~13)
(2)下列物质的名称或俗称与化学式均正确的是______。
A.胆矾CuSO4B.生石灰CaOHC.氯化氨NH4ClD.烧碱NaOH
(3)下列说法正确的是______。
A.pH<7的雨水叫酸雨 B.碱中一定含有氢元素和氧元素
C.碱中一定含有金属元素 D.氢氧化钠用于改良酸性土壤
(4)柑橘类水果中柠檬酸含量较高,其化学式是C6H8O7,是否属于氧化物(选填“是”或“否”),其中C、H、O三种原子的个数比为,氧元素的质量分数为(列式即可)。氧原子的原子结构示意图为,反应中易(选“得到”或“失去)电子,氧离子的化学符号为。
(5)盐酸是某种除锈剂的主要成分,请写出其与铁锈(主要成分为氧化铁)反应的化学方程式,现象是。某同学将除锈剂稀释后,放入一枚生锈的铁钉,片刻后铁锈脱落,铁钉表面产生气泡,产生气泡的原因是 (用化学方程式表示),基本反应类型是。
(5)Fe2O3+6HCl=2FeCl3+3H2O 铁锈逐渐消失,溶液由无色变为黄色 Fe+2HCl=FeCl2+H2↑ 置换反应
3.(2025福建中考)研究性学习小组开展“自制酸碱指示剂”实践活动。
【活动1】将紫甘蓝叶研碎后加入适量酒精浸泡一段时间,用纱布将浸泡出的汁液挤出,得到紫甘蓝液。
【活动2】探究紫甘蓝液在不同酸碱性溶液中的颜色变化,结果如下表所示。
pH | 1~2 | 3~6 | 7~9 | 10~11 | 12~14 |
颜色 | 红 | 紫 | 蓝 | 绿 | 黄 |
请回答下列问题:
(1)将紫甘蓝叶研碎的目的是。
(2)“用纱布将浸泡出的汁液挤出”相当于(填实验操作名称)。
(3)若往1mL pH=13的氢氧化钠溶液中滴加1~2滴紫甘蓝液,溶液呈色;继续滴加稀盐酸至溶液呈绿色,氢氧化钠和稀盐酸反应的化学方程式为,此时酸、碱是否恰好完全反应?答:(填“是”或“否”)。
4.(2025福建中考)博物院油画馆的讲解员告知同学们,油画若保存不当,其中的红铅颜料在空气中会缓慢变成白色。为探究红铅(Pb3O4)的变色原因,研究性学习小组开展实践活动。
【查阅资料】①Pb3O4是难溶于水的红色固体,暴露在空气中可转化为PbCO3、Pb(OH)2中的一种或两种;②PbCO3、Pb(OH)2均为难溶于水的白色固体,均能与稀硝酸(HNO3)发生复分解反应。
【活动1】探究红铅变色与光照强度的关系
在3支洁净试管中分别加入Pb3O4粉末,控制单一变量进行实验(如下表所示)。
试管编号 | I | II | III |
光照强度 | 弱 | 较强 | 强 |
实验现象 | 无明显变化 | 红色粉末少量变白 | 红色粉末变白 |
(1)实验过程中,试管应保持敞口状态的理由是。
(2)该实验可以得出的结论是。
(3)一定条件下,Pb3O4分解有O2产生。检验O2的方法是。
【活动2】探究白色固体的组成
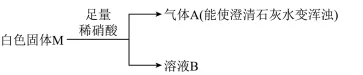
(4)由白色固体M生成气体A的化学方程式为。
(5)依据上述实验的现象,无法确定白色固体M中是否还含有Pb(OH)2,其理由是。
(6)将溶液B中的铅元素完全转化为PbCO3沉淀,并依据PbCO3沉淀的质量(x)和白色固体M的质量(y)的关系,可以确定白色固体M是否含有Pb(OH)2.若含有Pb(OH)2,则xy(填“>”“<”或“=”)。
(7)基于上述探究,为了更好地保护油画,请你为参观人员提出一条合理的建议:。
【答案】(1)与红铅颜料暴露在空气中的环境一致(2)光照越强,Pb3O4变色越快
(3)用带火星的木条检验(4)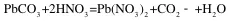
(5)无论是否含有Pb(OH)2,实验的现象都相同
(6)>(7)禁止开闪光灯拍照

酸碱盐是大家庭,本质上是离子对,
氢离子遇氢氧根,中和反应生成水,
碳酸根遇氢离子,二氧化碳来冒泡,
复分解离子结合,气体沉淀水来生,
物质分类找规律,酸碱盐尽在心中。






