高中自主招生考试化学试题
本试卷分第I卷和第II卷两部分,共6页。满分50分,考试时间30分钟。答题前,考生务必用0.5毫米黑色签字笔将自己的姓名、考号、毕业学校、考场等信息填涂在答题卡规定的位置。考试结束后,将试卷和答题卡一并交回。
第I卷(共15分)
注意事项:
1、第I卷共15小题,每小题1分,共15分。
2、每小题选出答案后,用 2B铅笔把答题卡上对应题目的答案标号涂黑,如需改动,用橡皮擦干净后,再选涂其他答案标号。不涂在答题卡上,只答在试卷上不得分。
相对原子质量:H 1 C 12 N 14 O 16 Na 23 Mg 24 Al 27 S 32 Cl 35.5 Fe 56Cu 64Ag 108
一、选择题(本题包括15小题,每小题1分,共15分。每小题只有一个选项符合题意。)
1、化学让生活更美好。下列有关说法中合理的是
A. 食盐是由钠原子和氯原子直接组成的
B. 95%的酒精一定比75%的酒精消毒效果更好
C. 模拟“侯氏制碱法”的实验中,应向饱和氯化钠溶液中依次通入CO2、NH3
D.“百炼成钢”是指通过反复锤炼,除去铁中部分杂质,使其转化为钢
2、化学概念存在如下图关系,下列对概念间相互关系的说法中正确的是
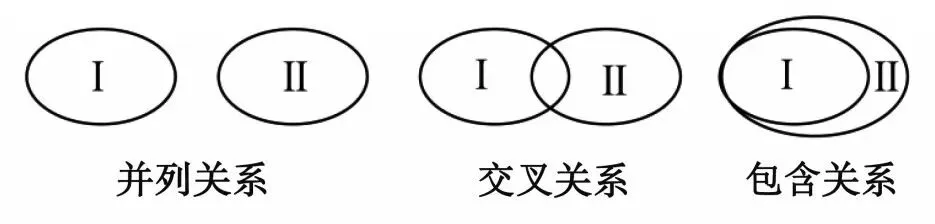
A. 糖类与纤维素属于并列关系B. 合成材料与塑料属于包含关系
C. 化合物与纯净物属于交叉关系D. 中和反应与复分解反应属于并列关系
3、某元素的气态氢化物化学式为H2R,此元素最高价氧化物对应水化物的化学式可能为
A. H2RO4B. HRO3C. H2RO3D. H3RO4
4、已知金属硫化物的溶解性比较复杂,如K2S、Na2S为可溶性硫化物,FeS、ZnS为难溶于水的硫化物,CuS、Ag2S为既难溶于水又难溶于强酸的硫化物。下列硫化物和酸的反应不正确的是
A. Na2S+2HCl=H2S↑+2NaClB. FeSO4+H2S=FeS↓+H2SO4
C. CuSO4+H2S=CuS↓+H2SO4D. ZnS+2HCl=H2S↑+ZnCl2
5、原子的质量主要由原子核决定。已知质量数为A的某阳离子Rn+,核外有X个电子,则核内中子数为
A. A-X+nB. A-XC. A+X-nD. A-X-n
6、如图是甲转化为丙的微观过程。下列说法不正确的是
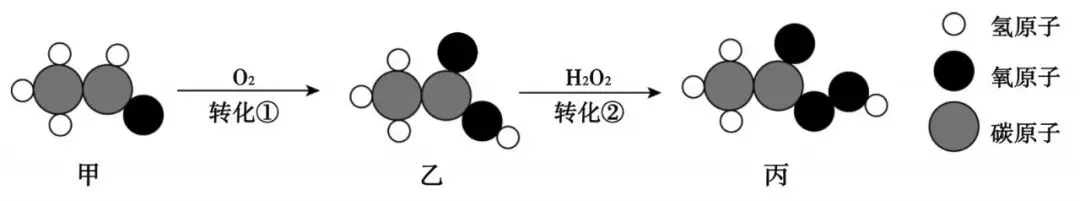
A. 甲、乙、丙完全燃烧的产物相同B. 转化①中甲和O2的分子数之比为2:1
C. 整个转化过程原子利用率为100%D. 甲、乙、丙中碳元素的质量分数依次降低
7、单晶硅是制作电子集成电路的基础材料高温,工业上通过以下反应将自然界中的二氧化硅(SiO2)转化成硅(Si):SiO2+2C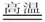 Si+2C0↑,下列分析正确的是
Si+2C0↑,下列分析正确的是
A. 碳表现出了还原性B. 碳表现出了氧化性
C. 二氧化硅发生了氧化反应D. 该反应是分解反应
8、已知1.42gR元素可与氧元素组成2.38g氧化物X,也可以与氧元素组成3.66g氧化物Y。则X、Y的化学式可能为
A. R2O3和R2O7B. R2O3和R2O5C. R2O和R2O4D. R2O和R2O3
9、原煤(含硫元素)在氧气中不完全燃烧会生成CO、CO2和SO2。若测得CO、CO2和SO2的混合气体中碳元素的质量分数为12%,则其中SO2的质量分数可能是
A. 40%B. 60%C. 72%D. 80%
10、有一包粉末,已知由CaCO3、FeCl3、MgCl2、Na2SO4、NaOH、NaNO3中的2种或2种以上物质组成。为了确定其成分,现进行以下实验(假设各步反应已充分):
①取一定质量的粉末,加水搅拌后过滤,得到沉淀甲和无色溶液A;
②向①的沉淀甲中加入足量稀盐酸,得到无色气体和黄色溶液;
③将①得到的无色溶液A进行如图所示的实验。
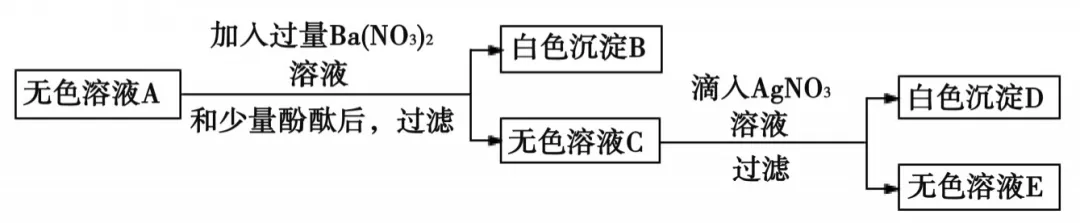
下列说法不正确的是:
A. 沉淀甲一定含有CaCO3、Fe(OH)3
B. 这包粉末中可能含有的物质是MgCl2、NaNO3
C. 无色溶液A中一定存在的溶质是Na2SO4、NaCl
D. 这包粉末中一定含有的物质是CaCO3、FeCl3、MgCl2、Na2SO4、NaOH
11、下列各组物质的溶液不用其他试剂无法鉴别的是
A. HClNaOHCuSO4MgSO4B. Na2CO3K2SO4BaCl2HCl
C. NaNO3HClCaCl2KOHD. H2SO4NaClNa2CO3CaCl2
12、向 100g NaOH 溶液中通入 CO2得到溶液 X,向溶液 X 中逐滴滴加 3.65% 的盐酸,产生CO2的质量与加入盐酸质量的关系如图(已知:Na2CO3+HCl=NaHCO3+NaCl,NaHCO3+HCl=NaCl+CO2↑+H2O)。下列说法不正确的是
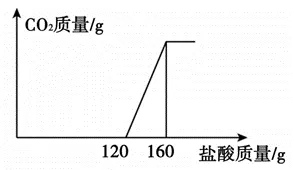
A. 通入CO2的质量为1.76gB. 溶液X中含有NaOH和Na2CO3
C. NaOH溶液的溶质质量分数为6.4%D. 加盐酸至120g时溶液中的溶质只有NaHCO3
13、已知金属阳离子氧化性(得电子能力):Fe3+>Cu2+>Fe2+>Zn2+,在溶有 Fe2(SO4)3和CuSO4的溶液中加入锌粉,下列说法中不正确的是
A. 若锌粉有剩余,则溶液中的金属阳离子只有Zn2+
B. 若锌粉有剩余,则不溶物中一定有铜和铁
C. 若固体仅有铜单质,则溶液中一定有Fe2+、Zn2+,可能有Cu2+、Fe3+
D. 若固体有铁单质,则溶液中一定无Fe3+、Cu2+,一定有Zn2+,但不能确定有无Fe2+
14、工业上常用空气中的氮气生产硝酸,其反应方程式如下:
①N2+3H2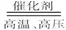 2NH3②4NH3+5O2
2NH3②4NH3+5O2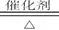 4NO+6H2O
4NO+6H2O
③2NO+O2 =2NO2④3NO2+H2O=2HNO3+NO(NO难溶于水)
下列说法错误的是
A. 工业上,30Kg NO生产得到42Kg HNO3
B. 用H2O吸收NO2的过程中通入过量的O2可以提高硝酸的产量
C. 上述①②③④中反应前后均有元素化合价的变化
D. 反应②④都不属于四种基本反应类型中的任何一种,反应①③均属于化合反应
15、下图为某科研机构研究利用铁的氧化物循环裂解水蒸气制氢气的过程示意图。下列关于该过程的说法正确的是
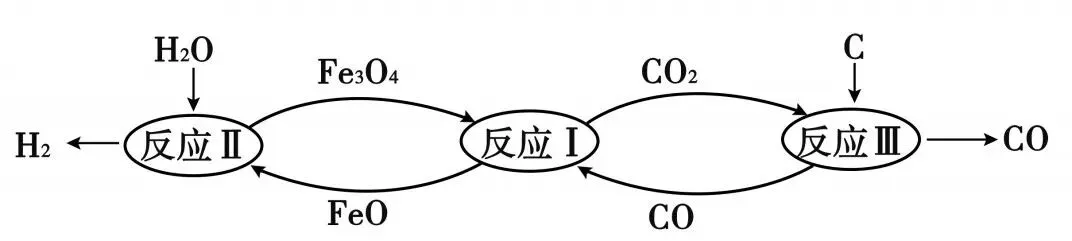
A. 反应过程中需不断添加 Fe3O4和 FeO
B. 理论上,反应II中每加入 18g水蒸气,会有 72g FeO参加反应
C. 反应过程中元素化合价发生改变的元素 Fe、C、H
D. 整个过程的总反应方程式可以表示为:2H2O(气) 2H2+ O2
2H2+ O2
第II卷(共35分)
注意事项:
1、第II卷共5小题,共35分。
2、考生用0.5毫米黑色签字笔将答案和计算步骤、过程填写在答题卡相应位置,直接在试卷上作答的不得分
二、填空题(本题包括3小题,共21分)
16、(9分)金属材料在生产生活中有着广泛应用。
⑴锂是一种银白色的金属元素,质软,容易受到氧化而变暗,是所有金属元素中最轻的。用途很广泛,涉及电池、陶瓷、玻璃、润滑剂、制冷液、核工业以及光电等领域。锂辉石的化学组成为 LiAlSi2O6,是主要含锂矿石之一,LiAlSi2O6也可表示为Li2O·Al2O3·xSiO2氧化物的形式,其中x=。
⑵从化合价和物质类别两个维度认识元素及其化合物性质是重要的化学学习方式。下图是Fe及其化合物的化合价——物质类别二维图。请回答下列问题:
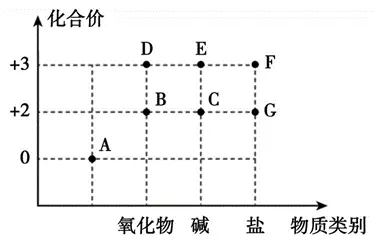
① D 的化学式是。
② C 在潮湿的空气中很容易发生化合反应变成E, 该反应的化学方程式是。
③ CO 和 CO2 可以通过化合反应相互转化,根据 CO 和 CO2 之间的这种转化规律,试写出 G 和 F 的氯化物之间相互转化的化学方程式(不写条件):;。
⑶在 5.6g 铁粉中,先逐滴加入一定量的 Cu(NO3)2 溶液,充分反应后再逐滴加入 AgNO3溶液,剩余固体质量与所加溶液总质量的关系如下图所示。下列说法正确的是
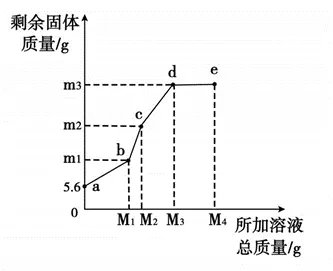
A. m3的值为10.8B. e点溶液中不含Cu(NO3)2
C. bc段发生的是Cu和AgNO3溶液的反应D. 当所加溶液质量为M1 g时,铁粉有剩余
17、(7分)化学源于生活,生活中蕴含化学。用所学化学知识解答相关问题
⑴已知氢氧化铝[Al(OH)3]是既可与强酸(如盐酸HCl),又可与强碱(如氢氧化钠NaOH)反应,且难溶于水白色沉淀,又已知:Al(OH)3+NaOH=NaAlO2+2H2O,其中NaAlO2叫偏铝酸钠,是一种溶于水的盐。向含有26.7g AlCl3的溶液中逐滴加入NaOH溶液至过量,观察到的现象为,反应一段时间后,当偏铝酸钠中的铝元素和沉淀中的铝元素质量相等时,则参加反应的NaOH的质量是g。
⑵某化工厂甲、乙两车间排放的甲、乙两溶液中,共含有Ba(NO3)2、Fe(NO3)3、CuSO4、KOH、K2SO4 五种溶质。当将甲、乙两溶液按适当质量比充分混合,经沉淀、过滤,滤液中只有一种钾盐。若甲溶液中只含有两种溶质,则乙溶液中含有的三种溶质的化学式为;甲、乙两溶液反应后滤液中溶质的化学式为。
⑶某无色、澄清溶液中可能含有Na+、SO42-、Cl-、HCO3-、CO32-、H+、Cu2+中的若干种。依次进行下列实验,且每步所加试剂均过量,观察到的现象如下:
步骤① 向溶液中滴加2~3滴紫色石蕊溶液,溶液变红;
步骤② 向溶液中滴加BaCl2和稀HCl,有白色沉淀;
步骤③ 将②中所得混合物过滤,向滤液中加入AgNO3溶液和稀HNO3,有白色沉淀生成。
则:该溶液中一定含有 (写离子符号,下同);一定不含有;若该溶液中每种离子个数相等,则该溶液中一定含有___________。
18、(5分)已知A、B、C、D、E是初中化学常见的五种不同物质,它们之间的关系如下图所示,图中“—”表示相连的两种物质能发生化学反应,“→”表示一种物质能转化为另一种物质,部分反应物、生成物及反应条件已略去。B、C、D、E是四种不同类别的化合物,A与B反应常用来检验铵态氮肥,B常用于改良酸性土壤,A、E含有相同的阴离子,且E中只含有两种元素。请回答下列问题:
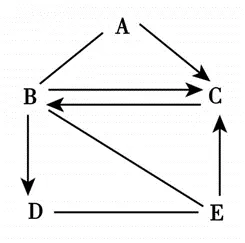
⑴B→D反应的现象为。⑵A—B反应的化学方程式为。
⑶C→B反应的化学方程式为。
三、实验题(本题包括1小题,共8分)
19、(8分)氢气在常温下化学性质稳定,但是它具有较强的可燃性、还原性。在点燃或加热的条件下,氢气很容易和多种物质发生化学反应,如将氢气通过灼热的氧化铜、氧化铁等金属氧化物,氢气可以夺取金属氧化物中的氧,同时生成了水和其他物质。根据题意完成下列问题:
【已知信息】Ⅰ. Cu和Cu2O均为不溶于水的红色固体;
Ⅱ. Cu2O与H2SO4能发生化学反应,有金属单质和硫酸盐等生成。
某化学课外兴趣小组的同学探究氢气还原氧化铜得到的红色固体的成分时,进行了以下探究过程。
【猜想假设】氢气还原氧化铜得到的红色固体含有什么物质?假设一:红色固体只含有Cu;假设二:红色固体只含Cu2O;假设三:(请补充完成假设三)。
【初步探究】
实验操作 | 实验现象 | 实验结论 |
a. 取少量红色固体加入到足量硫酸溶液中 | 无明显现象 | 假设 ① 成立 |
b. 取少量红色固体加入到足量硫酸溶液中充分反应 | ② | 假设二和假设三均可能成立 |
【继续探究】
⑴若要确认假设二和假设三究竟是谁成立,同学称取 Wg红色固体加入到足量硫酸溶液中使其充分反应后,过滤、洗涤、干燥,称量剩余红色固体质量为mg,若m g(选填>、<或=,下同),则假设二成立;若m
g(选填>、<或=,下同),则假设二成立;若m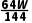 g,则假设三成立。
g,则假设三成立。
⑵写出Cu2O与H2SO4发生反应的化学方程式:。
四、计算题(本题包括1小题,共6分)
20、(6分)某有机化合物含有碳、氢、氧三种元素,其相对分子质量为32。取该有机物6.4 克,将其充分燃烧后的产物通入足量的石灰水被完全吸收,经过滤,得到20克沉淀物,滤液的质量比原石灰水减少了4克。求:
⑴原6.4克有机物中所含氧元素的质量为g;
⑵通过计算确定该有机物的化学式(写出计算过程)。






