2026年04月04日
上海初中化学中考趋势 | 2026年04月04日
今日主题
喀斯特地貌溶洞形成的化学探究与定量分析 · 地质小组探究喀斯特溶洞的形成,采集100g洞穴渗漏水(主要溶质为碳酸氢钙)。为测定浓度,将其持续加热至无气泡产生,发生反应:Ca(HCO₃)2=CaCO₃↓+H₂O+CO₂↑。测得生成白色沉淀1.0g。冷却过滤后,向滤液滴加肥皂水振荡,产生大量泡沫。此过程模拟了钟乳石的形成并实现了硬水软化。
核心知识点
• 碳酸盐与碳酸氢盐的转化
• 硬水与软水的检验
• 基于化学方程式的质量分数计算
教育价值
通过喀斯特地貌这一真实自然现象,引导学生理解宏观地质演变背后的微观化学原理。将硬水软化、物质检验与定量计算相融合,培养学生在复杂真实情境中提取有效信息、运用物质转化观和守恒观解决综合问题的科学素养。
情景化题型精讲
题目配图
图1:science 化学 20260404 1
【计算综合题】(挑战程度,总分14分)
我国西南地区广泛分布着壮丽的喀斯特地貌,其典型特征之一是千姿百态的溶洞与钟乳石。某地质兴趣小组为探究溶洞的形成原理及洞穴水质,前往当地地质公园考察后,为便于定量探究,在实验室配制了 100 g 模拟洞穴渗漏水(主要溶质为碳酸氢钙,并含有少量不参与反应的可溶性钠盐杂质)进行实验。
查阅资料可知,地表水吸收空气及土壤中的二氧化碳后,流经石灰岩(主要成分为碳酸钙)时发生化学反应,形成的碳酸氢钙易溶于水,随水渗入地下。当渗漏水滴入溶洞时,由于内部温度、压强等条件的变化,碳酸氢钙会发生分解,沉积成钟乳石或石笋。
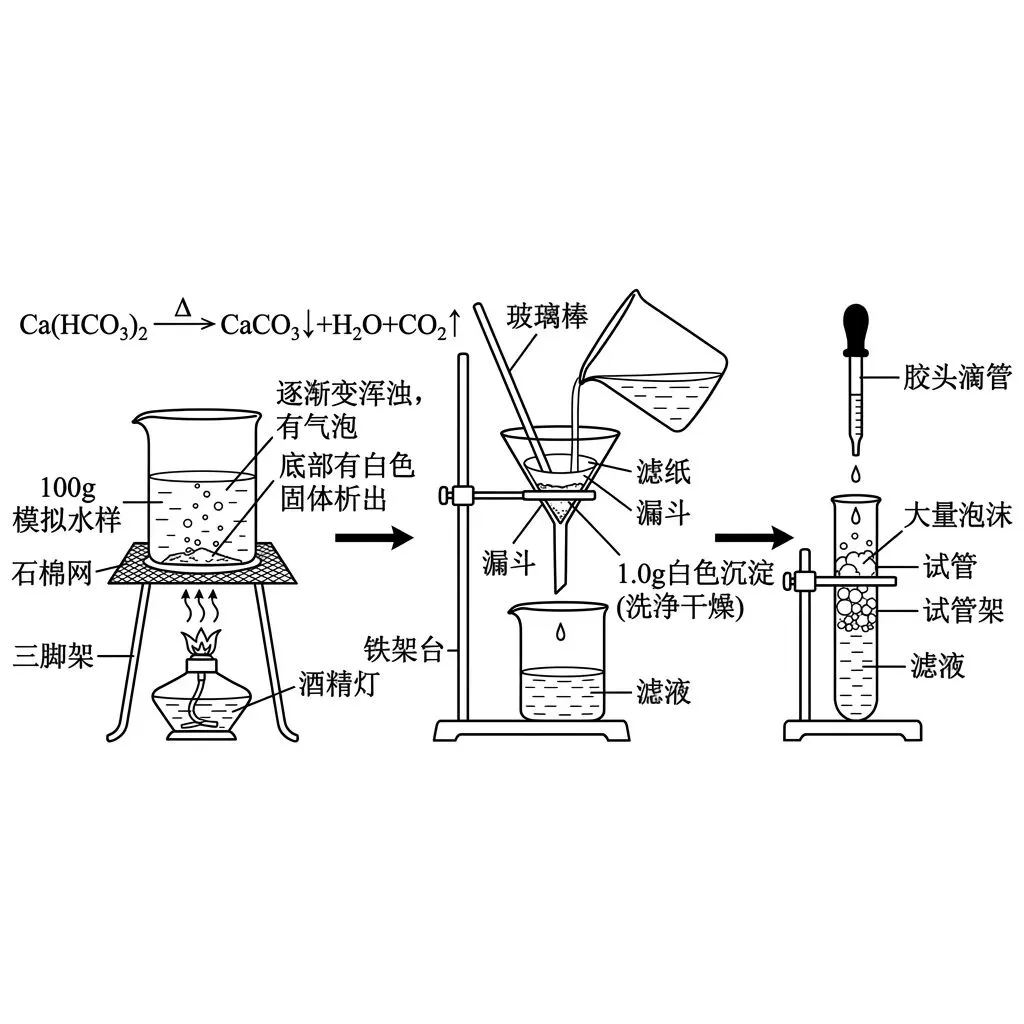
为测定该模拟水样中碳酸氢钙的质量分数,并模拟自然界钟乳石的形成过程,小组同学设计了如下实验探究(实验流程见图1):
步骤一:准确称取配制的 100 g 模拟水样于烧杯中,持续加热。观察到水中不断有气泡冒出,液体逐渐变浑浊,底部有白色固体析出。该过程发生的化学反应为:Ca(HCO₃)₂ Δ CaCO₃↓ + H₂O + CO₂↑。
步骤二:待无气泡产生且反应完全后,将烧杯中的混合物冷却至室温,进行过滤。对滤渣进行充分洗涤、干燥后,准确称得生成的白色沉淀质量为 1.0 g。
步骤三:取步骤二中得到的少量滤液于试管中,滴加适量肥皂水,振荡,观察到产生大量泡沫,几乎无浮渣。
通过上述探究,小组同学不仅定量测定了模拟水样的溶质含量,还成功实现了硬水的软化。

(1)步骤二中将固体与液体分离的操作名称是______;步骤三中“产生大量泡沫”的现象说明经过加热处理后的滤液属于______(填“硬水”或“软水”)。结合情境信息,写出自然界中溶洞形成初期,石灰岩被地表水溶解的化学方程式:______。(5分)
参考答案:
过滤;软水;CaCO₃ + H₂O + CO₂ = Ca(HCO₃)₂
解析:
解析:分离难溶性固体和液体的基本实验操作是过滤;向水样中加入肥皂水振荡,产生大量泡沫、无浮渣是软水的典型特征,说明加热使水中的钙离子转化为沉淀从而降低了水的硬度;根据情境背景中“地表水吸收空气及土壤中的二氧化碳后,流经石灰岩(主要成分为碳酸钙)时发生化学反应,形成的碳酸氢钙”这一信息,可推导出反应物为 CaCO₃、H₂O 和 CO₂,生成物为 Ca(HCO₃)₂。
(2)根据实验测得的数据,请综合分析并计算该模拟洞穴渗漏水中碳酸氢钙的质量分数。(写出完整的计算过程)(5分)
参考答案:
1. 62%
解析:
解析:
设 100 g 模拟水样中含有碳酸氢钙的质量为 x。
Ca(HCO₃)₂ Δ CaCO₃↓ + H₂O + CO₂↑
162 100
x 1.0 g
(162)/(100) = (x)/(1.0 g)
解得 x = 1.62 g
模拟水样中碳酸氢钙的质量分数为:(1.62 g)/(100 g) × 100% = 1.62%
答:该模拟洞穴渗漏水中碳酸氢钙的质量分数为 1.62%。
(3)自然状态下洞穴渗漏水中的碳酸氢钙分解极其缓慢。为在实验室中加快模拟“钟乳石”的形成(即加快碳酸钙沉淀的析出),除情境中采用的“加热”法外,请基于化学反应原理,提出一种不同的改进方案(可添加试剂或改变物理条件),并简述其科学道理。此外,若步骤二中未对滤渣进行“洗涤”直接干燥称重,会导致测得的碳酸氢钙质量分数偏大还是偏小?请说明理由。(4分,答案不唯一,言之有理即可)
参考答案:
改进方案参考:加入适量澄清石灰水(或氢氧化钙溶液),氢氧化钙能与碳酸氢钙发生反应生成碳酸钙沉淀和水。误差分析:偏大。若不洗涤滤渣,沉淀表面会附着残留的钠盐等可溶性杂质,导致称得的固体质量大于实际生成的碳酸钙质量,代入化学方程式计算出的碳酸氢钙质量随之偏大。
解析:
解析:第一问考察物质转化规律与方案设计能力。从化学试剂角度,加入碱类(如 Ca(OH)₂)可发生反应生成碳酸钙沉淀。第二问考察实验误差分析,未洗涤的沉淀表面会附着母液中的可溶性钠盐杂质,导致 m(CaCO₃) 测量值偏大,根据正比例关系,计算出的反应物质量及质量分数必然偏大。
知识点地图
喀斯特地貌成因(碳酸盐与碳酸氢盐转化) → 硬水软化与检验 → 基于化学方程式的质量分数计算 → 实验误差分析与方案设计
本题知识点之间的逻辑关联,帮助学生建立知识网络
思路拓展
1. 拓展问题1:如果将步骤一中的持续加热改为向水样中滴加足量稀盐酸,能否达到测定碳酸氢钙质量分数的目的?为什么?
2. 拓展问题2:地球气温的整体升高对全球喀斯特地貌溶洞中钟乳石的生长速度可能会产生怎样的影响?请结合本题中的化学反应尝试解释。
拓展问题不要求作答,目的是打开思路,培养发散思维
学习建议
1. 建议梳理碳酸钙与碳酸氢钙的相互转化网络。具体行动:在笔记本上画出“CaCO₃ - CO₂ - Ca(HCO₃)₂”的循环转化图,并写出对应的化学方程式:CaCO₃ + H₂O + CO₂ = Ca(HCO₃)₂ 和 Ca(HCO₃)₂ = CaCO₃↓ + H₂O + CO₂↑。结合溶洞形成(溶蚀和沉积)的自然现象,理解自然界中的碳循环,这有助于应对中考常考的物质推断与转化题。
2. 建议规范化学方程式计算的书写步骤,特别是质量关系的对应。具体行动:针对情景中的定量分析,练习已知沉淀质量求原溶液溶质质量分数的计算。列出已知量 m(CaCO₃) = 1.0 g,通过方程式 Ca(HCO₃)₂ = CaCO₃↓ + H₂O + CO₂↑ 计算出 m(Ca(HCO₃)₂),再除以溶液总质量 100 g 得到质量分数。注意计算过程中物理量符号要规范写为 m(物质),养成“列、设、写、找、解、答”的规范习惯。
3. 建议通过对比实验深化对硬水软化及检验的理解。具体行动:在家中取两只透明水杯,分别装入等量的自来水(硬水)和凉开水(软化水),滴加等量肥皂水振荡,观察泡沫和浮渣的差异。结合情景理解加热煮沸能将可溶的 Ca(HCO₃)₂ 转化为不溶的 CaCO₃↓ 从而降低水硬度,将试卷上的理论知识转化为生活常识。
4. 建议在复习中注重实验误差分析与探究思维的训练。具体行动:在分析“持续加热至无气泡产生”这一操作时,主动思考“若加热不彻底”或“过滤有损失”对结果的影响。如果在实际操作中测得的 m(CaCO₃) 小于理论值,尝试从反应物未完全分解、转移过程损耗等角度列出误差原因。这种逆向推导的思维方式,是解答中考化学实验探究题压轴部分的关键。
中考趋势分析
近期上海初中化学中考呈现以下趋势:
• 题目形式的变化:近年来上海中考化学在考查此类地质与环境主题时,逐渐减少单一知识点的选择题,转向将填空题、实验探究题与定量计算题相融合的综合大题。例如,将Ca(HCO₃)₂的受热分解现象与硬水软化检验结合在同一道实验探究题中,并附带基于生成1.0g CaCO₃沉淀的化学方程式计算。
• 知识考查的深度和广度:考查范围从基础的物质性质向物质转化规律拓展。不仅要求学生掌握硬水与软水的检验方法(滴加肥皂水),还要求深刻理解碳酸盐与碳酸氢盐的相互转化,如Ca(HCO₃)₂ = CaCO₃↓ + H₂O + CO₂↑,并能将此微观化学反应与宏观的钟乳石形成、硬水软化等自然与生活现象建立联系。
• 情景化、应用性题目的特点:命题高度贴近真实生活与跨学科实践。以地质小组采集100g洞穴渗漏水为背景,打破了传统纯文字或纯符号的枯燥设问。题目通过模拟钟乳石形成和硬水软化的真实操作流程,考查学生在复杂、陌生的真实情境中提取有效化学信息(如主要溶质为碳酸氢钙)并解决实际问题的能力。
• 对学生能力要求的变化:对学生的综合科学素养提出了更高要求。学生不仅需要具备扎实的实验基础(如冷却过滤操作、沉淀与气泡观察),还需具备较强的数据处理与定量分析能力。例如,能根据化学方程式和已知沉淀质量m(CaCO₃) = 1.0 g,计算出原100g渗漏水中Ca(HCO₃)₂的质量分数,体现了从定性探究到定量计算的思维跨越。
• 备考建议和重点:备考时应重点关注碳及其化合物的转化网络,特别是CO₂、CaCO₃与Ca(HCO₃)₂之间的相互转化关系。建议加强跨学科情境阅读训练,学会在大段背景文字中剥离出核心化学反应。同时,需规范化学方程式书写与定量计算步骤,熟练掌握利用已知生成物质量求解反应物质量的方法,并重视硬水软化等生活化实验的原理与操作细节。
实际应用
地下水及自来水水质检测、工业锅炉防垢除垢处理、地质勘探中的水文与岩石成分鉴定。
每日一题,助力中考
科学备考,稳步提升
更新时间: 2026-04-04 10:19:14
内容说明: 本栏目专注上海初中化学中考趋势分析,每日精选情景化题型,帮助学生掌握核心知识点和解题方法。
— 每日中考英语 · 自动推送 —






