


题型七 化学计算题
类型1 文字叙述型
1. [2025·威海中考]
利用电解饱和食盐水的方法制得的氢氧化钠样品中含有一定量的氯化钠。要测定其中氢氧化钠的质量分数,进行如下实验:取5 g样品,加水使其完全溶解,再向其中滴加氯化镁溶液至不再产生沉淀,经过滤、洗涤、干燥后,称得沉淀的质量为2.9 g,试计算该样品中氢氧化钠的质量分数。
2. [2025·陕西中考]
某水垢样品的主要成分是\ce{CaCO_{3}}和\ce{Mg(OH)_{2}}。学习小组同学想测定该水垢样品中\ce{CaCO_{3}}的质量分数,于是向盛有25 g水垢样品的烧杯中加入100 g足量稀盐酸,发生的反应是:\ce{CaCO_{3} + 2HCl = CaCl_{2} + H_{2}O + CO_{2}↑},\ce{Mg(OH)_{2} + 2HCl = MgCl_{2} + 2H_{2}O},待反应完全后,经称量烧杯内物质总质量为116.2 g(注意:忽略\ce{CO_{2}}在水中的溶解)。请完成下列分析及计算。
(1) 实验过程中生成气体的质量是______g。
(2) 计算该水垢样品中\ce{CaCO_{3}}的质量分数。(写出计算过程)
3. [2025·重庆中考]
实验小组利用甲烷、氧气和氢氧化钠溶液组成的燃料电池进行模拟实验。一定条件下发生反应的化学方程式为\ce{CH_{4} + 2O_{2} + 2NaOH\xlongequal{一定条件}Na_{2}CO_{3} + 3H_{2}O},理论上若所有反应物刚好完全反应,恰好消耗100 g 4%的\ce{NaOH}溶液。试计算:
(1)\ce{Na_{2}CO_{3}}中碳元素与氧元素的质量比为______。
(2) 所得溶液中溶质的质量分数。(写出计算过程,结果精确到0.1%)
类型2 坐标曲线型
4. [2025·潍坊中考]
某融雪剂的主要成分为\ce{NaCl},还含有少量的\ce{CaCl_{2}}。为测定该融雪剂中\ce{NaCl}的质量分数,化学兴趣小组进行以下实验:取40.0 g融雪剂样品于烧杯中,加入160.0 g蒸馏水使固体完全溶解;取100.0 g所得溶液,逐滴加入一定溶质质量分数的\ce{Na_{2}CO_{3}}溶液,产生沉淀的质量与滴加\ce{Na_{2}CO_{3}}溶液的质量关系如图所示。
回答下列问题。
(1)C点对应溶液的溶质是______(填化学式)。
(2)a=______。
(3) 计算融雪剂样品中\ce{NaCl}的质量分数。(写出计算过程,结果精确到0.1%)
5. [2025·日照中考]
实验室里有一瓶久置的氢氧化钠固体。为测定固体中是否含有碳酸钠,某同学取4.52 g干燥后固体放入烧杯中,加入蒸馏水配成51.94 g溶液。向烧杯中逐滴加入氢氧化钡溶液,发现有白色沉淀生成。白色沉淀的质量与加入氢氧化钡溶液的质量关系如图所示。回答下列问题。
(1) 氢氧化钠固体中是否含有碳酸钠?______(选填“是”或“否”)。
(2) 恰好完全反应时,计算所得溶液中溶质的质量分数。(写出计算过程)
6. [2024·滨州中考]
黄铜(铜锌合金)是一种重要的金属材料,常用于制造轴承、齿轮等机器零件。为回收黄铜中的铜,某化学兴趣小组的同学取32.5 g黄铜样品粉末,放入烧杯中,然后逐渐加入稀硫酸至过量。剩余固体的质量与所加稀硫酸的质量关系如图所示。试计算:
(1) 黄铜样品中铜的质量为______ g。
(2) 恰好完全反应时,所得溶液的溶质质量分数是多少?(写出计算过程)
类型3 表格数据型
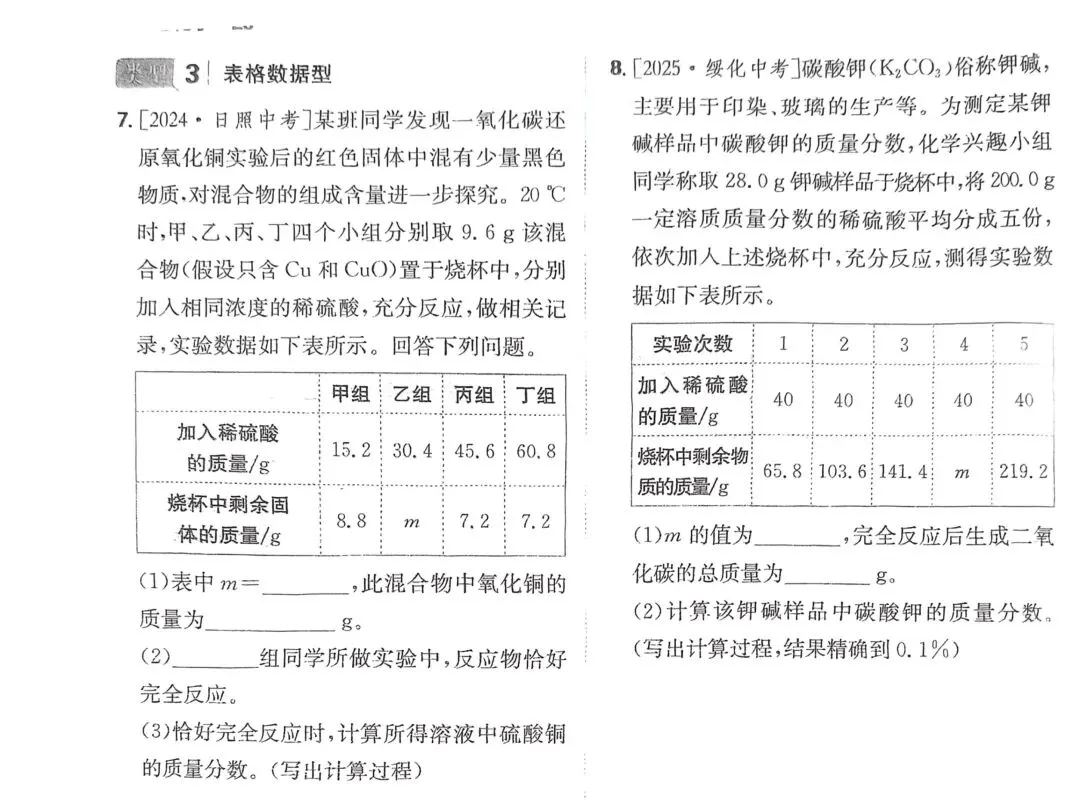
7. [2024·日照中考]
某班同学发现一氧化碳还原氧化铜实验后的红色固体中混有少量黑色物质,对混合物的组成含量进一步探究。20 ℃时,甲、乙、丙、丁四个小组分别取9.6 g该混合物(假设只含\ce{Cu}和\ce{CuO})置于烧杯中,分别加入相同浓度的稀硫酸,充分反应,做相关记录,实验数据如下表所示。回答下列问题。
甲组 乙组 丙组 丁组
加入稀硫酸的质量/g 15.2 30.4 45.6 60.8
烧杯中剩余固体的质量/g 8.8 7.2 7.2
(1) 表中m=,此混合物中氧化铜的质量为 g。
(2) ______组同学所做实验中,反应物恰好完全反应。
(3) 恰好完全反应时,计算所得溶液中硫酸铜的质量分数。(写出计算过程)
8. [2025·绥化中考]
碳酸钾(\ce{K_{2}CO_{3}})俗称钾碱,主要用于印染、玻璃的生产等。为测定某钾碱样品中碳酸钾的质量分数,化学兴趣小组同学称取28.0 g钾碱样品于烧杯中,将200.0 g一定溶质质量分数的稀硫酸平均分成五份,依次加入上述烧杯中,充分反应,测得实验数据如下表所示。
实验次数 1 2 3 4 5
加入稀硫酸的质量/g 40 40 40 40 40
烧杯中剩余物质的质量/g 65.8 103.6 141.4 219.2
(1)m的值为______,完全反应后生成二氧化碳的总质量为______ g。
(2) 计算该钾碱样品中碳酸钾的质量分数。(写出计算过程,结果精确到0.1%)
类型4 流程图型
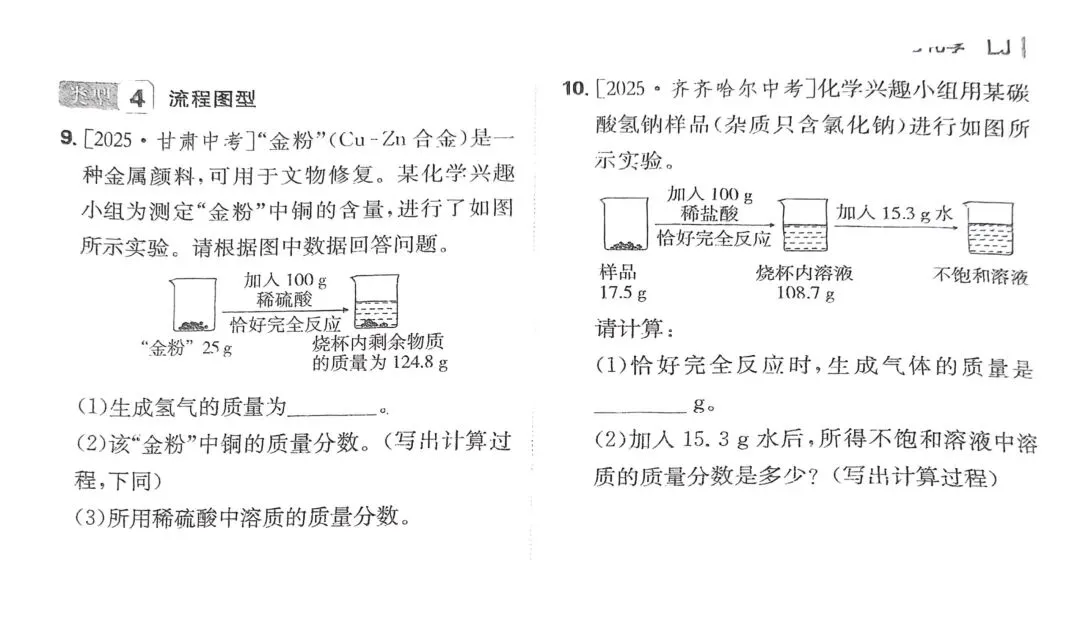
9. [2025·甘肃中考]
“金粉”(\ce{Cu-Zn}合金)是一种金属颜料,可用于文物修复。某化学兴趣小组为测定“金粉”中铜的含量,进行了如图所示实验。请根据图中数据回答问题。
(1) 生成氢气的质量为______。
(2) 该“金粉”中铜的质量分数。(写出计算过程,下同)
(3) 所用稀硫酸中溶质的质量分数。
10. [2025·齐齐哈尔中考]
化学兴趣小组用某碳酸氢钠样品(杂质只含氯化钠)进行如图所示实验。
请计算:
(1) 恰好完全反应时,生成气体的质量是______ g。
(2) 加入15.3 g水后,所得不饱和溶液中溶质的质量分数是多少?(写出计算过程)
类型5 综合型
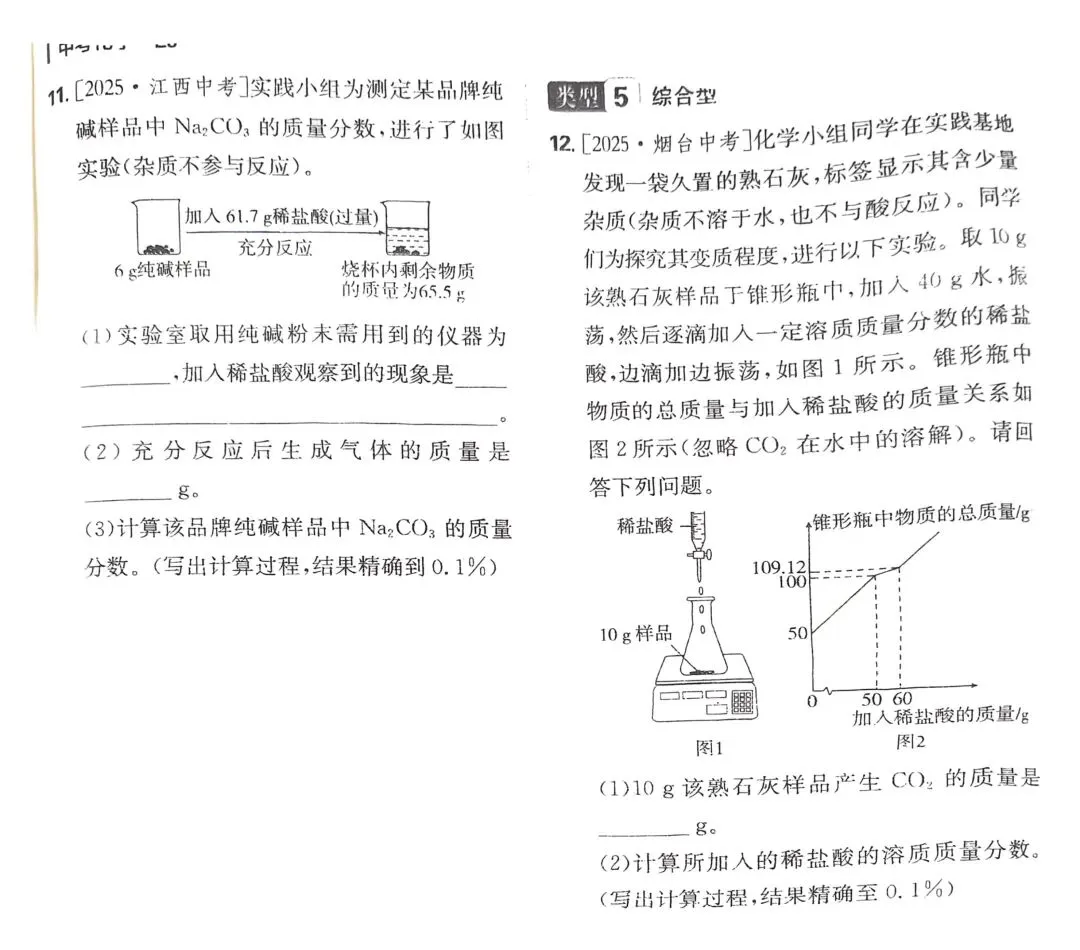
11. [2025·江西中考]
实践小组为测定某品牌纯碱样品中\ce{Na_{2}CO_{3}}的质量分数,进行了如图实验(杂质不参与反应)。
(1) 实验室取用纯碱粉末需用到的仪器为______,加入稀盐酸观察到的现象是______。
(2) 充分反应后生成气体的质量是______ g。
(3) 计算该品牌纯碱样品中\ce{Na_{2}CO_{3}}的质量分数。(写出计算过程,结果精确到0.1%)
12. [2025·烟台中考]
化学小组同学在实践基地发现一袋久置的熟石灰,标签显示其含少量杂质(杂质不溶于水,也不与酸反应)。同学们为探究其变质程度,进行以下实验。取10 g该熟石灰样品于锥形瓶中,加入40 g水,振荡,然后逐滴加入一定溶质质量分数的稀盐酸,边滴加边振荡,如图1所示。锥形瓶中物质的总质量与加入稀盐酸的质量关系如图2所示(忽略\ce{CO_{2}}在水中的溶解)。请回答下列问题。
(1) 10 g该熟石灰样品产生\ce{CO_{2}}的质量是______ g。
(2) 计算所加入的稀盐酸的溶质质量分数。(写出计算过程,结果精确至0.1%)







