




类型2 混合物成分的探究
考向1 固体成分的探究
6. [2025·福建中考]
博物院油画馆的讲解员告知同学们,油画若保存不当,其中的红铅颜料在空气中会缓慢变成白色。为探究红铅(\ce{Pb_{3}O_{4}})的变色原因,研究性学习小组开展实践活动。
[查阅资料]
①\ce{Pb_{3}O_{4}}是难溶于水的红色固体,暴露在空气中可转化为\ce{PbCO_{3}}、\ce{Pb(OH)_{2}}中的一种或两种。
②\ce{PbCO_{3}}、\ce{Pb(OH)_{2}}均为难溶于水的白色固体,均能与稀硝酸(\ce{HNO_{3}})发生复分解反应。
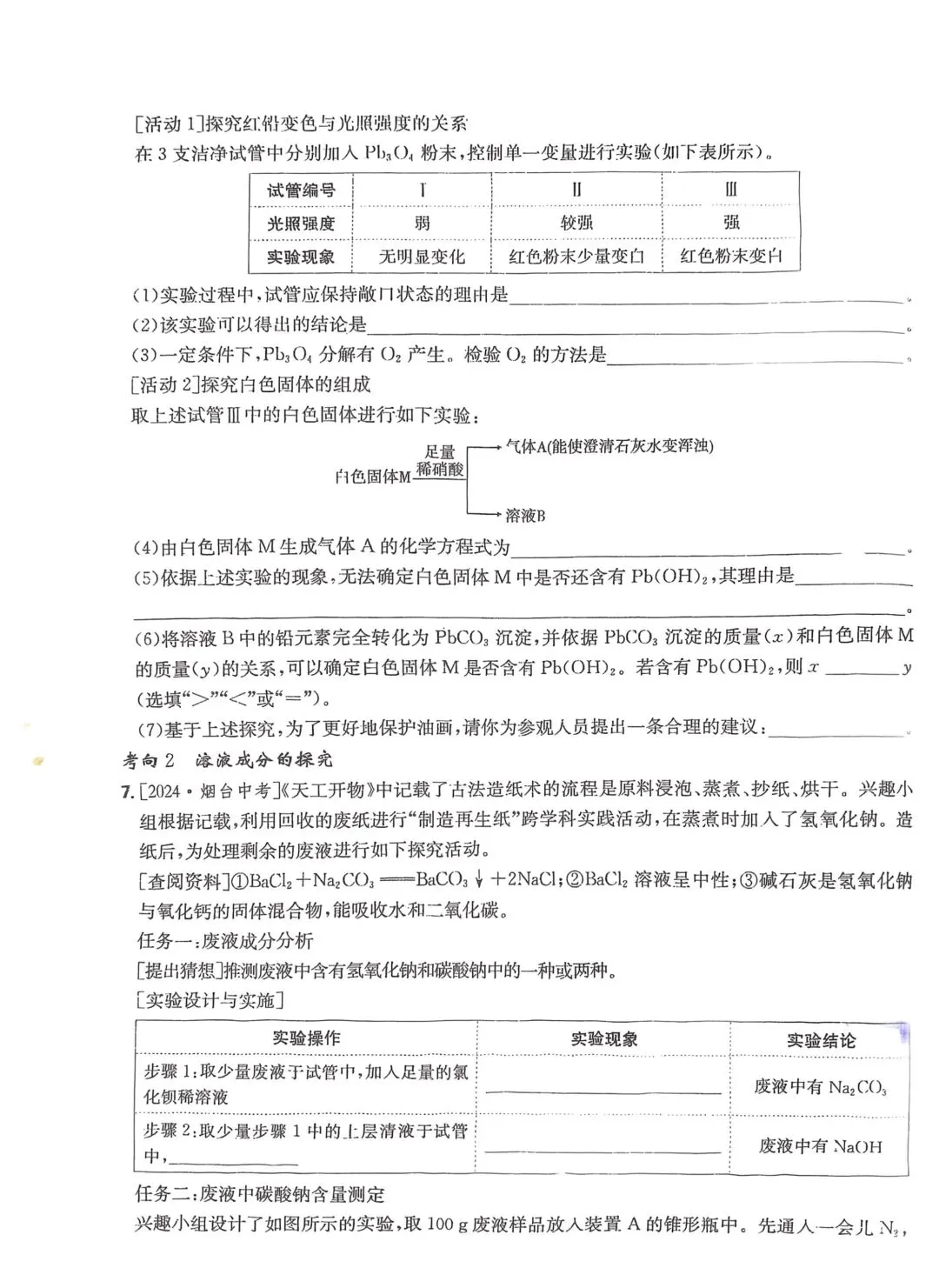
[活动1]探究红铅变色与光照强度的关系
在3支洁净试管中分别加入\ce{Pb_{3}O_{4}}粉末,控制单一变量进行实验(如下表所示)。
试管编号 Ⅰ Ⅱ Ⅲ
光照强度 弱 较强 强
实验现象 无明显变化 红色粉末少量变白 红色粉末变白
(1) 实验过程中,试管应保持敞口状态的理由是________________________。
(2) 该实验可以得出的结论是________________________。
(3) 一定条件下,\ce{Pb_{3}O_{4}}分解有\ce{O_{2}}产生。检验\ce{O_{2}}的方法是________________________。
[活动2]探究白色固体的组成
取上述试管Ⅲ中的白色固体进行如下实验:
\text{白色固体M} \xrightarrow[\text{足量}]{\text{稀硝酸}} \begin{cases} \text{气体A(能使澄清石灰水变浑浊)} \\ \text{溶液B} \end{cases}
(4) 由白色固体M生成气体A的化学方程式为________________________。
(5) 依据上述实验的现象,无法确定白色固体M中是否还含有\ce{Pb(OH)_{2}},其理由是________________________。
(6) 将溶液B中的铅元素完全转化为\ce{PbCO_{3}}沉淀,并依据\ce{PbCO_{3}}沉淀的质量(x)和白色固体M的质量(y)的关系,可以确定白色固体M是否含有\ce{Pb(OH)_{2}}。若含有\ce{Pb(OH)_{2}},则xy(选填“>”“<”或“=”)。
(7) 基于上述探究,为了更好地保护油画,请你为参观人员提出一条合理的建议:__________________。
考向2 溶液成分的探究
7. [2024·烟台中考]
《天工开物》中记载了古法造纸术的流程是原料浸泡、蒸煮、抄纸、烘干。兴趣小组根据记载,利用回收的废纸进行“制造再生纸”跨学科实践活动,在蒸煮时加入了氢氧化钠。造纸后,为处理剩余的废液进行如下探究活动。
[查阅资料]
①\ce{BaCl_{2} + Na_{2}CO_{3} = BaCO_{3}↓ + 2NaCl};
②\ce{BaCl_{2}}溶液呈中性;
③碱石灰是氢氧化钠与氧化钙的固体混合物,能吸收水和二氧化碳。
任务一:废液成分分析
[提出猜想] 推测废液中含有氢氧化钠和碳酸钠中的一种或两种。
[实验设计与实施]
实验操作 实验现象 实验结论
步骤1:取少量废液于试管中,加入足量的氯化钡稀溶液 ________________________ 废液中有
步骤2:取少量步骤1中的上层清液于试管中,________________________ ________________________ 废液中有
任务二:废液中碳酸钠含量测定
兴趣小组设计了如图所示的实验,取100 g废液样品放入装置A的锥形瓶中。先通入一会儿\ce{N_{2}},然后称量装置C、D的质量,再向锥形瓶中滴加足量稀硫酸,至不再产生气体,继续通一会儿\ce{N_{2}}后,测得装置C、D分别增重2.1 g和0.1 g。
(1) 锥形瓶中不再产生气体后,需要继续通一会儿\ce{N_{2}},其原因是________________________。
(2) 装置C中反应的化学方程式是________________________。
(3) 废液中碳酸钠的质量分数是________________________。
(4) 如果缺少装置B,会使测定的碳酸钠含量______(选填“偏大”或“偏小”)。
任务三:废液的处理
(5) 为使废液中的碳酸钠转化为氢氧化钠循环利用,需根据废液中碳酸钠的含量,加入一定量的某种物质,该物质与碳酸钠反应的化学方程式是________________________。
考向3 气体成分的探究
8. [2025·日照中考]
探究木炭和氧化铜反应生成的气体。兴趣小组将氧化铜粉末和木炭粉以质量比13.3:1混合进行实验(\ce{2CuO + C\xlongequal{高温} 2Cu + CO_{2}↑})。将生成的气体通入盛有澄清石灰水的试管中,试管中溶液先浑浊后变澄清。实验结束后称量,混合固体减少的质量大于试管增加的质量。
[查阅资料] \ce{CaCO_{3} + CO_{2} + H_{2}O = Ca(HCO_{3})_{2}},\ce{Ca(HCO_{3})_{2}}可溶于水。
(1) 任务一:探究固体减少的质量和试管增加的质量不相等的原因
[作出猜想] 木炭和氧化铜反应生成的气体:
①猜想一:只有\ce{CO_{2}};猜想二:只有\ce{CO};猜想三:。
②甲同学提出,猜想二不成立,依据是。
[实验探究1] 乙同学使用足量澄清石灰水,重复上述实验,发现固体减少的质量仍然大于试管增加的质量。
[实验结论1] ③猜想______不成立。
[实验探究2] 丙同学将氧化铜粉末与木炭粉以质量比13.3:1混合,称取0.4 g混合粉末放入W形玻璃管a处,在b处放入0.2 g氧化铜粉末,如图。a、b两处同时加热,一段时间后,发现a处固体变红,b处有少量红色固体产生。
④写出b处发生反应的化学方程式:________________________。
[实验结论2] 猜想三成立。
(2) 任务二:探究CO的来源
[作出猜想] 可能发生的化学反应:
猜想四:\ce{2CuO + C\xlongequal{高温} 2Cu + CO_{2}↑},\ce{C + CO_{2}\xlongequal{高温} 2CO};
猜想五:\ce{CuO + C\xlongequal{高温} Cu + CO↑}。
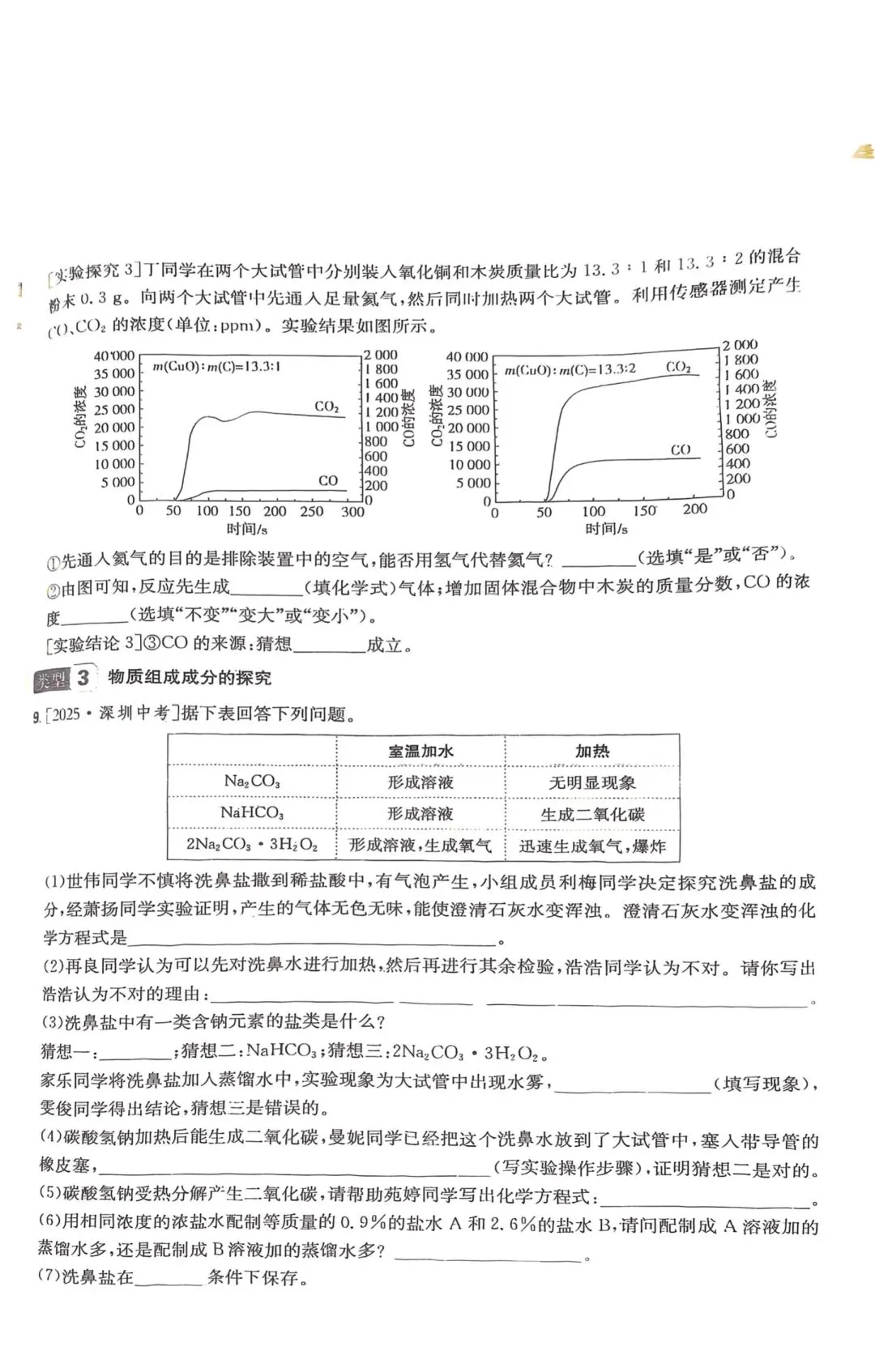
[实验探究3] 丁同学在两个大试管中分别装入氧化铜和木炭质量比为13.3:1和13.3:2的混合粉末0.3 g。向两个大试管中先通入足量氦气,然后同时加热两个大试管。利用传感器测定产生\ce{CO}、\ce{CO_{2}}的浓度(单位:ppm)。实验结果如图所示。
①先通入氦气的目的是排除装置中的空气,能否用氢气代替氦气?(选填“是”或“否”)。
②由图可知,反应先生成(填化学式)气体;增加固体混合物中木炭的质量分数,\ce{CO}的浓度______(选填“不变”“变大”或“变小”)。
[实验结论3] ③\ce{CO}的来源:猜想______成立。
类型3 物质组成成分的探究
9. [2025·深圳中考]
据下表回答下列问题。
物质 室温加水 加热
形成溶液 无明显现象
形成溶液 生成二氧化碳
形成溶液,生成氧气 迅速生成氧气,爆炸
(1) 世伟同学不慎将洗鼻盐撒到稀盐酸中,有气泡产生,小组成员利梅同学决定探究洗鼻盐的成分,经萧扬同学实验证明,产生的气体无色无味,能使澄清石灰水变浑浊。澄清石灰水变浑浊的化学方程式是________________________。
(2) 再良同学认为可以先对洗鼻水进行加热,然后再进行其余检验,浩浩同学认为不对。请你写出浩浩认为不对的理由:。
(3) 洗鼻盐中有一类含钠元素的盐类是什么?
猜想一:;猜想二:\ce{NaHCO_{3}};猜想三:\ce{2Na_{2}CO_{3}·3H_{2}O_{2}}。
家乐同学将洗鼻盐加入蒸馏水中,实验现象为大试管中出现水雾,(填写现象),爱俊同学得出结论,猜想三是错误的。
(4) 碳酸氢钠加热后能生成二氧化碳,曼妮同学已经把这个洗鼻水放到了大试管中,塞入带导管的橡皮塞,(写实验操作步骤),证明猜想二是对的。
(5) 碳酸氢钠受热分解产生二氧化碳,请帮助苑婷同学写出化学方程式:。
(6) 用相同浓度的浓盐水配制等质量的0.9\%的盐水A和2.6\%的盐水B,请问配制成A溶液加的蒸馏水多,还是配制成B溶液加的蒸馏水多?。
(7) 洗鼻盐在______条件下保存。
类型4 物质性质的探究
10. [2025·甘肃中考]
唐代《千金翼方》中记载了“枸杞以甘州者为真,叶厚大者是”,首次将甘州(今张掖)枸杞确立为道地药材。为了解张掖种植枸杞的土壤酸碱性及相关成分,某校化学兴趣小组对当地的土壤样本进行了探究。
[实验探究]
任务一:测定土壤酸碱性
(1) 选取一定量的土壤样本加入足量蒸馏水,充分搅拌后静置,过滤后得到土壤浸出液。用________________________测定浸出液的pH,若显碱性,则pH______7(选填“<”“=”或“>”)。
任务二:探究土壤中钠盐的主要成分
张掖年降水量少且蒸发量大,使土壤中较多的可溶性钠盐化合物随水分蒸发而析出。当土壤含盐量较高时,一般含有较多的氯化钠,可能含有碳酸钠。
(2) 小组同学为检验土壤样本是否含有碳酸钠(假设不含硫酸钠),进行如下实验。
实验方法 实验现象 实验结论
方法1:取少量土壤浸出液于试管中,滴加适量的________________________ 有气泡产生 含有
方法2:取少量土壤浸出液于试管中,滴加适量的氯化钙溶液 ________________________ 含有
(3) 方法2中反应的化学方程式是________________________,属于________________________(填基本反应类型)反应。
[实验结论]
(4) 以上探究表明,该土壤含有碳酸钠,显________________________(选填“酸性”“中性”或“碱性”)。该土壤除了种植枸杞,还适合种植的下表中的作物有______(填字母)。
作物 A. 茶树 B. 樱桃 C. 甘草
适宜的土壤pH 4.5~5.5 5.6~7.0 7.2~8.5
11. [2025·江西中考]
化学社团探究金属的化学性质时进行了如图所示实验。
(1) 用砂纸打磨铁片的目的是________________________。
(2) 铁与硝酸银溶液发生置换反应的化学方程式为________________________,证明铁的金属活动性比银______。
[查阅资料] 室温下,氯化银是难溶于水的白色固体;粉末状的银为黑色。
[提出问题] 在水中,铁能与溶于水的硝酸银反应,是否也能与难溶于水的氯化银反应?
[作出猜想] 猜想Ⅰ:能反应;猜想Ⅱ:不能反应。
[实验预测]
(3) 若猜想Ⅰ正确,则可观察到反应后溶液的颜色为______。
[进行实验]
(4) 取少量氯化银于烧杯中,加入蒸馏水,再加入过量的铁粉,充分搅拌,静置后液体颜色无明显变化。甲同学据此认为猜想Ⅱ正确,乙同学认为影响液体颜色变化的因素很多,液体颜色无明显变化不能说明反应没有发生。于是他们将烧杯中的物质过滤,继续实验。请完成表格中①~③处填空。
实验操作 实验现象 实验分析与结论
a. 取少量滤液于试管中,滴加硝酸银溶液 ①________________________ 滤液中含有氯化亚铁,滤渣的成分为③________________________。猜想Ⅰ正确
b. 取滤渣于另一支试管中,向其中加入足量②________________________,振荡 产生气泡,试管内有黑色固体剩余
[反思提升] 科学探究中,我们要敢于质疑、收集证据、修正错误观点,提高科学思维能力。
类型5 影响因素的探究
12. [2025·安徽中考]
学习了“常见的酸、碱、盐”后,某化学兴趣小组为探究\ce{NaHCO_{3}}和\ce{NaOH}的性质,设计并进行了如下实验。
[实验一]探究\ce{NaHCO_{3}}固体的稳定性
该小组用如图1所示装置进行实验。
(1) 实验进行一段时间后,观察到甲中________________________(填实验现象)时,证明有水生成;乙中澄清石灰水变浑浊,原因是________________________(用化学方程式表示)。
实验结论:\ce{NaHCO_{3}}固体受热能分解。
[实验二]探究\ce{NaHCO_{3}}溶液的酸碱性
取少量\ce{NaHCO_{3}}溶于试管中,向其中滴加1~2滴酚酞溶液,溶液变为红色。
(2) 实验结论:\ce{NaHCO_{3}}溶液呈______性。
[实验三]探究\ce{NaHCO_{3}}溶液的稳定性
常温下,在密闭容器(如图2)中放入盛有100 mL蒸馏水的烧杯,开启\ce{CO_{2}}传感器,测得容器内\ce{CO_{2}}浓度基本不变;将蒸馏水换成100 mL\ce{NaHCO_{3}}的稀溶液,开启\ce{CO_{2}}传感器,测得容器内\ce{CO_{2}}浓度增大。
(3) 用100 mL蒸馏水做实验的目的是________________________。
(4) 实验三的结论是________________________。
[实验四]数字化实验探究\ce{NaOH}的性质
常温下,取一定量的\ce{NaOH}溶液,分成两等份。
向一份\ce{NaOH}溶液中滴入稀盐酸,用pH传感器测定该过程中溶液的pH变化,测定结果如图3中曲线M。
向另一份\ce{NaOH}溶液中先通入一定量的\ce{CO_{2}},充分反应后得到溶液X。再向溶液X中滴入相同质量分数的稀盐酸,同时用pH传感器测定pH变化,得到溶液的pH随盐酸体积(mL)变化曲线N(未在图3中画出)。
(5) 溶液X的pH______(选填“大于”“小于”或“等于”)A点的pH。
(6) 曲线N上横坐标为10时,对应溶液中的溶质是________________________(填化学式)。
13. [2025·山东中考]
暖身贴可持续发热,能用于身体局部热敷。某品牌暖身贴的发热包内含有铁粉、活性炭、吸水树脂(具有吸水、保水功能)、盐。兴趣小组对发热包的发热原理开展探究活动。
(1) 验证发热包中含有铁粉
将未使用的发热包中原料取出,进行实验。
步骤 操作 现象 结论
Ⅰ 将磁体靠近原料 部分黑色粉末被磁体吸引
Ⅱ 将磁体吸引的黑色粉末加入试管内,加入适量________________________,振荡 黑色粉末溶解,产生气泡,溶液变成浅绿色 原料中含有铁粉
(2) 探究发热包的发热原理
打开使用后的发热包,发现其中有红色物质,同学们猜想发热包的发热原理可能与铁钉(含Fe、C等)生锈的原理相同。利用图1所示装置(夹持装置已略去)进行实验。
步骤Ⅰ:组装好仪器后,需进行的操作为________________________。
步骤Ⅱ:向三颈烧瓶内加入一定量铁粉、活性炭和氯化钠,向注射器内加入少量蒸馏水。
步骤Ⅲ:进行以下操作,测得装置内\ce{O_{2}}的体积分数和温度变化如图2所示,正确的操作顺序为________________________(用①②③④表示)。
①推动注射器,向装置内注入蒸馏水,静置1000 s。
②打开止水夹a、b,向装置内迅速充满干燥的空气,关闭止水夹a、b,静置1000 s。
③打开止水夹a、b,向装置内迅速充满干燥的\ce{CO_{2}},关闭止水夹a、b,静置1000 s。
④打开止水夹a、b,向装置内迅速充满干燥的\ce{O_{2}},关闭止水夹a、b,静置1000 s。
由实验可知,发热包的发热原理与铁钉生锈的原理________________________(选填“相同”或“不同”)。






